Número Atual: Janeiro-Março 2017 - Volume 1 - Número 1
- Imprimir
- Indicar
- Estatísticas
- (0)
Comentários - Como Citar
- Download da Citação
- Artigos Relacionados
-
Outros dos
Autores
ARTIGO ESPECIAL
Vacina rotavírus: segurança e alergia alimentar - Posicionamento das Sociedades Brasileiras de Alergia e Imunologia (ASBAI), Imunizações (SBIm) e Pediatria (SBP)
Rotavirus vaccine: safety and food allergy - Position paper of the Brazilian Societies of Allergy and Immunology (ASBAI), Immunizations (SBIm), and Pediatrics (SBP)
Renato A. Kfouri1,2; Juarez Cunha2; Emanuel C. Sarinho1,3; Dirceu Solé1,3; Eduardo Jorge da Fonseca Lima1; Renata R. Cocco3; Fátima R. Fernandes3; Ana Karolina B. B. Marinho3; Luciana R. Silva1; Norma de Paula M. Rubini3
DOI: 10.5935/2526-5393.20170006
1. Sociedade Brasileira de Pediatria (SBP)
2. Sociedade Brasileira de Imunizaçoes (SBIm)
3. Associaçao Brasileira de Alergia de Imunologia (ASBAI)
Endereço para correspondência:
Renato de Avila Kfouri
E-mail: renatokfouri@uol.com.br
Submetido em: 10/01/2017
Aceito em: 15/02/2017
Nao foram declarados conflitos de interesse associados à publicaçao deste artigo.
RESUMO
O rotavírus continua sendo o principal agente causador de diarreia na criança, a despeito da ampla utilizaçao de vacinas nos programas públicos de vacinaçao em todo o mundo. No Brasil, a vacina monovalente foi introduzida no Programa Nacional de Imunizaçoes (PNI) em 2006, e a segurança da vacina está bem documentada em diferentes estudos pré e pós-licenciamento. Embora nao haja nenhuma associaçao entre o uso da vacina rotavírus e o desenvolvimento da alergia às proteínas do leite de vaca (APLV), existe o receio, por parte de alguns pediatras e familiares, da vacina estar relacionada ao surgimento ou desencadeamento desta reaçao de hipersensibilidade. Este artigo faz uma revisao dos dados de segurança da vacina e aborda aspectos imunológicos das reaçoes de hipersensibilidade, demonstrando nao haver nexo causal entre a vacina e a APLV, reforçando o posicionamento e recomendaçoes de organismos nacionais, internacionais e das sociedades científicas.
Descritores: Vacina, rotavírus, alergia alimentar, eventos adversos.
INTRODUÇAO
Sao frequentes os questionamentos de médicos e familiares sobre a utilizaçao da vacina rotavírus, especialmente no que se refere à sua eficácia e segurança, com particular atençao às crianças com quadros de alergia alimentar, em particular aquelas com diagnóstico ou suspeita de alergia às proteínas do leite de vaca (APLV).
As Sociedades Brasileiras de Imunizaçoes (SBIm), de Alergia e Imunologia (ASBAI) e de Pediatria (SBP) - por seus Departamentos Científicos de Imunizaçoes, Alergia e Alergia alimentar - fazem aqui uma breve revisao da literatura sobre a doença rotavírus, as vacinas hoje licenciadas e a importância de sua utilizaçao, além de abordar aspectos sobre alergia alimentar, com o objetivo de esclarecer e orientar o profissional da saúde, especialmente o pediatra, para uma adequada orientaçao.
SOBRE O ROTAVIRUS
A diarreia causada por rotavírus representa um grave problema de saúde pública. Segundo a Organizaçao Mundial da Saúde (OMS), a infecçao por esse agente é a mais comum causa de diarreia em crianças menores de cinco anos em todo o mundo, sendo responsável por aproximadamente 600 mil mortes por ano e 40% das hospitalizaçoes por gastroenterites1. Apenas no continente americano, estima-se que ocorram ao redor de 75 mil internaçoes e 15 mil óbitos anualmente relacionados à doença. Atinge tantos países ricos como pobres e em desenvolvimento, sendo, portanto, uma questao mundial com grande impacto na mortalidade e morbidade infantil1,2. Desde 2009, a OMS estabeleceu uma rede mundial de vigilância sentinela de doenças diarreicas bacterianas invasivas e de rotavírus1,2.
O prolongamento para diarreia persistente nao é raro, podendo determinar a necessidade do uso de fórmulas especiais, o que encarece ainda mais o tratamento, especialmente no âmbito da saúde pública.
SOBRE AS VACINAS ROTAVIRUS
A vacina rotavírus é recomendada pela OMS e utilizada em 89 países de todos os continentes em seus calendários de vacinaçao1.
Existem duas vacinas disponíveis: uma monovalente (Rotarixr/GSK), administrada em duas doses, adotada pelo Programa Nacional de Imunizaçoes (PNI) do Brasil desde 2006, e outra, pentavalente (RotaTeqr/Merck), com esquema de três doses, disponível somente na rede privada2,3.
Inúmeros estudos de efetividade têm demonstrado um grande impacto na reduçao de hospitalizaçoes e óbitos relacionados a este agente em diferentes cenários epidemiológicos4. Estudo sobre o impacto da adoçao da vacina no Brasil evidenciou uma reduçao de 40 mil hospitalizaçoes por diarreia aguda entre crianças menores de 5 anos, mesmo em regioes de melhor condiçao social (ano 2009); - declínio de 22% na mortalidade por diarreia, com cerca de 200 mortes evitadas5.
Outros estudos já demonstraram que em locais com alta cobertura vacinal há proteçao estendida para faixas etárias maiores, incluindo idosos, pela chamada proteçao indireta ou "efeito rebanho"4.
Costa e cols. avaliaram as mortes e hospitalizaçoes por diarreia em menores de 5 anos após a introduçao da vacina no Brasil, e observaram6:
- diminuiçao de 20,9% nos óbitos por gastroenterite (GE) em menores de 5 anos;
- diminuiçao de 57,1% nos óbitos hospitalares por GE em menores de 5 anos;
- diminuiçao de 26,6% em hospitalizaçoes por GE em menores de 5 anos;
- evidência de efeitos diretos e indiretos.
Em outro estudo, Fernandes e cols. avaliaram o impacto da vacinaçao em hospitalizaçoes por rotavírus em Sao Paulo, e demonstraram7:
- diminuiçao de hospitalizaçao por diarreia em 40% em menores de 5 anos;
- diminuiçao de hospitalizaçao por diarreia em 50% em lactentes;
- economia de US$ 2 milhoes/ano para o Estado de Sao Paulo.
SEGURANÇA DAS VACINAS ROTAVIRUS: MONOVALENTE E PENTAVALENTE
Os eventos adversos mais comuns das vacinas rotavírus sao: irritabilidade, febre, vômitos e diarreia, o que pode ser também atribuído às vacinas que sao aplicadas simultaneamente no calendário vacinal da criança8.
Na fase de pesquisa clínica, cerca de 1.400 crianças foram estudadas, em diversos estados americanos. Nao houve diferença nos eventos adversos para os dois tipos de vacinas. O evento adverso mais relatado entre todos os grupos foi irritabilidade, e cerca de 10% a 15% apresentaram febre, diarreia e vômitos, todos autolimitados. Durante o estudo, 70 bebês foram hospitalizados, mas apenas uma dessas hospitalizaçoes foi atribuída à vacina. Foi de um bebê de 2 meses, internado por 48 horas, 5 dias após a primeira dose, com um quadro de gastroenterite, que se resolveu sem nenhuma sequela9.
Além disso, sangue nas fezes foi relatado em 33 pacientes, e, entre estes, 14 supostamente atribuídos à vacina, todos resolvidos sem sequelas. Um caso de invaginaçao intestinal foi relatado 91 dias após a última dose, nao tendo sido relacionado à vacina8,9. Outros eventos adversos gastrintestinais relatados com as vacinas foram: flatulência em 2,2%, e hematoquezia em 0,6%8,9.
A hematoquezia em si é um evento adverso raro, na maioria das vezes os casos têm resoluçao benigna e sao autolimitados, nao sendo fator para contraindicar doses subsequentes, entretanto deve ser acompanhada de perto pelo Pediatra até a sua resoluçao e ter conduta terapêutica individualizada, sempre considerando outros fatores associados (histórico pessoal e/ou familiar de alergias, exposiçao alimentar)2,8.
Mais de 60.000 crianças participaram dos estudos de fase III, pré-licienciamento, de cada uma das vacinas, demonstrando novamente a eficácia e o perfil de segurança das vacinas rotavírus9.
INTUSSUSCEPÇAO E A VACINA
Em 1999, a vacina RotaShieldr/Pfizer, primeira vacina contra o rotavírus licenciada no mercado norte americano, teve seu uso suspenso após a detecçao de aumento de casos de invaginaçao (intussuscepçao) intestinal - na fase de vigilância pós-comercializaçao. Como consequência, aumentou-se o rigor nos testes clínicos pré e pós-comercializaçao das novas vacinas rotavírus10.
Em 2011, Patel e cols., em estudo de vigilância pós-vacinaçao no México e no Brasil, demonstraram aumento dos casos de invaginaçao intestinal após a introduçao da vacina monovalente, de 1 caso a cada 51.000-68.000 bebês vacinados. Houve uma morte no México e duas no Brasil por invaginaçao até 7 dias após a vacina, principalmente após a segunda dose. Porém, a vacina preveniu em torno de 80.000 hospitalizaçoes e 1.300 mortes a cada ano nos dois países, o que conclui que a sua efetividade supera um eventual risco de invaginaçao intestinal ou morte entre os vacinados11.
Fernandes e cols., em outro estudo de vigilância, observaram que os casos de intussuscepçao em 2007 (n = 26) e 2008 (n = 19) nao foram maiores que a média anual (31, faixa de 24-42) durante os anos-base de 2001-2005. Os autores sugerem que embora nao tenha sido observado aumento de intussuscepçao no período, a vigilância desse agravo era fundamental e deveria ser reforçada12.
Importante ressaltar que o pediatra deve estar atento a essas consideraçoes, sempre avaliando o risco/benefício e notificando qualquer suspeita de evento adverso relacionado às vacinas, às Secretarias Estaduais ou à Agência Nacional de Vigilância Sanitária (ANVISA)13.
CONTRAINDICAÇOES E PRECAUÇOES DAS VACINAS ROTAVIRUS14-16
Sao contraindicaçoes para a utilizaçao das vacinas rotavírus:
- alergia grave em dose prévia;
- alergia a um dos componentes da vacina;
- lactentes com suspeita ou diagnóstico de imunodeficiência;
- história prévia de intussuscepçao;
- malformaçoes intestinais.
Sao consideradas precauçoes para o uso das vacinas rotavírus:
- doença aguda moderada ou grave com ou sem febre;
- outras imunodeficiências;
- doenças gastrintestinais (GI) crônicas;
- malformaçoes congênitas intestinais e urinárias, como espinha bífida e extrofia de bexiga.
SOBRE ALERGIA ALIMENTAR
Alergia alimentar é o termo reservado às reaçoes adversas a alimentos consequentes a uma resposta imunológica anômala à ingestao de um determinado alimento17. Segundo o mecanismo imunológico envolvido, pode ser classificada em mediada por IgE, nao mediada por IgE e mistas, o que determina as manifestaçoes clínicas pelas quais a alergia se manifesta17,18.
Embora o trato gastrintestinal (TGI) receba grande quantidade de proteínas alimentares potencialmente alergênicas, a maioria das crianças nao desenvolve alergia alimentar19. Predisposiçao genética e uma série de fatores ambientais (epigenética) contribuem para que haja uma quebra da tolerância oral (TO) e consequentemente o aparecimento dos sintomas relacionados20. A TO é definida como um estado de ausência de reatividade local e sistêmica do sistema imunológico quando em contato com antígenos administrados por via oral20. A microbiota intestinal exerce importante papel neste processo. A perda da TO é o primeiro passo para o desenvolvimento da alergia alimentar20,21.
Entre os fatores ambientais identificados como fatores de risco para a quebra da TO, encontramos: gênero, etnia, presença de polimorfismos genéticos, mudanças na dieta (vitamina D, tipo de gordura, antioxidantes, obesidade), hipótese da higiene (reduçao de exposiçao a agentes infecciosos, parasitas, tipo de colonizaçao intestinal), exposiçao a alérgenos alimentares antes dos 4 meses de vida e sensibilizaçao por via cutânea apresentam destaque na investigaçao científica22.
Os principais alimentos envolvidos na alergia alimentar sao: leite de vaca (LV), soja, trigo, ovo, amendoim, peixes e crustáceos. Entre os lactentes predomina a alergia às proteínas do leite de vaca (APLV)23. A real dimensao da APLV no Brasil é desconhecida. Estudo observacional revelou ser 5,4% a prevalência de suspeita de ALPV entre crianças com sintomas gastroenterológicos, e 2,2% a incidência24.
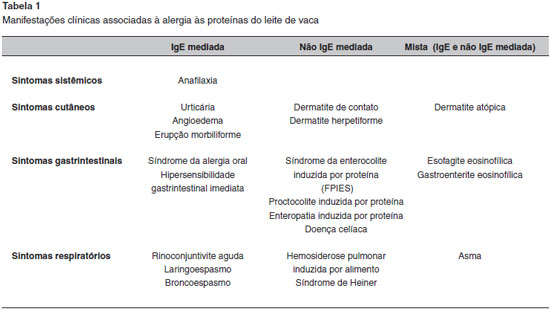
As manifestaçoes clínicas da alergia alimentar, como a APLV, sao dependentes do mecanismo imunológico envolvido. As reaçoes mediadas por IgE sao de início rápido (urticária, angioedema, vômitos, diarreia, broncoespasmo agudo e choque anafilático), em até duas horas após exposiçao ao alérgeno25,26. As nao mediadas por IgE (possivelmente linfócitos T) geralmente se manifestam com sintomas tardios, envolvendo preferencialmente o trato gastrintestinal (coloproctite, proctite ou proctocolite eosinofílica alérgica, enterocolite induzida por proteína e a hemossiderose pulmonar)26. Alergias mistas decorrem da associaçao de mecanismo IgE dependente e nao IgE dependente. Sao exemplos: esofagite eosinofílica, a gastroenteropatia eosinofílica, a dermatite atópica e mais raramente, asma (Tabela 1).
As formas nao mediadas por IgE sao mediadas por células T e em boa parte dos casos apresentam história natural efêmera, ou seja, a tolerância imunológica ocorre nos primeiros anos de vida26,27.
Importante ressaltar que a permeabilidade intestinal permanece aumentada por período variável após o nascimento, e favorece a absorçao de antígenos que modulam a resposta imunológica. Neste período, a formaçao adequada do microbioma e o aleitamento materno constituem importantes moduladores para a formaçao de uma microflora adequada28,29.
ASSOCIAÇAO ENTRE VACINA ROTAVIRUS E APLV
Nao há estudos publicados que demonstrem aumento ou desencadeamento de APLV em crianças vacinadas contra o rotavírus. Lactentes que apresentam quadro de APLV com doença diarreica moderada ou grave ou vômitos, devem ter a aplicaçao da vacina adiada até a recuperaçao geral14.
A vacina pode, raramente, causar sangue nas fezes (hematoquezia) pela hiperplasia nodular linfoide, resultante de colite crônica inespecífica8.
A rigor a doença causada pelo RV historicamente nunca esteve associada à APLV, mas, eventualmente, houve relatos de casos de diarreia prolongada em algumas crianças em que o RV causou extensa destruiçao das vilosidades intestinais, com reduçao da atividade da lactase, que voltou à normalidade após recuperaçao do epitélio intestinal.
Ambas as vacinas sao compostas por vírus vivo atenuado, incapazes de causar doença, nao havendo relaçao com o desenvolvimento de APLV. Por outro lado, nos últimos 10 anos, a ampliaçao do conhecimento e uso de exames diagnósticos para APLV têm contribuído para maior número de casos suspeitos e diagnosticados. Além disso, a idade em que a vacina é realizada coincide com a idade de maior diagnóstico da APLV, podendo aí haver forte coincidência temporal de fatores envolvidos, associados ao fato de que as alergias alimentares estao aumentando em número, mesmo antes da introduçao da vacina rotavírus, em 200630.
Pacientes que apresentaram reaçao alérgica ameaçadora à vida relacionada a algum componente vacinal e aqueles com reaçao alérgica grave ao látex, nao devem receber esta vacina31.
No 12th Annual International Rotavirus Symposium, realizado em setembro de 2016, (com participaçao de orgaos como Center for Diseases and Control - CDC, Instituto Sabin, Fundaçao Bill & Melinda Gates, entre outros), em momento algum se estabelece uma relaçao vacina rotavírus e APLV32.
Posicionamento da Organizaçao Pan-americana da Saúde (OPAS), Organizaçao Mundial da Saúde (OMS) e Ministério da Saúde (MS) sobre o assunto:
"Tem circulado nas redes sociais informaçoes falsas sobre a vacina rotavírus humano (VORH) atenuada estar desencadeando alergia às proteínas do leite de vaca nas crianças vacinadas. A Organizaçao Pan-Americana da Saúde (OPAS/OMS) endossa o posicionamento do Ministério da Saúde brasileiro ao esclarecer que essa vacina nao contém a proteína do leite de vaca em sua composiçao. Tampouco há evidências científicas do desenvolvimento de alergia ao leite desse animal após a administraçao do produto, conforme constatado pelos laboratórios Biomanguinhos e GSK (responsáveis pela produçao da vacina distribuída no Brasil)"33.
RECOMENDAÇOES
A OMS em seu último position paper sobre a vacina rotavírus mantém a recomendaçao da vacinaçao universal1.
CALENDARIOS
Ministério da Saúde
Vacina rotavírus humano: administrar 2 doses, aos 2 e 4 meses de idade. A primeira dose pode ser administrada a partir de 1 mês e 15 dias até 3 meses e 15 dias. A segunda dose pode ser administrada a partir de 3 meses e 15 dias até 7 meses e 29 dias. Manter intervalo mínimo de 30 dias entre as doses. Se a criança regurgitar, cuspir ou vomitar após a vacinaçao, nao repetir a dose34.
Sociedade Brasileira de Imunizaçoes (SBIm)
Vacina rotavírus monovalente RV1: duas doses, idealmente aos 2 e 4 meses de idade. Vacina rotavírus pentavalente RV5: três doses, idealmente aos 2, 4 e 6 meses de idade. Para ambas as vacinas, a primeira dose pode ser feita a partir de 6 semanas de vida e no máximo até 3 meses e 15 dias, e a última dose até 7 meses e 29 dias. O intervalo mínimo entre as doses é de 30 dias. Se a criança cuspir, regurgitar ou vomitar após a vacinaçao, nao repetir a dose. Nao utilizar em crianças hospitalizadas. Em caso de suspeita de imunodeficiência ou RNs cujas maes fizeram uso de biológicos durante a gestaçao, a vacina pode estar contraindicada e seu uso deve ser avaliado pelo médico (consulte os Calendários de vacinaçao SBIm pacientes especiais)35.
Sociedade Brasileira de Pediatria
Rotavírus - existem duas vacinas licenciadas. A vacina monovalente incluída no PNI, indicada em duas doses, seguindo os limites de faixa etária: primeira dose aos 2 meses (limites de 1 mês e 15 dias até, no máximo, 3 meses e 15 dias) e a segunda dose aos 4 meses (limites de 3 meses e 15 dias até no máximo 7 meses e 29 dias). A vacina pentavalente, disponível na rede privada, é recomendada em três doses, aos 2, 4 e 6 meses. A primeira dose deverá ser administrada no máximo até 3 meses e 15 dias e a terceira dose deverá ser administrada até 7 meses e 29 dias. O intervalo mínimo é de quatro semanas entre as doses. Se a criança regurgitar, cuspir ou vomitar durante a administraçao da vacina ou depois dela, a dose nao deve ser repetida. Recomenda-se completar o esquema com a vacina do mesmo laboratório produtor36.
CONCLUSAO
As Sociedades Brasileiras de Alergia e Imunologia (ASBAI), Imunizaçoes (SBIm) e de Pediatria (SBP - Departamentos de Imunizaçoes e Alergia) reafirmam a eficácia e a segurança das vacinas rotavírus e recomendam o uso rotineiro no calendário vacinal da criança, face à grande importância e impacto que a doença tem na saúde infantil.
REFERENCIAS
1. World Health Organization (WHO). Rotavirus vaccines WHO position paper - January 2013. Wkly Epidemiol Rec. 2013; 88:49. Disponível em: http://www.who.int/wer/2013/wer8805.pdf?ua=1. Acessado em 15 de outubro de 2016.
2. Rota Council. Rotavirus: common, severe, devastating, preventable. The latest evidence & what's needed to stop illnesses and deaths. February 2016. Disponível em: http://rotacouncil.org/resources/White-paper-FINAL-v2.pdf. Acessado em 18 de outubro de 2016.
3. Centers for Disease Control and Prevention. Epidemiology and Prevention of Vaccine-Preventable Diseases. The Pink Book: Course Textbook - 13th Edition (2015).
4. Centers for Disease Control and Prevention. MMWR. Sustained Decrease in Laboratory Detection of Rotavirus after Implementation of Routine Vaccination - United States, 2000-2014. April 10, 2015 / 64(13);337-342. Disponível em: https://www.cdc.gov/mmwr/preview/mmwrhtml/mm6413a1.htm. Acessado em 15 de outubro de 2016.
5. do Carmo GM, Yen C, Cortes J, Siqueira AA, de Oliveira WK, Cortez-Escalante JJ, et al. Decline in Diarrhea Mortality and Admissions after Routine Childhood Rotavirus Immunization in Brazil: A Time-Series Analysis. PLosMed. 2011;Apr;8(4):e1001024.
6. Costa I, Linhares AC, Cunha MH, Tuboi S, Argüello DF, Justino MC, et al. Sustained Decrease in Gastroenteritis-related Deaths and Hospitalizations in Children Less Than 5 Years of Age After the Introduction of Rotavirus Vaccination: A Time-Trend Analysis in Brazil (2001-2010), Pediatr Infect Dis J. 2016;35(6):e180-90.
7. Fernandes EG, Sato HK, Leshem E, Flannery B, Konstantyner TC, Veras MA, et al. Impact of rotavirus vaccination on diarrhea-related hospitalizations in Sao Paulo State, Brazil. Vaccine. 2014;5;32(27):3402-8.
8. Centers for Disease Control and Prevention. Rotavirus Vaccine Safety. Disponível em: http://www.cdc.gov/vaccinesafety/vaccines/rotavirus-vaccine.html. Acessado em 20 de outubro de 2016.
9. Yen C, Healy K, Tate JE, Parashar UD, Bines J, Neuzil K, et al. Rotavirus vaccination and intussusception - Science, surveillance, and safety: A review of evidence and recommendations for future research priorities in low and middle income countries. Hum Vaccin Immunother. 2016;12(10):2580-9.
10. Advisory Committee on Immunization Practices: vaccines for children program vaccines to prevent rotavirus gastroenteritis. Disponível em: https://www.cdc.gov/vaccines/programs/vfc/downloads/resolutions/0608-rotavirus.pdf. Acessado em 25 de outubro de 2016.
11. Patel MM, López-Collada VR, Bulhoes MM, De Oliveira LH, Bautista Márquez A, Flannery B, et al. Intussusception risk and health benefits of rotavirus vaccination in Mexico and Brazil. N Eng J Med. 2011;364:2283-92.
12. Fernandes EG, Leshem E, Patel M, Flannery B, Pellini AC, Veras MA, et al. Hospital-based surveillance of intussusception among infants. J Pediatr (Rio J). 2016;92:181-7.
13. Notificaçao de eventos adversos em vacinas, Anvisa. Disponível em: http://portal.anvisa.gov.br/servicos/form/farmaco/notificacao_usu.pdf. Acessado em 30 de setembro de 2016.
14. Wang CM, Chen SC, Chen KT. Current status of rotavirus vaccines. World J Pediatr. 2015;11(4):300-8.
15. Centers for Disease Control and Prevention. Addition of History of Intussusception as a Contraindication for Rotavirus Vaccination. MMWR, October 21, 2011, Vol. 60, #41. Disponível em: https://www.cdc.gov/mmwr/preview/mmwrhtml/mm6041a5.htm. Acessado em 12 de novembro de 2016.
16. Centers for Disease Control and Prevention. Addition of Severe Combined Immunodeficiency as a Contraindication for Administration of Rotavirus Vaccine. MMWR, June 11, 2010, Vol. 59, #22. Disponível em: https://www.cdc.gov/mmwr/preview/mmwrhtml/mm5922a3.htm. Acessado em 21 de novembro de 2016.
17. Fiochi A, Brozek J, Schünemann H, Bahna SL, von Berg A, Beyer K, et al. World Allergy Organization (WAO) diagnosis and rationale for action against cow's milk allergy (DRACMA) guidelines. Pediatr Allergy Immunol. 2010;21(Sup21):1-125.
18. Solé D, Amancio OMS, Jacob CM, Cocco RR, Sarni ROS, Suano F, et al. Guia Prático de diagnóstico e tratamento da Alergia as Proteínas do Leite de Vaca mediada pela imunoglobulina E. Rev Bras Alerg Imunopatol. 2012;35(6):203-33.
19. Jacob CMA, Pastorino AC. Manejo da alergia ao leite de vaca. In: Solé D, Bernd LAG, Rosario Filho NA, eds. Tratado de Alergia e Imunologia clínica. 1ª ed. Sao Paulo: Atheneu; 2011. p. 357-65.
20. Gupta RS, Springston EE, Warrier MR, Smith B, Kumar R, Pongracic J, et al. The prevalence, severity, and distribution of childhood food allergy in the United States. Pediatrics. 2011;128(1):e9-17.
21. Pabst O, Mowat AM. Oral tolerance to food protein. Mucosal Immunol. 2012;5:232-39.
22. Lack G. Update on risk factors for food allergy. J Allergy Clin Immunol. 2012;129:1187-97.
23. Mallozi MC, Cocco RR. Alergia a alimentos. In: Solé D, Bernd LAG, Rosario Filho NA, eds. Tratado de Alergia e Imunologia clínica. 1a ed. Sao Paulo: Atheneu; 2011. p. 345-65.
24. Vieira MC, Morais MB, Spolidoro JV, Toporovski MS, Cardoso AL, Araujo GT, et al. A survey on clinical presentation and nutritional status of infants with suspected cow's Milk allergy. BMC Pediatrics. 2010,10:25.
25. Motta MEFA, et al. Intolerância ou alergia à proteína do leite de vaca. In: Sarinho ESC, Alves JGB. Alergia e Imunologia na Criança e no Adolescente. 1ªed. Rio de Janeiro: IMIP, Medbook; 2013.
26. Sampson HA, Aceves S, Bock SA, James J, Jones S, Lang D, et al. Food allergy: A practice parameter update-2014. J Allergy Clin Immunol. 2014;134:1016-25.
27. Sampson HA. Food allergy: Past, present and future. Allergol Int. 2016;65(4):363-9.
28. Pozzo-Rubio T, de Palma G, Mujico JR, Olivares M, Marcos A, Acuña MD, et al. Influence of early environmental factors on lymphocyte subsets and gut microbiota in infants at risk of celiac disease; the PROFICEL study. Nutri Hosp. 2013;28(2):464-73.
29. Ang Li, Arboleya S, Lihua G, Chuihui Y, Nan Q, Suarez M, et al. The establishment of the infant intestinal microbiome is not affected by rotavirus vaccination. Sci Rep 4:7417 doi:10.1038/srep07417.
30. Prescott S, Allen KJ. Food allergy: Riding the second wave of the allergy epidemic. Pediatr Allergy Immunol. 2011 Mar;22(2):155-60.
31. Sarinho ECS, Chong-Neto HJ, Pastorino AC, Azoubel A, Kushnir F, Solé D, et al. Anafilaxia, Guia Prático de Atualizaçao. Departamento de Alergia, Sociedade Brasileira de Pediatria. Disponível em http://www.sbp.com.br/src/uploads/2012/12/Alergia-GuiaPratico-Anafilaxia-Final.pdf. Acessado em 10 de novembro de 2016.
32. Program for Appropriate Technology in Health (PATH). Disponível em: http://www.path.org/publications/files/CVIA_rotavirus_fs.pdf. Acessado em 30 de novembro de 2016.
33. Posicionamento OPAS/OMS. Disponível em: http://www.paho.org/bra/index.php?option=com_content&view=article&id=4925:opasoms-e-ministerio-da-saude-esclarecem-que-vacina-contra-rotavirus-nao-causa-alergia&Itemid=821. Acessado em 12 de novembro de 2016.
34. Calendário nacional de vacinaçao, Ministério da Saúde do Brasil. Disponível em: http://portalsaude.saude.gov.br/index.php/o-ministerio/principal/leia-mais-o-ministerio/197-secretaria-svs/13600-calendario-nacional-de-vacinacao . Acessado em 12 de novembro de 2016.
35. Sociedade Brasileira de Imunizaçoes (SBIm). Calendário de Vacinaçao da Criança. Disponível em: http://sbim.org.br/images/files/calend-sbim-crianca-2016-17-160914c-spread.pdf. Acessado em 12 de janeiro de 2017.
36. Sociedade Brasileira de Pediatria. Calendário de Vacinaçao 2016. Disponível em http://www.sbp.com.br/src/uploads/2016/08/Calendario-Vacinacao-2016-19out16.pdf. Acessado em 12 de janeiro de 2017.