Número Atual: Outubro-Dezembro 2024 - Volume 8 - Número 3
- Imprimir
- Indicar
- Estatísticas
- (0)
Comentários - Como Citar
- Download da Citação
- Artigos Relacionados
-
Outros dos
Autores
Comunicação Clínica e Experimental
Dessensibilização rápida à idursulfase adaptada para um paciente com Mucopolissacaridose tipo II
Rapid idursulfase desensitization tailored to a patient with mucopolysaccharidosis type II
Pietro Henrique Massuda1; Mariana Malucelli2; Mara Lucia Schmitz Ferreira Santos2; Pedro Giavina-Bianchi3; Tsukiyo Kamoi2
1. Hospital Pilar - Curitiba, PR, Brasil
2. Hospital Pequeno Príncipe - Curitiba, PR, Brasil
3. Disciplina de Imunologia Clínica e Alergia, Faculdade de Medicina da Universidade de São Paulo - São Paulo, SP, Brasil
Endereço para correspondência:
Pietro Henrique Massuda
E-mail: dr.pietromassuda@gmail.com
Submetido em: 05/11/2024
Aceito em: 12/11/2024.
Não foram declarados conflitos de interesse associados à publicação deste artigo.
RESUMO
A Mucopolissacaridose tipo II (MPS II), ou Síndrome de Hunter, é uma doença genética rara ligada ao cromossomo X, caracterizada pelo acúmulo de glicosaminoglicanos (GAGs) devido à deficiência da enzima iduronato-2-sulfatase. O tratamento padrão é a terapia de reposição enzimática (TRE) com idursulfase, que, apesar de eficaz, pode provocar reações adversas graves, incluindo anafilaxia. A dessensibilização é uma opção em casos de reações alérgicas graves quando não há terapias substitutas viáveis. Relatamos o caso de menino de 9 anos, com MPS II, que após 2 anos e 9 meses de uso de idursulfase desenvolveu reações alérgicas graves durante as infusões. Testes cutâneos indicaram uma possível reação de hipersensibilidade mediada por IgE. Após várias tentativas de ajuste da infusão e uso de pré-medicações, optou-se pela dessensibilização, utilizando protocolo baseado no descrito pela Profa. Castells. A primeira tentativa foi malsucedida, porém, após modificações no tempo de infusão e uso de pré-medicação adicional, o paciente passou a tolerar a dose completa de idursulfase semanalmente. Reações de hipersensibilidade imediata à idursulfase são comuns, e os testes cutâneos são úteis na identificação de reações mediadas por IgE. A dessensibilização demonstrou ser eficaz neste caso, evitando a suspensão do tratamento. O protocolo foi ajustado conforme a resposta do paciente, destacando a importância de abordagens individualizadas. A dessensibilização à idursulfase é uma alternativa segura e eficaz para pacientes com MPS II que apresentam reações de hipersensibilidade imediata graves à TRE. Este caso contribui para a compreensão da gestão de reações alérgicas no tratamento com idursulfase, incentivando estudos futuros para aprimorar a técnica.
Descritores: Idursulfase, mucopolissacaridose tipo II, Doença de Hunter, dessensibilização.
Introdução
As mucopolissacoridoses (MPS) são doenças genéticas raras, heterogêneas, que levam ao acúmulo de mucopolissacarídeos nos lisossomos teciduais, causando diversas manifestações sistêmicas que ocorrem com a progressão do tempo1,2. A mucopolissacaridose tipo II (MPS II) ou Síndrome de Hunter é uma doença de padrão recessivo, ligada ao cromossomo X, e que por esse motivo afeta primariamente o sexo masculino e raramente o feminino3,4. Apresenta uma prevalência que varia de 0,38 a 1,07 por 100.000 nascidos vivos5, e foi descrita pela primeira vez por Charles Hunter, em 1917, após a observação de dois irmãos6.
Nesta doença, ocorre uma alteração genética no cromossomo Xq28 que leva a níveis insuficientes da enzima iduronato-2-sulfase codificada pelo gene IDS, responsável pela degradação de glicosaminoglicanas (GAG). A ausência desta enzima leva ao acúmulo de GAG lisossomal, o que resulta em organomegalias e disfunção de sistemas como o ocular, nervoso central, esquelético, respiratório, cardíaco e gastrointestinal, podendo variar de espectros leves, muitas vezes sem déficit cognitivo, até espectros graves, com déficit cognitivo importante e possível falência de órgãos, principalmente o cardíaco7-10.
O tratamento para essa patologia por muitos anos se restringiu a tratamentos de suportivos e paliativos. Desde a descoberta das bases genéticas e fisiopatológicas da doença, conseguiu-se alterar essa realidade, introduzindo em 1980 os transplantes de medula óssea e de células hematopoiéticas e, em 2006, a terapia de reposição enzimática (TRE), que segue sendo o tratamento mais utilizado até hoje11-13.
A idursulfase (Elaprase®) fornece a enzima deficitária aos portadores de MPS II, resultando na quebra de GAGs acumulados no interior das células sendo essencial para o tratamento dessa patologia14. Está indicada para todos os pacientes sintomáticos com diagnóstico confirmado de MPS II, apesar de ainda haver algumas dúvidas sobre seus benefícios de longo prazo11,15,16. O grande problema da TRE endovenosa advém do fato de não chegar em todos os órgão afetados, principalmente o sistema nervoso central (por não atravessar a barreira hematoencefálica), e, portanto, não levar a uma melhora do comprometimento cognitivo, além de possuir uma elevada taxa de reações adversas durante as infusões, chegando à até dois terços dos pacientes, principalmente nos três primeiros meses11,17.
A maioria das reações adversas infusionais (RAI) são leves a moderadas, como o surgimento de rash, cefaleia, febre, dispepsia, urticária, angioedema, dor abdominal, rinite e em alguns casos broncoconstrição17,18. Estas são usualmente tratadas e prevenidas com uso de pré-medicações como os anti-histaminicos, antipiréticos ou corticosteroides e com mudanças na velocidade ou interrupção da infusão15,17,19. Entretanto, existem na literatura alguns relatos de anafilaxia, e o uso de adrenalina nesses casos deve ser de extrema cautela devido ao risco aumentado de doenças coronarianas nesses pacientes15,20.
As reações de hipersensibilidade nas RAI podem ocorrer por mecanismos IgE mediados e não IgE mediados. A formação de IgG e IgM e IgE anti-idursulfase, estimulo à cascata do complemento, liberação de citocinas, estímulo direto de mastócito, deposição de imunocomplexos ou estímulo de células T são todo mecanismos possíveis, porém a exata causa ainda não se encontra totalmente exclarecida11,19-24. No caso de reações de hipersensibilidade imediata (RHI) graves ou recorrentes e com falha na prevenção com uso de pré-medicações está indicado a dessensibilização19.
A dessensibilização rápida a medicamento é um tratamento utilizado para induzir um estado de hiporresponsividade do sistema imunológico a alérgenos específicos. Este tratamento envolve a administração gradual e controlada ao paciente do medicamento responsável pela reação, com o objetivo de modificar a resposta imunológica e inibir a RHI. Está indicada quando há uma RHI a um medicamento necessário e uma ausência de substitutos viáveis ou com um melhor risco-benefício25,26.
Aqui reportamos, ao nosso conhecimento, a primeira descrição de caso brasileiro de dessensibilização para idursulfase.
Relato de caso
Paciente de 9 anos, do sexo masculino, natural e procedente de Umuarama, PR, pesando 37 kg, portador de MPS tipo II diagnosticada aos 5 anos e em uso de idursulfase, semanalmente, na dose de 0,5 mg/kg desde os 5 anos e 4 meses de idade. Após 2 anos e 9 meses do início das infusões semanais (setembro de 2022), iniciou com eritema e prurido no local de aplicação da medicação, minutos após término da infusão. Desde então foram incluídas pré-medicações antes das infusões: anti-histamínico de primeira geração, corticosteroide endovenoso e anti-inflamatório não esteroidal, resultando em resolução das reações.
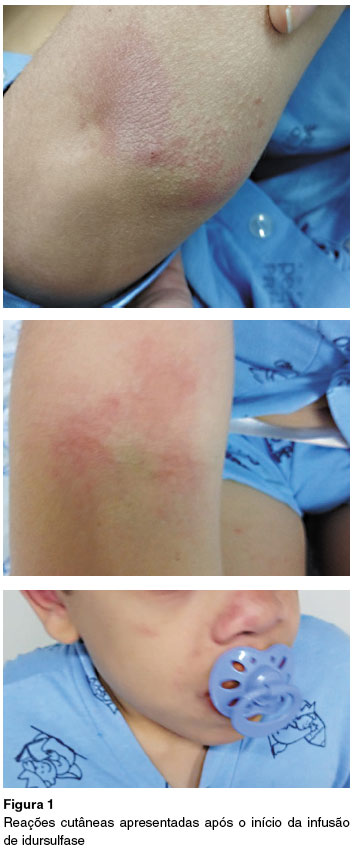
Em dezembro/2022 iniciou novamente com reação, nessa ocasião ocorrendo uma hora após início da infusão, resultando em eritema em face, membros superiores e tronco, associados a prurido local e extrema irritação. A medicação foi suspensa imediatamente, seguido de regressão das manifestações cutâneas, sem uso de outras medicações, e a infusão foi adiada para a próxima semana. Na semana seguinte, uma hora novamente após início da infusão de idursulfase, apresentou a mesma reação cutânea, com melhora espontânea após a suspensão da infusão. Não recebeu outras medicações (Figura 1).
Desde então, foram realizadas diversas tentativas para tentar infundir a medicação, com uso de pré-medicações antes e durante o processo e diminuição da velocidade de infusão até uma velocidade máxima de 50 mL/h, porém sempre com reações durante o procedimento com bastante desconforto para a família e para o paciente. Além disso, a dose necessária da medicação de 18 gramas não estava sendo alcançada, chegando a um limite máximo semanal tolerado de 6 gramas antes que a infusão necessitasse ser suspensa indefinidamente.
Em abril/2023 nossa equipe foi chamada para avaliar o caso. Primeiramente foram realizadas provas cutâneas em ambiente controlado para averiguar reação de hipersensibilidade imediata mediada (RHI) por IgE específica. Foi utilizado a prova cutânea de leitura imediata (prick test) com idursulfase na concentração de 2 mg/mL (não diluída), controle negativo (solução salina) e controle positivo (histamina). A leitura de 15 minutos após o prick foi negativa para a idursulfase e para o controle negativo e positiva para histamina (3x3 mm). Em seguida se prosseguiu para o teste intradérmico nas diluições de 1/1000 (0,002 mg/mL), 1/100 (0,02 mg/mL) e 1/10 (0,2 mg/mL) da idursulfase, com leitura 20 minutos após cada uma das concentrações. A prova de 1/10 (0,2 mg/mL) foi a única que resultou positiva, com aumento da pápula inicial em 3 mm (3x3 mm para 6x6 mm).
Observada provável reação IgE mediada ou de mecanismo misto, foi optado por realizar a dessensibilização para medicação. Como o paciente já havia tentado previamente uma infusão lenta à velocidade fixa de 50 mL/h e reagido após início da infusão, foi estabelecido o valor de 50 mL/h como o valor máximo ideal para ser atingido.
O protocolo de dessensibilização utilizado foi baseado no protocolo de Castells M. e cols.27, com utilização de três bolsas de SF 0,9% de 100 mL, onde foi diluída a medicação, com o objetivo de chegar em uma dose final total de 18 mg (posologia de 0,5 mg/kg, conforme orientações do fabricante). Foram realizados aumentos progressivos de concentração e velocidade de infusão, com aferição de dados vitais entre as etapas, de 15 em 15 minutos, até chegar na última etapa na velocidade final da bolsa 3 de 50 mL/h, quando se mantém constante a velocidade até finalizar a bolsa, conforme Tabela 1.
Após primeira tentativa de dessensibilização, precedida de pré-medicações (anti-H1 oral e corticoide oral), o paciente reagiu na velocidade de 25 mL/h da terceira bolsa (etapa 11), sendo necessário interromper a infusão. Na semana seguinte, segunda tentativa, foi realizado uma alteração no protocolo, prolongando o tempo da etapa 10 (velocidade 12,5 mL/h da terceira bolsa) para 30 minutos e inserindo pré-medicação novamente após essa etapa. Também foi prolongado o tempo para 30 minutos da etapa 11 de 25 mL/h. Após essas adaptações, o paciente não reagiu mais às infusões, sendo então mantidas essas alterações, subsequentemente tornando possível que o paciente conseguisse receber a dose total semanal de 18 mg de idulsulfase.
Discussão
Na suspeita de reação de hipersensibilidade IgE mediada, a primeira etapa para investigação consiste na realização do teste cutâneo alérgico com a medicação em questão. Para idursulfase, a positividade parece apresentar boa correlação com reações IgE mediadas. Segundo estudo de Kim J e cols., o teste cutâneo de leitura imediata com idursulfase apresentou uma sensibilidade de 66,7% e uma especificidade de 100% para sintomas IgE mediados nos pacientes testados. Do total de 34 pacientes que receberam a medicação, 3 apresentaram reações anafiláticas (8,8%) durante as infusões e o prick test para idursulfase se mostrou positivo em quatro pacientes, incluindo todos os que tiveram anafilaxia (100%). Nesse mesmo estudo também foi demonstrada a presença de IgE anti-idursulfase por meio de ELISA, que mostrou resultados acima de dois desvios padrões da média de controles saudáveis em sete pacientes com reações de hipersensibilidade20.
Foi postulado que essa sensibilização ocorre de maneira de novo devido ao elevado grau de pureza da medicação, que elimina impurezas no processo de fabricação, à falta de similaridade da sequência de aminoácidos da idursulfase com relação a outros alérgenos conhecidos, e ao tempo necessário para começar a desenvolver reações - várias infusões após o início, conforme também foi observado em nosso relato20.
Optamos pela dessensibilização com o medicamento em questão por considerar os riscos-benefícios favoráveis, para evitar descontinuação da medicação e por não haver possibilidade de substituí-la por outro fármaco com a mesma função. O protocolo realizado pode muitas vezes variar, dependendo do alérgeno em questão, da gravidade da RHI, e das características individuais do paciente25-27.
O primeiro relato de dessensibilização para idursulfase foi de Serrano C.D., em 2011. Nesse caso, o paciente iniciou com urticária após a 6ª infusão com a medicação. As provas cutâneas realizadas no paciente foram negativas, sendo considerada uma reação não IgE mediada e, por conta desse motivo, utilizado um protocolo alternativo de 8 horas de duração com sucesso na dessensibilização28.
No relato de Bustamante L.L. e cols., após 3 anos de início de tratamento com a medicação, o paciente apresentou um quadro de anafilaxia. Foram realizadas provas cutâneas para as mesmas concentrações por nós testadas com positividade para a concentração de 1/10 (0,2 mg/mL) demonstrando também se tratar de uma possível reação IgE mediada. Nesse estudo, cinco indivíduos saudáveis controles foram testados com todas as concentrações da idursulfase para descartar reação irritativa, sendo todos negativos. A dessensibilização foi realizada em 12 passos, assim como em nosso relato, e ocorreu sem intercorrências29.
No estudo realizado por Emeksiz Z.S. e cols., o paciente desenvolveu reação anafilática após 12 anos de infusões semanais. Foram realizados testes cutâneos com ausência de positividade, e por isso foi considerado como reação não IgE mediada e optado por utilizar uma dessensibilização de 16 passos para a próxima infusão. O paciente não sofreu mais reações com o procedimento e o mesmo foi mantido para as próximas infusões30.
Gragnaniello e cols. também realizaram a dessensibilização em um paciente em que o teste cutâneo veio negativo, mas nesse caso, os sintomas começaram 18 horas após a primeira infusão, febre e vômitos, e recorreram na oitava infusão onde após 1 hora do início da infusão o paciente desenvolveu rash malar bilateral que os levaram a optar por realizar dessensibilização com um protocolo com três bolsas e de 7 horas. Entretanto, mesmo assim, o paciente apresentou sintomas de febre e broncospasmo 4 horas após início da dessensibilização. Os autores não conseguiram diferenciar se essa reação se devia a um processo infeccioso ou a uma reação à medicação, apesar de coletarem posteriormente um swab para rinovírus que resultou em positivo24.
De toda forma, reações durante o processo de dessensibilização podem ocorrer, e a abordagem nesse momento pode variar consideravelmente dependendo da equipe que acompanha o caso, sem haver um consenso definido sobre o tema. Pode-se manter o protocolo e tratar as reações, suspender o protocolo e depois modificá-lo para uma nova abordagem ou tentar retomá-lo com uma concentração ou velocidade menor em um step anterior ao da reação, sendo todas opções válidas25-27.
No caso relatado por Gragnaniello e cols. foi optado por diminuir a dose total para 50% da dose necessária nas próximas infusões, seguindo o mesmo processo de dessensibilização anterior com três bolsas, e progredindo a dose máxima tolerada a cada 2 infusões sucessivas, chegando na dose alvo desejada em 1,5 meses. Progressivamente também foi aumentado a concentração para diminuir o tempo de infusão para 3,5 horas, não havendo mais reações após 3 meses24. Diferentemente, em nosso caso, modificamos o protocolo com o aumento do tempo de infusão nos últimos steps do protocolo de dessensibilização, além de repetirmos pré-medicação antes do step que desencadeou reação no último procedimento.
Por fim, Spataro F. e cols. trouxeram uma nova abordagem para o processo de dessensibilização com idursulfase. No relato, dois pacientes com MPS II iniciaram com sintomas de RHI (urticas) após 1 ano do início da infusão semanal, no primeiro caso, e 3 anos, no segundo caso. Ambos tiveram um teste cutâneo positivo na concentração de 1:100 e, portanto, foram consideradas reações IgE mediadas. Foi optado por realizar a dessensibilização em 12 passos baseado em Casells M.C. e cols., e, assim como em nosso caso, os pacientes também apresentaram reação durante o processo. No primeiro paciente ocorreu reação durante o step 12 da primeira dessensibilizarão em uma velocidade de 150 mL/h, a qual foi tratada com anti-H1 e coricosteroide EV. Com a redução da velocidade de infusão para 40 mL/h por 60 minutos, depois conseguiram retomar a velocidade de 150 mL/h sem outras reações31.
No segundo paciente, um menino de 9 anos, muito similarmente ao nosso caso, foi primeiro tentado aumentar o tempo de infusão e diminuir a dose total da medicação por vários meses, mas o paciente apenas tolerava 4 mg da dose total diária necessária. Quando implementada a dessensibilização, com protocolo de 12 etapas, assim como o do primeiro paciente, com pré-medicação antes e entre as etapas 8 e 9 da dessensibilização, o paciente apresentou reação ao chegar ao step 12, com um quadro de urticária generalizada, sendo medicado novamente com anti-H1 e corticoide EV, e retomada a velocidade final após resolução do quadro, sem mais intercorrências31.
Nos dois pacientes, após as reações durante a dessensibilização, foi implementado um protocolo de imunoterapia similar à realizada com himenópteros, associado à dessensibilização tradicional. O protocolo consistia de injeções subcutâneas de idursulfase (3 ou 4 a cada sessão), intradérmicas, com espaçamento de 20 minutos entre elas, a cada 2 dias, com aumento de concentração e volume na progressão dos steps da dessensibilização, com duração total de 3 semanas. No primeiro paciente não houve mais reações, e por isso os autores conseguiram diminuir o tempo de infusão para 3 horas com uso apenas anti-H1 oral de pré-medicação. Não foi necessário manter as injeções intradérmicas nesse paciente após os 3 meses iniciais. O segundo paciente, por outro lado, seguiu reagindo por mais duas dessensibilizações. Quando o procedimento foi aumentado para 4 bolsas e 20 steps, o paciente não apresentou mais reações. Ao longo das seguintes semanas o protocolo de imunoterapia possibilitou que a infusão fosse reduzida para apenas 6 steps, com uma bolsa, e em aproximadamente 2 horas31.
Estes casos, assim como o nosso, demonstram que as possibilidades são diversas para a dessensibilização, e que nem sempre realizá-la é uma garantia de ausência de reação. O nosso paciente não está mais apresentando reações com nosso protocolo modificado, mas ainda o mantém semanalmente. Como próximo passo, temos a perspectiva de simplificação e de redução do tempo de nosso protocolo de dessensibilização.
Referências
1. Suarez-Guerrero JL, Gómez Higuera PJI, Arias Flórez JS, Contreras-García GA. Mucopolysaccharidosis: clinical features, diagnosis and management. Rev Chil Pediatr [Internet]. 2016;87(4):295-304.
2. Nagpal R, Goyal RB, Priyadarshini K, Kashyap S, Sharma M, Sinha R, et al. Mucopolysaccharidosis: A broad review. Indian J Ophthalmol [Internet]. 2022 Jul;70(7):2249-61.
3. Martin R, Beck M, Eng C, Giugliani R, Harmatz P, Muñoz V, et al. Recognition and diagnosis of mucopolysaccharidosis II (Hunter syndrome). Pediatrics [Internet]. 2008 Feb;121(2):e377-86.
4. Tuschl K, Gal A, Paschke E, Kircher S, Bodamer OA. Mucopolysaccharidosis type II in females: Case report and review of literature. Pediatr Neurol [Internet]. 2005 Apr;32(4):270-2.
5. Khan SA, Peracha H, Ballhausen D, Wiesbauer A, Rohrbach M, Gautschi M, et al. Epidemiology of mucopolysaccharidoses. Mol Genet Metab [Internet]. 2017 Jul;121(3):227-40.
6. Hunter C. A Rare Disease in Two Brothers. Proc R Soc Med [Internet]. 1917;10(Sect Study Dis Child):104-16.
7. Pereira EC, Sacomani DG, Motta AAP da. Manifestações clínicas na Mucopolissacaridose do tipo II grave. Rev Neurociências. 2001;19(4):675-80.
8. Muenzer J. Overview of the mucopolysaccharidoses. Rheumatology (Oxford) [Internet]. 2011 Dec;50 Suppl 5:v4-12.
9. Pinto LLC, Schwartz IVD, Puga ACS, Vieira TA, Munoz MVR, Giugliani R, et al. Avaliação prospectiva de 11 pacientes Brasileiros com mucopolissacaridose II. J Pediatr (Rio J). 2006;82(4):273-8.
10. Holt JB, Poe MD, Escolar ML. Natural Progression of Neurological Disease in Mucopolysaccharidosis Type II. Pediatrics [Internet]. 2011 May 1;127(5):e1258-e1265.
11. Bradley LA, Haddow HRM, Palomaki GE. Treatment of mucopolysaccharidosis type II (Hunter syndrome): Results from a systematic evidence review. Genet Med. Elsevier Masson SAS; 2017;19(11):1187-201.
12. Prasad VK, Kurtzberg J. Cord blood and bone marrow transplantation in inherited metabolic diseases: scientific basis, current status and future directions. Br J Haematol [Internet]. 2010 Feb;148(3):356-72.
13. D'avanzo F, Rigon L, Zanetti A, Tomanin R. Mucopolysaccharidosis type II: One hundred years of research, diagnosis, and treatment. Int J Mol Sci. 2020;21(4).
14. Clarke LA. Idursulfase for the treatment of mucopolysaccharidosis II. Expert Opin Pharmacother [Internet]. 2008 Feb;9(2):311-7.
15. Giugliani R, Federhen A, Muñoz Rojas MV, Vieira TA, Artigalás O, Pinto LLC, et al. Terapia de reposição enzimática para as mucopolissacaridoses I, II e VI: recomendações de um grupo de especialistas brasileiros. Rev Assoc Med Bras [Internet]. 2010;56(3):271-7.
16. da Silva EMK, Strufaldi MWL, Andriolo RB, Silva LA. Enzyme replacement therapy with idursulfase for mucopolysaccharidosis type II (Hunter syndrome). Cochrane Database Syst Rev. 2016;2016(2).
17. Burton BK, Whiteman DAH. Incidence and timing of infusion-related reactions in patients with mucopolysaccharidosis type II (Hunter syndrome) on idursulfase therapy in the real-world setting: A perspective from the Hunter Outcome Survey (HOS). Mol Genet Metab [Internet]. 2011 Jun;103(2):113-20.
18. Wraith JE. Enzyme replacement therapy with idursulfase in patients with mucopolysaccharidosis type II. Acta Paediatr Int J Paediatr. 2008;97(SUPPL. 457):76-8.
19. Concolino D, Deodato F, Parini R. Enzyme replacement therapy: Efficacy and limitations. Ital J Pediatr. 2018;44(Suppl 2).
20. Kim J, Park MR, Kim DS, Lee JO, Maeng SH, Cho SY, et al. IgE-mediated anaphylaxis and allergic reactions to idursulfase in patients with Hunter syndrome. Allergy Eur J Allergy Clin Immunol. 2013;68(6):796-802.
21. Muenzer J, Wraith JE, Beck M, Giugliani R, Harmatz P, Eng CM, et al. A phase II/III clinical study of enzyme replacement therapy with idursulfase in mucopolysaccharidosis II (Hunter syndrome). Genet Med [Internet]. 2006 Aug;8(8):465-73.
22. Giugliani R, Harmatz P, Jones SA, Mendelsohn NJ, Vellodi A, Qiu Y, et al. Evaluation of impact of anti-idursulfase antibodies during long-term idursulfase enzyme replacement therapy in mucopolysaccharidosis II patients. Mol Genet Metab reports [Internet]. 2017 Sep;12:2-7.
23. Wraith JE, Scarpa M, Beck M, Bodamer OA, De Meirleir L, Guffon N, et al. Mucopolysaccharidosis type II (Hunter syndrome): A clinical review and recommendations for treatment in the era of enzyme replacement therapy. Eur J Pediatr. 2008;167(3):267-77.
24. Gragnaniello V, Carraro S, Rubert L, Gueraldi D, Cazzorla C, Massa P, et al. A new strategy of desensitization in mucopolysaccharidosis type II disease treated with idursulfase therapy: A case report and review of the literature. Mol Genet Metab Reports [Internet]. Elsevier Inc.; 2022;31(April):100878.
25. Cernadas JR, Brockow K, Romano A, Aberer W, Torres MJ, Bircher A, et al. General considerations on rapid desensitization for drug hypersensitivity - A consensus statement. Allergy Eur J Allergy Clin Immunol. 2010;65(11):1357-66.
26. Giavina-Bianchi P, Aun MV, Galvão VR, Castells M. Rapid Desensitization in Immediate Hypersensitivity Reaction to Drugs. Curr Treat Options Allergy. 2015;2(3):268-85.
27. Castells M. Rapid Desensitization for Hypersensitivity Reactions to Medications. Immunol Allergy Clin North Am. 2009;29(3):585-606.
28. Serrano CD, Gomez JF. Successful desensitization to idursulfase in a patient with type II mucopolysaccharidosis (Hunter syndrome). J Investig Allergol Clin Immunol [Internet]. 2011;21(7):571-2.
29. Bustamante LL, Garavaglia L, Garramone EI, Amartino H, Parisi CAS. Idursulfase desensitization in a child with Hunter syndrome (mucopolysaccharidosis II). Arch Argent Pediatr. 2021;119(1):E41-E44.
30. Sengül Emeksiz Z, Büyük Yaytokgil S, Külhas Çelik I, Kasapkara Ç, Dibek Misirlioglu E. Successful Idursulfase Desensitization Experience in a Pediatric Patient. Asthma Allergy Immunol. 2022;20(1):68-70.
31. Spataro F, Viggiani F, Macchia DG, Rollo V, Tummolo A, Suppressa P, et al. Novel approach to idursulfase and laronidase desensitization in type 2 and type 1 S mucopolysaccharidosis (MPS). Orphanet J Rare Dis. 2022;17(1):1-11.