Número Atual: Abril-Junho 2024 - Volume 8 - Número 2
- Imprimir
- Indicar
- Estatísticas
- (0)
Comentários - Como Citar
- Download da Citação
- Artigos Relacionados
-
Outros dos
Autores
Artigo Original
Imunoterapia sublingual no tratamento da rinite alérgica local na infância: relato de caso
Sublingual immunotherapy in the management of local allergic rhinitis in childhood: a case report
Fausto Yoshio Matsumoto; Raquel L.T. Alves; Dirceu Solé; Gustavo Falbo Wandalsen
Universidade Federal de São Paulo, Disciplina de Alergia, Imunologia Clínica e Reumatologia, Departamento de Pediatria - São Paulo, SP, Brasil
Endereço para correspondência:
Fausto Yoshio Matsumoto
E-mail: faustoym@gmail.com
Submetido em: 19/06/2024
Aceito em: 01/07/2024.
Não foram declarados conflitos de interesse associados à publicação deste artigo.
RESUMO
A rinite alérgica local (RAL) é um fenótipo de rinite definido recentemente e seu diagnóstico configura um grande desafio tanto para médicos, como para os seus pacientes. A RAL não apresenta evidências de sensibilização sistêmica e, por essa razão, é frequentemente classificada de forma inadequada como uma rinite não alérgica. Este fenótipo de rinite apresenta resposta inflamatória alérgica T2 nasal e síntese local de IgE específica, sendo que o teste de provocação nasal específico é considerado o método padrão ouro para realizar o seu diagnóstico. A RAL possui características clínicas semelhantes aos outros fenótipos de rinite, e pela dificuldade diagnóstica é subdiagnosticada em todas as faixas etárias. O diagnóstico fenotípico correto da rinite tem potenciais benefícios para os pacientes, não apenas por possibilitar a implementação de cuidados para a redução da exposição ambiental aos alérgenos identificados, mas principalmente por permitir a realização de imunoterapia alérgeno específica.
Descritores: Rinite alérgica, alergia a ácaros, criança, imunoterapia sublingual.
Introdução
A rinite alérgica local (RAL) é um fenótipo de rinite definido recentemente e seu diagnóstico configura um grande desafio tanto para médicos, como para os seus pacientes. A RAL não apresenta evidências de sensibilização sistêmica e, por essa razão, é frequentemente classificada de forma inadequada como uma rinite não alérgica. Este fenótipo de rinite apresenta resposta inflamatória alérgica T2 nasal e síntese local de IgE específica1, sendo que o teste de provocação nasal específico (TPNe) é considerado o método padrão ouro para realizar o seu diagnóstico2,3. A RAL possui características clínicas semelhantes aos outros fenótipos de rinite1, e pela dificuldade diagnóstica é subdiagnosticada em todas as faixas etárias. Em adultos, estima-se que até 50% dos pacientes com rinite sem sensibilização sistêmica possam ter o diagnóstico de RAL4. Em crianças, uma revisão sistemática recente5 demonstrou grande variabilidade na prevalência da RAL, demonstrando maior prevalência em países ocidentais (22,3% a 83,3%) quando comparados a países orientais (3,7% a 16,6%). No Brasil, a incidência da RAL em crianças e adolescentes só foi estimada em um serviço terciário de Alergia e Imunologia, obtendo-se prevalência de 40% de pacientes com RAL entre os pacientes com rinite e sem sensibilização sistêmica6.
O diagnóstico fenotípico correto da rinite tem potenciais benefícios para os pacientes, não apenas por possibilitar a implementação de cuidados para a redução da exposição ambiental aos alérgenos identificados, mas principalmente por permitir a realização de imunoterapia alérgeno específica.
Descrição do caso
Este relato de caso descreve paciente do sexo feminino, com 14 anos de idade, com sintomas de rinite que se iniciaram aproximadamente aos 2 anos de idade, que eram esporádicos e associados a mudanças climáticas. Aos 8 anos, os sintomas tornaramse mais frequentes, quando iniciou-se tratamento com corticosteroide tópico nasal (budesonida) e anti-histamínicos orais.
Aos 11 anos, devido à persistência dos sintomas, a paciente foi encaminhada para um serviço terciário de Alergia e Imunologia. Durante investigação etiológica apresentou ausência de resposta positiva aos testes de sensibilização sistêmicos (teste cutâneo de hipersensibilidade imediata e dosagem de IgE sérica específica) para todos os alérgenos testados: Dermatophagoides pteronyssinus (Dp), Blomia tropicalis (Bt), Blattella germanica (Bg), Periplaneta americana (Pa), epitélio de cão, epitélio de gato e mix de fungos. Também realizou avaliação endoscópica da via aérea superior (nasofibroscopia), tendo sido descartadas outras doenças locais que pudessem justificar ou colaborar com a falta de resposta terapêutica.
Durante os primeiros meses de acompanhamento, apesar da introdução da associação de corticosteroide e anti-histamínico nasal (fluticasona + azelastina nasal) e antagonistas de receptores de leucotrienos, a paciente persistia com sintomas e com a necessidade de uso frequente de anti-histamínicos orais, além de escore de sintomas nasais (ESN; escala 0 a 12) de 6, indicando rinite grave e não controlada.
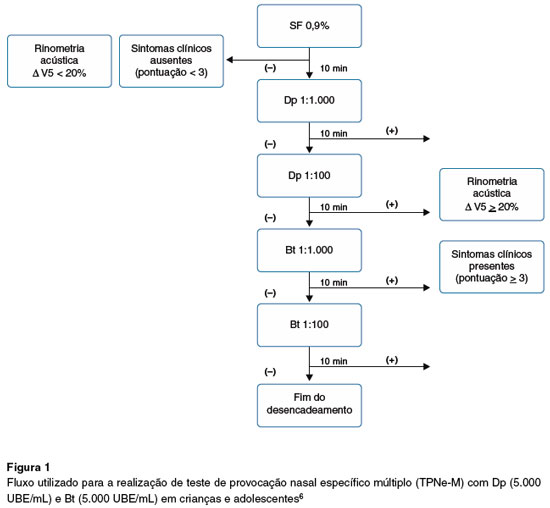
Assim, prosseguiu-se com a investigação etiológica realizando-se TPNe múltiplo (TPNe-M) com Dp e Bt (FDA ALLERGENIC® - Brasil, 5.000 UBE/ml), de acordo com protocolo previamente validado para crianças e adolescentes6. Este consiste na instilação de concentrações crescentes de alérgenos (spray nasal bilateral) de maneira sequencial, com intervalos de 15 minutos, na mesma visita. Os resultados foram monitorados subjetivamente por questionário de sintomas e, objetivamente, pela rinometria acústica (RnA) (Figura 1).
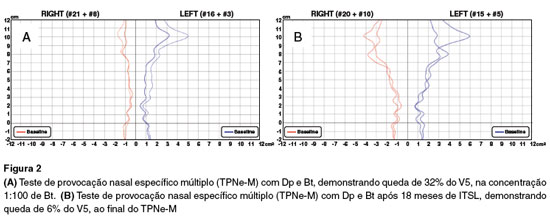
A paciente apresentou TPN negativo para Dp e positivo para Bt na concentração de 1:100, documentado pela queda de 32% do volume nos primeiros 5 cm da cavidade nasal (V5) mensurado pela RnA (Figura 2A).
Após a confirmação de RAL, foi iniciada imunoterapia sublingual (ITSL) para Bt (IPI ASAC Pharma® - Brasil). A paciente apresentou redução parcial dos sintomas nasais após o quarto mês de tratamento (ESN = 4) e progrediu para controle adequado a partir do nono mês de ITSL (ESN = 3), possibilitando redução gradual dos medicamentos empregados, incluindo o corticosteroide tópico nasal, permanecendo apenas com uso de anti-histamínicos orais sob demanda.
Após 18 meses de ITSL, paciente permanecia na fase de manutenção da ITSL e apresentava sintomas nasais controlados (ESN = 3) apenas com uso eventual de anti-histamínico oral. Nesta ocasião, foi realizado novo TPNe-M com Dp e Bt, que apresentou resultado negativo para ambos os alérgenos (Figura 2B).
Discussão
O caso descrito evidencia não apenas as dificuldades no diagnóstico de RAL, mas também o potencial benefício em realizá-lo. Exemplifica também que a gravidade da RAL não difere dos outros fenótipos de rinite, como já demonstrado por outros autores7.
O diagnóstico correto deste fenótipo demonstra sua importância, pois sem realizá-lo adequadamente, não há possibilidade de instituição da imunoterapia alérgeno específica, limitando o arsenal terapêutico disponível para tratamento individualizado.
O tratamento da RAL com a ITSL com Bt, reforça a importância desta ferramenta no tratamento de crianças e adolescentes com RAL. Em adultos, a imunoterapia com alérgeno subcutânea (ITSC) tem demonstrado bons resultados no tratamento da RAL8,9. Duas metanálises recentes8,9 avaliaram a eficácia e a segurança da ITSC no tratamento da RAL em adultos. Ambas sugerem que a imunoterapia induza: efeito significativo na melhoria dos sintomas, redução do consumo de medicamentos, aumento de IgG4 sérica específica após 2 anos de tratamento, e aumento da tolerância ao alérgeno após ITSC9. Além disso, outra metanálise8 demonstrou tendência de maior benefício nos pacientes com RAL sazonal em comparação com aqueles com sintomas perenes. Nenhum dos estudos analisados pelas metanálises avaliou a resposta de longo prazo, após o término do tratamento. Destaca-se que, nestas metanálises, não foi possível avaliar a eficácia da ITSL na RAL, devido à falta de dados disponíveis.
Na faixa exclusivamente pediátrica, há poucos estudos e informações disponíveis sobre a RAL e não há na literatura algum relato de resposta terapêutica à ITSC ou à ITSL.
Neste caso, a ITSL com Bt foi capaz não apenas de induzir uma boa resposta clínica, demonstrado pela diminuição no ESN e diminuição do consumo de medicamentos, mas também foi possível evidenciar o aumento na tolerância do paciente ao alérgeno ao longo do tratamento, fato demonstrado pela negativação do TPNe-M após 18 meses do início do tratamento.
Novos trabalhos, tanto em adultos como em crianças, devem ser realizados com objetivo de acompanhar não apenas os benefícios da ITSL e da ITSC, em curto prazo, mas também os benefícios em longo prazo, após término dos 3 anos da imunoterapia, avaliando a possibilidade de persistência de resposta e impacto definitivo na melhora da qualidade de vida destes pacientes.
Referências
1. Rondón C, Fernandez J, Canto G, Blanca M. Local allergic rhinitis: Concept, clinical manifestations, and diagnostic approach. J Investig Allergol Clin Immunol. 2010;20(5):364-71.
2. Cho SH, Nanda A, Keswani A, Adinoff A, Baroody FM, Bernstein JA, et al. Nasal allergen challenge (NAC): Practical aspects and applications from an EU/US perspective-a Work Group Report of the AAAAI Rhinitis, Rhinosinusitis and Ocular Allergy Committee. J Allergy Clin Immunol. 2023 May 1;151(5):1215-1222.e4.
3. Augé J, Vent J, Agache I, Airaksinen L, Campo Mozo P, Chaker A, et al. EAACI Position paper on the standardization of nasal allergen challenges. Allergy: European Journal of Allergy and Clinical Immunology. 2018;73(8):1597-608.
4. Rondón C, Campo P, Zambonino MA, Blanca-Lopez N, Torres MJ, Melendez L, et al. Follow-up study in local allergic rhinitis shows a consistent entity not evolving to systemic allergic rhinitis. Journal of Allergy and Clinical Immunology. 2014;133(4):1026-31.
5. Matsumoto FY, Tranquillini Gonçalves TR, Solé D, Wandalsen GF. Local allergic rhinitis in children: A systematic review. Allergol Immunopathol (Madr). 2022 Mar 1;50(2):40-7.
6. Matsumoto FY, Tranquillini Gonçalves TR, Solé D, Wandalsen GF. Local allergic rhinitis in children: identification and characterization in a specialty outpatient clinic. Eur Ann Allergy Clin Immunol. 2024 Jan 23. doi: 10.23822/EurAnnACI.1764-1489.327.
7. Rondon C, Campo P, Eguiluz-Gracia I, Plaza C, Bogas G, Galindo P, et al. Local allergic rhinitis is an independent rhinitis phenotype: The results of a 10-year follow-up study. Allergy: European Journal of Allergy and Clinical Immunology. 2018;73(2):470-8.
8. Hoang MP, Samuthpongtorn J, Chitsuthipakorn W, Seresirikachorn K, Snidvongs K. Allergen-specific immunotherapy for local allergic rhinitis: a systematic review and meta-analysis. Rhinology. 2022 Feb 1;60(1):11-9.
9. Zhu W, Gao P, Zhang Q, Chen J. Efficacy and Safety of Subcutaneous Immunotherapy for Local Allergic Rhinitis: A Meta-Analysis of Randomized Controlled Trials. Am J Rhinol Allergy. 2022 Mar 19;36(2):245-52.