Número Atual: Abril-Junho 2019 - Volume 3 - Número 2
CARTA AO EDITOR
Imunoglobulina humana (Ig) e anticorpos neutralizantes
Carolina Sanchez Aranda1; Ana Maria Martins2; Dirceu Solé3
DOI: 10.5935/2526-5393.20190034
1. Universidade Federal de São Paulo, Departamento de Pediatria - São Paulo, SP, Brasil
2. Universidade Federal de São Paulo, Departamento de Pediatria - São Paulo, SP, Brasil
3. Universidade Federal de São Paulo, Departamento de Pediatria - São Paulo, SP, Brasil
Endereço para correspondência:
Dirceu Solé
E-mail: dirceu.sole@unifesp.br
Não foram declarados conflitos de interesse associados à publicação desta carta.
Prezado Editor,
A imunoglobulina humana, atualmente, está indicada em duas grandes situações: em pacientes com níveis séricos de imunoglobulina G (IgG) diminutos que necessitem de doses de reposição (400 até 600 mg/Kg/dose), abrangendo aqueles com imunodeficiências primárias associadas à deficiência humoral, mieloma múltiplo, leucemia linfoide crônica e uso de anticorpos monoclonais anti-CD20 com depleção de linfócitos B e queda dos níveis de IgG, e em pacientes com doenças que cursam com inflamação exagerada, às vezes com formação de autoanticorpos, como no lúpus eritematoso sistêmico, na esclerose múltipla, nas encefalites autoimunes, entre outras1. Nessa segunda indicação, as doses recomendadas são altas, chamadas imunomodulatórias (1 até 2 g/Kg/dose). Os mecanismos envolvidos no uso de doses aumentadas de imunoglobulina envolvem o receptor DC-SIGN (Dendritic Cell-Specific Intercellular adhesion molecule-3-Grabbing Non-integrin; CD209), expresso na superfície de células dendríticas e de macrófagos que é capaz de reconhecer exclusivamente a porção Fc ligada ao ácido siálico das imunoglobulinas. Essa ligação aumenta a produção de interleucina (IL) 33, essencial na ativação de basófilos que produzem IL-4, a qual induz o aumento da expressão de receptores inibitórios dos macrófagos. Com isso, a administração de doses imunomodulatórias de imunoglobulinas aumenta a resposta do tipo linfócito helper 2 (Th2) após a interação da porção sFc com DC-SIGN, o que promove o controle de respostas inflamatórias2. Além disso, altas doses de Ig aumentam as prostaglandinas E2 e os linfócitos T regulatórios FOXP3+ e desativam a via dos linfócitos Th17, diminuindo a inflamação e promovendo um estado de latência temporária na produção de anticorpos3.
A partir desses conhecimentos, o alergista/imunologista pode ser requisitado para auxílio nas diversas especialidades. Um paciente com Doença de Pompe, erro inato do metabolismo caracterizado pelo acúmulo de macromoléculas, pode apresentar dois tipos de status imunológico, o CRIM (Cross reactive immunological material ) positivo com atividade residual da enzima alglucosidase alfa (GAA), e CRIM negativo, com completa ausência de GAA endógena4. Nos casos de pacientes com CRIM negativo, ao receber tratamento com a enzima recombinante (alglucosidase alfa - rhGAA), há formação de anticorpos neutralizantes (IgG anti-enzima recombinante), prejudicando de maneira drástica a eficácia do tratamento. À semelhança do ocorrido na Doença de Pompe, outros tratamentos que utilizem enzimas recombinantes ou anticorpos monoclonais podem ser prejudicados pela formação de anticorpos neutralizantes. Ademais a formação de IgG antidroga5, a produção de qualquer classe de anticorpos antidrogas (ADA - anti-drug antibody ), inclusive a formação de IgE antidroga responsáveis pelas reações de hipersensibilidade imediatas, pode prejudicar diferentes tratamentos, influenciando na segurança e/ou eficácia do mesmo. Com isso, estratégias de prevenção e tratamento da formação dos anticorpos antidrogas estão sendo formuladas com o auxílio da Imunologia, como a dessensibilização6 e outras formas de imunomodulação.
Assistimos a paciente masculino com cardiomegalia em ultrassonografia intraútero que apresentou hipoglicemia nas primeiras 24 horas de vida secundária a sucção débil. Foi realizado o diagnóstico de Doença de Pompe aos 3 meses de vida, com atividade de alfa-glicosidase negativa em leucócitos e sequenciamento completo do gene GAA com variante patogênica em homozigose, descrita como c2501_2502delCA, inferindo status CRIM negativo. Nesses casos, um protocolo validado de imunotolerância está indicado4.
Aos 4 meses, o paciente foi admitido em nosso serviço para iniciar terapia de reposição com alglucosidase alfa (rhGAA) associada a indução de imunotolerância com rituximabe, metotrexate e imunoglobulina endovenosa na dose de reposição4. Entretanto, antes de iniciar o protocolo, o paciente apresentou parada cardiorrespiratória secundária a broncoaspiração, com necessidade de intubação orotraqueal e encaminhado à UTI. Na ocasião, ecocardiograma com doppler (ECO) revelava hipertrofia de ventrículo esquerdo de 343,9 g/m2. Devido à instabilidade clínica, o protocolo padrão não seria tolerado pelo paciente pelo alto risco de morte. Dessa maneira, optamos iniciar reposição de rhGAA com a realização de altas doses de imunoglobulina humana (1 g/kg quinzenalmente - 2 g/kg/mês) no dia anterior à reposição enzimática na tentativa de diminuição da formação dos anticorpos neutralizantes.
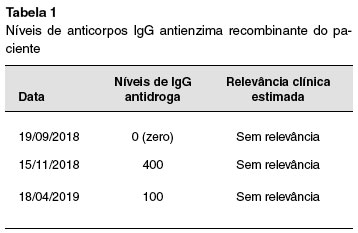
As dosagens de anti-rhGAA (Sanofi-Genzyme - enzyme-linked immunosorbent assay - ELISA) foram realizadas após 2, 4 e 9 meses do início da terapia de reposição enzimática (resultados descritos na Tabela 1), todas com resultados não relevantes clinicamente. Na literatura, níveis superiores a 12.8004 são indicativos de neutralização do medicamento. Atualmente o paciente apresenta-se clinicamente estável, fora de ventilação mecânica e com o último ECO revelando melhora significativa da hipertrofia de ventrículo esquerdo (283,2 g/m2).
Embora a Doença de Pompe seja um erro inato do metabolismo raro, o diagnóstico precoce com introdução oportuna de reposição enzimática tem potencial de reduzir significativamente a morbimortalidade dos pacientes. Apesar de não estar descrito como primeira opção terapêutica, o uso isolado de altas doses de imunoglobulina humana para imunomodulação mostrou-se eficaz e com baixos riscos para nosso paciente. Até onde sabemos, esse paciente foi o primeiro bebê na literatura a ser tratado de maneira inicial com imunoglobulina para diminuir a formação de anticorpos neutralizantes, com ótimos resultados clínicos e laboratoriais.
Em conclusão, o uso isolado de imunoglobulina humana em dose imunomodulatória deve ser avaliado como opção segura e eficaz nos pacientes com instabilidade clínica e que necessitam de indução de imunotolerância para uso de drogas com alto risco de gerar anticorpos neutralizantes. As diferentes técnicas de imunomodulação para manejo da formação dos anticorpos antidrogas são relevantes e devem ser vistas como um tópico essencial na prática clínica da nossa especialidade.
Agradecimentos: a todos os Médicos Residentes de Alergia e Imunologia, de Pediatria e de Genética Médica da Universidade Federal de São Paulo dos anos de 2018 e 2019, pelo empenho e carinho nas visitas diárias ao paciente relatado.
REFERÊNCIAS
1. Pecoraro A, Crescenzi L, Granata F, Genovese A, Spadaro G. Immunoglobulin replacement therapy in primary and secondary antibody deficiency: The correct clinical approach. Int Immunopharmacol. 2017;52:136-42.
2. Anthony RM, Kobayashi T, Wermeling F, Ravetch JV. Intravenous gammaglobulin suppresses inflammation through a novel T(H)2 pathway. Nature. 2011,19;475(7354):110-3.
3. Ballow M. Mechanisms of immune regulation by IVIG. Curr Opin Allergy Clin Immunol. 2014;14(6):509-15.
4. Kazi ZB, Desai AK, Berrier KL, Troxler RB, Wang RY, Abdul-Rahman OA, et al. Sustained immune tolerance induction in enzyme replacement therapy-treated CRIM-negative patients with infantile Pompe disease. JCI Insight. 2017,17;2(16).
5. Krishna M, Nadler SG. Immunogenicity to Biotherapeutics - The Role of Anti-drug Immune Complexes. Front Immunol. 2016,2;7:21.
6. Castells MC. A New Era for Drug Desensitizations. J Allergy Clin Immunol Pract. 2015;3(4):639-40.



