Número Atual: Outubro-Dezembro 2017 - Volume 1 - Número 4
- Imprimir
- Indicar
- Estatísticas
- (0)
Comentários - Como Citar
- Download da Citação
- Artigos Relacionados
-
Outros dos
Autores
Artigo Original
Incidência aumentada de haplótipo de HLA de classe II na anafilaxia grave secundária à carboplatina
Increased incidence of a class II HLA haplotype in severe anaphylaxis secondary to carboplatin
Violeta Régnier Galvao1; Elizabeth Phillips2,3; Mariana Castells4; Pedro Giavina-Bianchi1
DOI: 10.5935/2526-5393.20170055
1. Faculdade de Medicina da Universidade de Sao Paulo, Imunologia Clínica e Alergia - Sao Paulo,SP, Brasil
2. Vanderbilt University, Division of Infectious Diseases - Nashville - Tennessee, Estados Unidos
3. Murdoch University, Institute for Immunology and Infectious Diseases - Perth, WA, Austrália
4. Brigham and Women`s Hospital, Rheumatology, Immunology and Allergy - Boston, MA, Estados Unidos
Endereço para correspondência:
Violeta Régnier Galvao
E-mail: violeta_galvao@yahoo.com.br
Submetido em: 03/11/2017
Aceito em: 20/11/2017.
Nao foram declarados conflitos de interesse associados à publicaçao deste artigo.
RESUMO
OBJETIVO: O papel de biomarcadores nas reaçoes de hipersensibilidade a platinas tem sido estudado, e é conhecido que a presença da mutaçao do gene BRCA1/2 é fator de risco para reaçoes de hipersensibilidade à carboplatina. A genotipagem de HLA de classes I e II auxilia na identificaçao de pacientes de risco para reaçoes IgE-mediadas e mediadas por linfócitos T associadas a beta-lactâmicos e abacavir, respectivamente. Nao sao conhecidos alelos ou haplótipos de HLA mais prevalentes em pacientes alérgicos à carboplatina. O objetivo principal do estudo foi avaliar se alelos específicos de HLA de classe II sao mais prevalentes em pacientes alérgicos à carboplatina submetidos à dessensibilizaçao (DS).
MÉTODO: Genotipagem de HLA de classe II realizada em 11 pacientes portadoras de neoplasias malignas tubo-ovarianas, alérgicas à carboplatina, e submetidas à DS, e em 12 pacientes tolerantes à carboplatina, por no mínimo oito ciclos. Analisou-se também a prevalência da mutaçao BRCA1/2 nos dois grupos estudados.
RESULTADOS: O alelo HLA-DRB1*15:01 foi mais prevalente entre as pacientes alérgicas (5/11; 45%) do que nos controles (1/12; 8,3%) (p = 0,06). O haplótipo de classe II DQA1*01:02-DQB1*06:02-DRB1*15:01 foi mais expresso no grupo de pacientes alérgicas. A mutaçao do BRCA1/2 mostrou-se mais prevalente no grupo alérgico.
CONCLUSOES: A identificaçao de pacientes de risco para reaçoes alérgicas à carboplatina é de extrema importância com o uso crescente da medicaçao. A genotipagem de HLA e a pesquisa da mutaçao BRCA1/2 mostramse ferramentas promissoras que podem aumentar a segurança durante infusao regular de carboplatina e DS.
Descritores: Antígenos HLA, anafilaxia, neoplasias ovarianas, carboplatina, dessensibilizaçao imunológica.
INTRODUÇAO
A genotipagem de HLA de classes I e II tem identificado pacientes de risco para reaçoes medicamentosas graves IgE/mastócito-mediadas e mediadas por células1-4.
O abacavir e a carbamazepina induzem reaçoes mediadas por linfócitos T na presença de alelos específicos do complexo principal de histocompatibilidade (MHC). A ocorrência do alelo de MHC classe I HLA-B*57:01, presente em aproximadamente 6% da populaçao, foi correlacionada a aumento de risco para reaçoes de hipersensibilidade (RH) tardias ao abacavir. Este achado motivou o uso do rastreamento para o HLA-B*5701 em candidatos ao uso de abacavir1, reduzindo drasticamente a incidência de RH a este medicamento. O alelo de classe I HLA-B*15:02 foi associado à síndrome de Stevens Johnson (SSJ) e a necrólise epidérmica tóxica (NET) induzidas por carbamazepina em populaçoes de etnia chinesa Han, tai e malaia2. Adicionalmente, o alelo HLA-A*31:01 foi relacionado à síndrome de hipersensibilidade ligada à carbamazepina e a exantema maculopapular em populaçoes caucasianas, japonesas, coreanas e chinesas5. Variantes de HLA-DRA classe II sao associadas a reaçoes de hipersensibilidade imediata a beta-lactâmicos3, e o alelo HLA-DRB1*07:01 relaciona-se a reaçoes IgE-mediadas à asparaginase4.
É conhecido que pacientes expostos a seis ou mais ciclos de carboplatina apresentam risco de desenvolver RH imediata à droga, com incidência estimada em 6 a 27%6-8. A geraçao de IgE sérica para a carboplatina é proposta como mecanismo causal principal, o que é demonstrado pelos testes de IgE sérica específica9 e cutâneos de leitura imediata10 na avaliaçao de pacientes alérgicos a este medicamento. Os resultados do teste de ativaçao de basófilos (BAT)11-13 e o aumento nos níveis de triptase sérica indicam que há envolvimento de basófilos e mastócitos, respectivamente, nas reaçoes anafiláticas à carboplatina.
Fatores de risco para reaçoes alérgicas à carboplatina têm sido foco de pesquisas recentes. Nosso grupo demonstrou que a expressao dos marcadores de ativaçao basofílica CD63 e CD203c encontra-se aumentada após estimulaçao com carboplatina e oxaliplatina em pacientes alérgicos a estes medicamentos, e que o BAT pode identificar pacientes de risco para reaçoes durante a dessensibilizaçao a estes quimioterápicos12. Em estudo prospectivo, Iwamoto et al. demonstraram que pacientes que se tornaram alérgicos à carboplatina durante o estudo apresentavam expressao aumentada de CD203c no dia anterior ao da reaçao11.
Estudo de 2013 evidenciou que a mutaçao dos genes BRCA 1 e 2 tem prevalência aumentada nos pacientes que desenvolvem reaçoes imediatas à carboplatina14. Moon et al. observaram em estudo retrospectivo que a maioria dos pacientes que apresentaram RH à carboplatina possuíam mutaçoes deletérias para os genes BRCA 1 e 2 (93%, 27/29), em comparaçao a 50% (29/58) em pacientes tolerantes à droga (p < 0,0001)14.
Nosso grupo observou prevalência de 34% da mutaçao BRCA 1/2 em pacientes portadoras de neoplasias tubo-ovarianas alérgicas à carboplatina, tratadas no hospital Dana Farber Cancer Institute (DFCI) e submetidas à dessensibilizaçao no hospital Brigham and Women's Hospital (BWH), em Boston, EUA15. É conhecido que a prevalência desta mutaçao em pacientes portadoras de neoplasias tubo-ovarianas varia de 13 a 17%16 e, especificamente em pacientes portadoras de câncer de mama tratadas no DFCI, é 6,1%17. Também relatamos que pacientes com a mutaçao apresentavam risco maior de RH durante a dessensibilizaçao à carboplatina (p < 0,01).
Embora a mutaçao do BRCA 1/2 e o BAT sejam métodos promissores para a identificaçao de pacientes de risco, eles apresentam baixa sensibilidade para identificar número maior de pacientes potencialmente alérgicos. O objetivo principal do nosso estudo foi avaliar se alelos específicos de classe II do HLA sao mais prevalentes em pacientes que apresentam reaçoes de hipersensibilidade imediatas à carboplatina. Como objetivo secundário, buscamos caracterizar a prevalência da mutaçao do gene BRCA 1/2 na populaçao estudada.
MÉTODOS
O estudo foi aprovado pelo comitê de ética em pesquisa Partners Institutional Review Board (protocolo 13-288), dos hospitais BWH e DFCI, afiliados à Harvard Medical School, em Boston, Massachusetts, Estados Unidos da América. As pacientes alérgicas e controles foram selecionadas no período de outubro de 2014 a novembro de 2015, de acordo com os critérios descritos a seguir.
Seleçao das pacientes alérgicas
Pacientes caucasianas portadoras de neoplasias malignas tubo-ovarianas, maiores de 18 anos e referenciadas ao Drug Hypersensitivity and Desensitization Center do BWH para realizaçao de dessensibilizaçao à medicaçao foram selecionadas. Essas pacientes apresentaram originalmente reaçoes de hipersensibilidade imediata à carboplatina graus 2 ou 3, de acordo com a classificaçao de Brown18.
Seleçao das pacientes do grupo controle
Foram selecionadas 12 pacientes caucasianas, com idade superior a 18 anos, portadoras de neoplasias malignas tubo-ovarianas. As pacientes foram tolerantes a oito ou mais ciclos de carboplatina e submetidas à infusao da medicaçao no DFCI.
Extraçao de DNA
O DNA foi extraído de amostra de sangue coletada durante a visita das pacientes alérgicas para dessensibilizaçao ou durante infusao regular das pacientes do grupo controle. O kit QiAmp DNA Mini Kit (Qiagen, Hilden, Alemanha) foi utilizado para extrair DNA de amostras de sangue de 200 µl. Todas as amostras de DNA foram armazenadas a -20° C até que a genotipagem de HLA fosse realizada.
Genotipagem de HLA
A genotipagem HLA A, B, C, DR, DQ e DP foi realizada utilizando-se sequenciamento de segunda geraçao em plataforma MiSeq (Illuminar).
Análise da mutaçao BRCA 1/2
A avaliaçao da presença de mutaçao nos genes BRCA 1 e 2 foi realizada utilizando-se painel OvaNext (AmbryGeneticsr), por sequenciamento de nova geraçao ou pelo teste BRACAnalysisr (Myriadr).
Análise estatística
A frequência dos alelos de HLA entre pacientes alérgicas e controles foi comparada utilizando-se teste exato de Fisher. O programa Cobygram foi utilizado para a visualizaçao dos blocos de haplótipos.
RESULTADOS
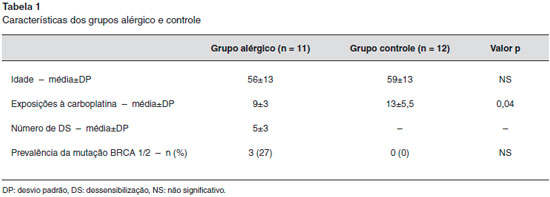
As características gerais das pacientes alérgicas e do grupo controle podem ser observadas na Tabela 1. As pacientes apresentaram média de idade semelhante: 56±13 anos no grupo alérgico e 59±13 anos no grupo controle. As pacientes alérgicas apresentaram número menor de exposiçoes prévias à carboplatina (9±3) do que o grupo controle (13±5,5).
No grupo alérgico, 36% (4/11) das pacientes apresentaram reaçoes iniciais grau 2 e 64% (7/11) grau 3 (Figura 1a). Os testes cutâneos de leitura imediata foram positivos em 81% das pacientes alérgicas, a maioria na diluiçao de 1 mg/dL do teste intradérmico para carboplatina (67%) (Figura 1b). Todas as pacientes alérgicas toleraram a dessensibilizaçao e conseguiram completar seus tratamentos.
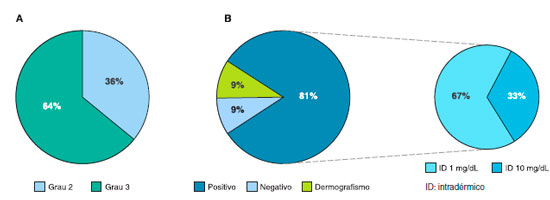
Figura 1 A. Graus das reaçoes de hipersensibilidade iniciais B. Distribuiçao dos resultados dos testes cutâneos nas pacientes alérgicas
A mutaçao dos genes BRCA1/2 foi encontrada em 3/11 pacientes alérgicas versus 0/12 no grupo controle (Tabela 1). O alelo HLA-DRB1*15:01 foi mais prevalente entre as pacientes alérgicas (5/11, 45%) do que entre pacientes do grupo controle (1/12, 8,3%) (Figura 2, p = 0,06). A análise Cobygram identificou que o haplótipo de classe II DQA1*01:02-DQB1*06:02DRB1*15:01 apresentou aumento de representaçao nas pacientes alérgicas (Figura 3).
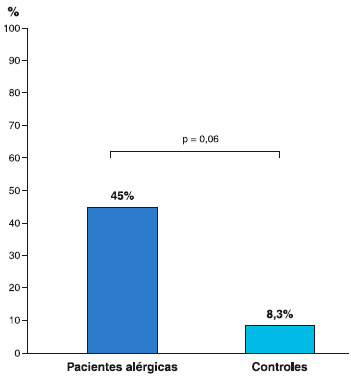
Figura 2 Prevalência do alelo HLA DRB1*15:01 nas pacientes alérgicas e controles
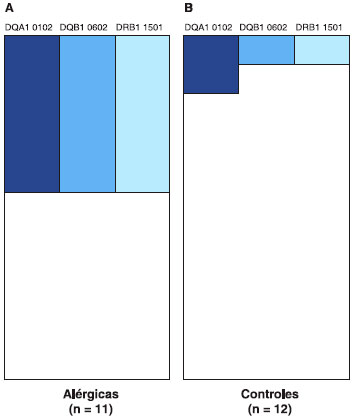
Figura 3 Aumento de representaçao do haplótipo DQA1*01:02-DQB1*06:02-DRB1*15:01 no grupo alérgico
DISCUSSAO
Em nossa coorte de pacientes caucasianas portadoras de neoplasias malignas tubo-ovarianas, foi observado que o alelo de HLA classe II DRB1*15:01 e o haplótipo de classe II DQA1*01:02-DQB1*06:02DRB1*15:01 apresentaram aumento de prevalência em relaçao ao grupo controle. O estudo fornece informaçoes preliminares a respeito da farmacogenética aplicada a reaçoes de hipersensibilidade IgEmediadas à carboplatina.
O exemplo mais notório da influência do HLA na predisposiçao a reaçoes medicamentosas é a relaçao entre HLA-B*5701 e RH tardias ao abacavir19. RH tardias potencialmente letais ao abacavir (SSJ, NET) podem ser observadas em 5 a 8% de pacientes soropositivos para o HIV tratados com terapia antirretroviral, e sao geralmente observadas nas primeiras 6 semanas de tratamento. O rastreamento do HLAB*5701 minimiza toxicidades potenciais por meio da identificaçao de pacientes de risco, apresenta sensibilidade de 94 a 100% em pacientes com reaçoes imunológicas confirmadas ao abacavir (via teste de contato com a droga), e especificidade de 90 a 100%, independente do diagnóstico da reaçao basear-se na apresentaçao clínica ou em confirmaçao imunológica20. Além de eficaz, o rastreamento também foi comprovado ser custo-efetivo21. O estudo PREDICT-1 contou com a participaçao de 1956 pacientes de 19 países e observou incidência de RH confirmada ao abacavir em 2,7% no grupo controle versus 0% no grupo rastreado (p < 0,001)1. Em outro estudo prospectivo, com 137 pacientes soropositivos de origem étnica mista, foi evidenciado 0% de incidência de RH ao abacavir no grupo submetido a rastreamento.
Dados sobre a relaçao entre HLA e a ocorrência de reaçoes IgE-mediadas sao escassos22,23. Um estudo chinês propôs associaçao de alelos na regiao HLA-DRB a RH imediatas à penicilina por meio da modulaçao da síntese de IgE séricas específicas para a penicilina23.
Embora o número de pacientes avaliadas tenha sido pequeno, houve tendência de expressao maior da mutaçao dos genes BRCA 1/2 no grupo alérgico. Este resultado é esperado, tendo em vista que a mutaçao é fator de risco para RH imediatas à carboplatina. Ainda nao é conhecido o mecanismo fisiopatológico que vincule a mutaçao à reaçao alérgica, porém especula-se que as mutaçoes do BRCA 1/2 influenciem a expressao de genes Th2 e aumentem níveis de IgE sérica à carboplatina e/ou aumentem transduçoes de sinal durante ativaçao mastocitária em resposta à carboplatina24.
A importância de se pesquisar a mutaçao do BRCA 1/2 em pacientes que se submetem à dessensibilizaçao à carboplatina foi evidenciada recentemente pelo nosso grupo15. Em casuística composta por 138 pacientes portadoras de neoplasias malignas tubo-ovarianas, foi observado que RH durante DS ocorreram em 51% dos portadores da mutaçao BRCA 1/2 comparado a 27% nos pacientes sem a mutaçao (p < 0,01). Embora a gravidade das reaçoes tenha sido semelhante entre os grupos, os achados reforçam o papel da pesquisa da mutaçao como rastreamento pré-infusao.
Nosso estudo tem como limitaçao o tamanho da amostra estudada, o que impossibilita conclusoes definitivas acerca do tema. Caso os achados sejam confirmados em populaçoes maiores, é possível estabelecer os papéis do alelo HLA-DRB1*15:01 e haplótipo DQA1*01:02-DQB1*06:02-DRB1*15:01 como potenciais fatores de risco para reaçoes imediatas à carboplatina. Desta forma, de maneira semelhante ao rastreamento populacional para o alelo B*57:01 em candidatos ao abacavir, poderia ser proposta genotipagem de HLA em candidatos à infusao regular e à dessensibilizaçao à carboplatina para a identificaçao de pacientes de alto risco.
AGRADECIMENTOS
Agradecemos a Alicia Beeghly-Fadiel, pela análise estatística; e a Rebecca Pavlos, Elizabeth Mckinnon, Kristina Williams e Alec Redwood, pelo auxílio na genotipagem de HLA das amostras.
REFERENCIAS
1. Mallal S, Phillips E, Carosi G, Molina J-M, Workman C, Tomazic J, et al. HLA-B*5701 screening for hypersensitivity to abacavir. N Engl J Med. 2008;358(6):568-79.
2. Chen P, Lin J-J, Lu C-S, Ong C-T, Hsieh PF, Yang C-C, et al. Carbamazepine-induced toxic effects and HLA-B*1502 screening in Taiwan. N Engl J Med. 2011;364(12):1126-33.
3. Guéant J-L, Romano A, Cornejo-Garcia J-A, Oussalah A, Chery C, Blanca-López N, et al. HLA-DRA variants predict penicillin allergy in genome-wide fine-mapping genotyping. J Allergy Clin Immunol. 2015;135(1):253-9.
4. Fernandez CA, Smith C, Yang W, Daté M, Bashford D, Larsen E, et al. HLA-DRB1*07:01 is associated with a higher risk of asparaginase allergies. Blood. 2014;124(8):1266-76.
5. McCormack M, Alfirevic A, Bourgeois S, Farrell JJ, Kasperavičiūtė D, Carrington M, et al. HLA-A*3101 and Carbamazepine- Induced Hypersensitivity Reactions in Europeans. N Engl J Med. 2011;364(12):1134-43.
6. Markman M, Kennedy A, Webster K, Elson P, Peterson G, Kulp B, et al. Clinical features of hypersensitivity reactions to carboplatin. J Clin Oncol. 1999;17(4):1141.
7. Makrilia N, Syrigou E, Kaklamanos I, Manolopoulos L, Saif MW. Hypersensitivity reactions associated with platinum antineoplastic agents: a systematic review. Met-Based Drugs. 2010;2010:1-11.
8. Gadducci A, Tana R, Teti G, Zanca G, Fanucchi A, Genazzani AR. Analysis of the pattern of hypersensitivity reactions in patients receiving carboplatin retreatment for recurrent ovarian cancer. Int J Gynecol Cancer Off J Int Gynecol Cancer Soc. 2008;18(4):615-20.
9. Caiado J, Venemalm L, Pereira-Santos MC, Costa L, Barbosa MP, Castells M. Carboplatin-, Oxaliplatin-, and Cisplatinspecific IgE: Cross-reactivity and Value in the Diagnosis of Carboplatin and Oxaliplatin Allergy. J Allergy Clin Immunol Pract. 2013;1(5):494-500.
10. Castells MC, Tennant NM, Sloane DE, Hsu FI, Barrett NA, Hong DI, et al. Hypersensitivity reactions to chemotherapy: outcomes and safety of rapid desensitization in 413 cases. J Allergy Clin Immunol. 2008;122(3):574-80.
11. Iwamoto T, Yuta A, Tabata T, Sugimoto H, Gabazza EC, Hirai H, et al. Evaluation of basophil CD203c as a predictor of carboplatin-related hypersensitivity reaction in patients with gynecologic cancer. Biol Pharm Bull. 2012;35(9):1487-95.
12. Iwamoto T, Hirai H, Yamaguchi N, Kobayashi N, Sugimoto H, Tabata T, et al. Carboplatin-induced severe hypersensitivity reaction: role of IgE-dependent basophil activation and FcεRI. Cancer Sci. 2014;105(11):1472-9.
13. Giavina-Bianchi P, Galvao VR, Picard M, Caiado J, Castells MC. Basophil activation test is a relevant biomarker of the outcome of rapid desensitization in platinum compounds-allergy. J Allergy Clin Immunol Pract. 2017;5(3):728-36.
14. Moon DH, Lee J-M, Noonan AM, Annunziata CM, Minasian L, Houston N, et al. Deleterious BRCA1/2 mutation is an independent risk factor for carboplatin hypersensitivity reactions. Br J Cancer. 2013;109(4):1072-8.
15. Galvao VR, Phillips E, Giavina-Bianchi P, Castells MC. Carboplatinallergic patients undergoing desensitization: prevalence and impact of the BRCA 1/2 mutation. J Allergy Clin Immunol Pract. 2017;5(3):816-8.
16. Pal T, Permuth-Wey J, Betts JA, Krischer JP, Fiorica J, Arango H, et al. BRCA1 and BRCA2 mutations account for a large proportion of ovarian carcinoma cases. Cancer. 2005;104(12):2807-16.
17. Tung N, Lin NU, Kidd J, Allen BA, Singh N, Wenstrup RJ, et al. Frequency of germline mutations in 25 cancer susceptibility genes in a sequential series of patients with breast cancer. J Clin Oncol. 2016;34(13):1460-8.
18. Brown SG. Clinical features and severity grading of anaphylaxis. J Allergy Clin Immunol. 2004;114(2):371-6.
19. Mallal S, Nolan D, Witt C, Masel G, Martin AM, Moore C, et al. Association between presence of HLA-B*5701, HLA-DR7, and HLA-DQ3 and hypersensitivity to HIV-1 reverse-transcriptase inhibitor abacavir. Lancet Lond Engl. 2002;359(9308):727-32.
20. Ma JD, Lee KC, Kuo GM. HLA-B*5701 testing to predict abacavir hypersensitivity. PLoS Curr [Internet]. 2010 Dec 7 [cited 2016 Jul 1];2. Disponível em: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3000684/
21. Schackman BR, Scott CA, Walensky RP, Losina E, Freedberg KA, Sax PE. The cost-effectiveness of HLA-B*5701 genetic screening to guide initial antiretroviral therapy for HIV. AIDS Lond Engl. 2008;22(15):2025-33.
22. Stone SF, Phillips EJ, Wiese MD, Heddle RJ, Brown SGA. Immediatetype hypersensitivity drug reactions. Br J Clin Pharmacol. 2014 Jul;78(1):1-13.
23. Yang J, Qiao H, Zhang Y, Jia L, Tian X, Gao N. HLA-DRB genotype and specific IgE responses in patients with allergies to penicillins. Chin Med J (Engl). 2006;119(6):458-66.
24. Jiang Q, Greenberg RA. Deciphering the BRCA1 Tumor Suppressor Network. J Biol Chem. 2015 Jul 17;290(29):17724-32.