Número Atual: Julho-Setembro 2017 - Volume 1 - Número 3
- Imprimir
- Indicar
- Estatísticas
- (0)
Comentários - Como Citar
- Download da Citação
- Artigos Relacionados
-
Outros dos
Autores
Artigo Original
Reações adversas locais e sistêmicas à imunoterapia alérgeno-específica para ácaros em pacientes de ambulatório especializado de Hospital Universitário em são Paulo
Local and systemic adverse reactions to allergen-specific immunotherapy for mites among patients seen at a university hospital's specialty outpatient clinic in Sao Paulo
Cynthia Mafra Fonseca de Lima1; Alessandra Morais da Silva1; Giovanna Hernandes y Hernandes1; Adriana Teixeira Rodrigues2; Jorge Kalil2; Clóvis E. S. Galvao2
DOI: 10.5935/2526-5393.20170040
1. Faculdade de Medicina da Universidade Anhembi-Morumbi, Sao Paulo, SP
2. Hospital das Clínicas da Faculdade de Medicina da Universidade de Sao Paulo, Sao Paulo, SP
Endereço para correspondência:
Cynthia Mafra Fonseca de Lima
E-mail: mafracynthia@gmail.com
Submetido em: 28/06/2017
Aceito em: 14/07/2017.
Nao foram declarados conflitos de interesse associados à publicaçao deste artigo.
Financiamento FAPESP: Processo N° 2011/11192-2.
RESUMO
OBJETIVO: Relatar e classificar as reaçoes adversas à imunoterapia subcutânea (ITSC) com extratos de ácaros no tratamento de alergias.
MÉTODO: Foram incluídos 38 pacientes que receberam ITSC com extratos de Dermatophagoides pteronyssinus (Der p) isolado ou associado a Blomia tropicalis (Blo t). As reaçoes adversas sistêmicas que ocorreram durante o tratamento foram registradas e classificadas de acordo com a WAO - World Allergy Organization. Também foram registrados o tratamento instituído e a evoluçao do quadro.
RESULTADOS: A média de idade dos pacientes do estudo foi 36 anos. Foram administradas 1.127 doses de ITSC com extrato de Der p. Destas, 87,3% (984) provocaram reaçao. De acordo com a classificaçao proposta pela WAO, 35,49% das reaçoes foram Grau 1; 46,85% Grau 2; e 17,6% Grau 3. O tratamento utilizado foi: anti-histamínico em 81,3% das reaçoes, corticosteroide em 81,3%, e beta-agonista inalatório em 70% dos casos. A adrenalina foi administrada em 41% das reaçoes. No grupo que recebeu extrato associado de Der p e Blo t foram administradas 435 doses, das quais 155 (37,47%) resultaram em reaçoes, sendo 78% de Grau 1, e 21,9% de Grau 2. O tratamento utilizado foi: anti-histamínico em 77,2% das reaçoes, corticosteroide em 77,2% e beta-agonista inalatório em 58% dos casos.
CONCLUSAO: Na populaçao estudada, as reaçoes sistêmicas para Der p de acordo com a classificaçao da WAO, foram na sua maioria reaçoes Grau 2. Já na imunoterapia para Der p e Blo t associados, as reaçoes de Grau 1 prevaleceram. Embora seja um tratamento seguro, a imunoterapia pode levar ao aparecimento de reaçoes sistêmicas, e deve ser realizada pelo médico especialista, em ambiente adequado e equipado para tratamento de reaçoes sistêmicas.
Descritores: Alergia e imunologia, ácaros, imunoterapia, reaçoes adversas.
INTRODUÇAO
A imunoterapia alérgeno-específica (IT) foi introduzida por Noon e Freeman em 1911, quando estes inocularam extrato de pólen em um paciente com rinite alérgica sazonal a pólen. A imunoterapia foi, inicialmente, destinada ao tratamento da rinite alérgica e, atualmente, após conquistar credibilidade e notoriedade, está indicada para o tratamento das doenças alérgicas asma, rinite, conjuntivite, rinoconjuntivite, dermatite atópica induzida por aeroalérgenos e anafilaxia ao veneno de insetos himenópteros (abelhas, vespas e formigas). Consiste na administraçao de alérgenos em doses crescentes, até que se atinja a dose efetiva para induzir tolerância imunológica em pacientes alérgicos e cessar os sintomas decorrentes das exposiçoes posteriores ao alérgeno em questao. A asma, a rinite e a rinoconjuntivite alérgicas sao exemplos de doenças alérgicas que ocorrem de forma crônica por exposiçao contínua a alérgenos do ambiente, como os derivados de ácaros, polens, animais e fungos do ar. Essas alergias respiratórias, no Brasil, estao associadas, principalmente, à sensibilizaçao aos ácaros da poeira doméstica. A IT pode ser realizada através das vias subcutânea (ITSC) ou sublingual, sendo esta através da mucosa. Para as duas vias, extratos padronizados diluídos em diferentes soluçoes carreadoras sao utilizados. As diluiçoes dos extratos alergênicos deverao ser individualizadas para cada paciente candidato ao tratamento1,2.
Este tratamento foi reconhecido em 1998 pela Organizaçao Mundial de Saúde (OMS), como a única modalidade terapêutica capaz de alterar a evoluçao natural das alergias respiratórias e prevenir o surgimento de asma em crianças com rinite alérgica, além de novas sensibilizaçoes. Apesar de seguro, pode provocar reaçoes adversas locais ou sistêmicas, as quais podem levar ao atraso do tratamento ou, até mesmo, sua interrupçao2,3.
Ainda nao há um consenso sobre o momento mais adequado para o uso da adrenalina no tratamento das reaçoes sistêmicas à IT, que podem variar tanto com relaçao à gravidade quanto à evoluçao clínica. As reaçoes podem comprometer apenas um órgao, como no caso da urticária aguda, ou apresentar-se como anafilaxia grave, uma reaçao sistêmica potencialmente fatal. A evoluçao clínica e prognóstica também pode variar, nao sendo possível predizer como irá evoluir um quadro que, inicialmente, pode se apresentar como uma reaçao leve3,4.
O diagnóstico de anafilaxia, de acordo com as diretrizes de 2011, deve ser realizado quando, no mínimo, dois órgaos sistêmicos estiverem comprometidos. No entanto, esses critérios nao devem ser utilizados para diagnosticar a anafilaxia que pode, eventualmente, ocorrer durante a realizaçao da IT, pois nessa situaçao especial, está sendo introduzido um alérgeno para o qual o paciente sabidamente possui IgE específica e resposta de hipersensibilidade prévia. Logo, o retardo no diagnóstico da anafilaxia e do uso da adrenalina durante as reaçoes sistêmicas graves à IT está diretamente relacionado com o aumento da mortalidade5,6. Desta maneira, faz-se necessário ampliar os conhecimentos sobre as características clínicas e evoluçao destas reaçoes, visando à instituiçao do diagnóstico e tratamento adequados o mais rapidamente possível. Várias classificaçoes têm sido propostas ao longo do tempo, com o objetivo de padronizar o manejo das reaçoes adversas à IT. A classificaçao mais recente sugere, pela primeira vez, que apenas o envolvimento de um órgao pode ser indicativo do uso de adrenalina. Ainda, também, propoe o registro do momento em que foi realizado o tratamento com a adrenalina7,8.
Apesar de proposta há pouco mais de seis anos (2010)1, esta nova classificaçao vem sendo utilizada com sucesso em alguns países, e poderá trazer informaçoes úteis para uma futura padronizaçao do diagnóstico e tratamento das reaçoes adversas à IT. No entanto, nao há, até o momento, um estudo sobre o uso desta nova proposta de classificaçao das reaçoes adversas à IT no Brasil. O presente estudo propoe o registro e a classificaçao das reaçoes adversas à ITSC para ácaros apresentadas pelos pacientes do ambulatório especializado de Hospital Universitário em Sao Paulo, assim como o tratamento instituído, de acordo com os parâmetros atuais, com a finalidade de contribuir para o conhecimento sobre o diagnóstico e manejo das reaçoes adversas à ITSC.
MÉTODOS
Foram incluídos 38 pacientes de um Serviço Ambulatorial de Imunologia Clínica e Alergia que realizaram tratamento com ITSC para o controle da rinite, asma e conjuntivite alérgicas e dermatite atópica. Neste estudo, consideramos apenas os pacientes que já haviam recebido pelo menos 3 anos de imunoterapia na dose de manutençao.
Os extratos utilizados no tratamento destes pacientes foram de Dermatophagoides pteronissinus (Der p) isolado e também sua associaçao com Blomia tropicalis (Blo t) (Immunotech, Rio de Janeiro, Brasil), administrados em concentraçoes crescentes, atingindo a manutençao com 8 µg/mL de alérgeno principal em ambos os casos. O projeto foi aprovado pelo comitê de ética da instituiçao e todos os indivíduos assinaram previamente um termo de consentimento livre e esclarecido onde concordam com a sua participaçao nesta pesquisa.
As reaçoes adversas sistêmicas que ocorreram durante o tratamento com a ITSC foram registradas e classificadas de acordo com a proposta da WAO1. Também foi registrado o tratamento instituído e a evoluçao do quadro clínico.
RESULTADOS
A média de idade dos pacientes do estudo foi 36 anos (21 a 57 anos), sendo 52,6% do sexo masculino e 47,3% do sexo feminino. Dentre os pacientes incluídos na pesquisa, 36,8% foram previamente diagnosticados com rinoconjuntivite alérgica, enquanto 23,6% com asma, 15,7% com rinite, 13,1% com conjuntivite alérgica, 5,2% com dermatite atópica e, por fim, 5,2% com rinite, asma e conjuntivite em associaçao.
Foram administradas 1.127 doses de ITSC com extrato de Der p. Destas aplicaçoes, 87,3% (984) estiveram associadas a reaçao. De acordo com a classificaçao da WAO, 35,49% (349) das reaçoes foram Grau 1, 46,85% (461) foram Grau 2, e 17,6% (174) foram Grau 3. Nao ocorreram reaçoes Grau 4 ou 5. O tratamento utilizado foi: anti-histamínico em 81,3% (800) das reaçoes, corticosteroide em 81,3% (800) e beta-agonista inalatório em 74,4% (732) dos casos. A adrenalina foi administrada em 41% das reaçoes. O uso da adrenalina foi mais frequente nas reaçoes de grau 2 e 3.
A relaçao entre a concentraçao do alérgeno Der p que causou reaçao e sua gravidade pode ser observada na Figura 1.
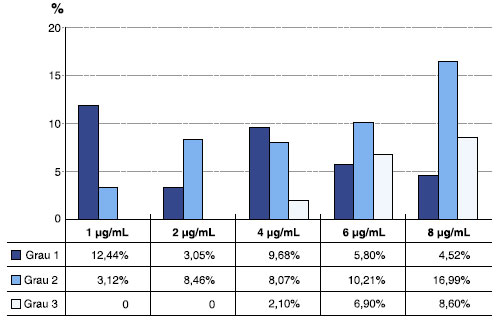
Figura 1 Distribuiçao das reaçoes por gravidade e de acordo com a concentraçao de Der p administrada
As reaçoes ocorreram, em sua maioria, nos primeiros 10 a 15 minutos após a administraçao da imunoterapia. As manifestaçoes clínicas das reaçoes foram bastante variadas e se distribuíram conforme mostrado na Tabela 1.
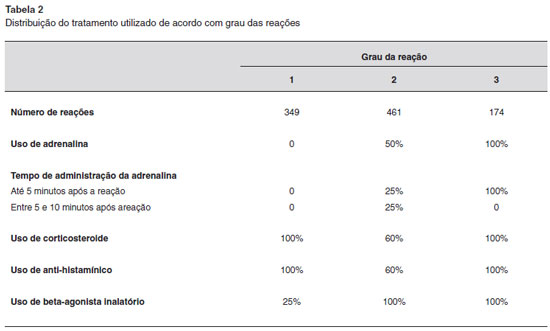
Sintomas abdominais e cardiovasculares nao foram descritos nestas reaçoes. Na Tabela 2 descrevemos a distribuiçao do tratamento de acordo com o grau das reaçoes.
No grupo que recebeu extrato associado de Der p e Blo t foram administradas 435 doses, das quais 155 (37,47%) resultaram em reaçoes, sendo 78% (121) de Grau 1 e 21,9% (34) de Grau 2. As reaçoes de Grau 3, 4 e 5 nao ocorreram. O tratamento utilizado foi: anti-histamínico em 77,2% (119) das reaçoes, corticosteroide em 77,2% (119), e beta-agonista inalatório em 58% (90) dos casos.
A Figura 2 mostra a relaçao entre a concentraçao do alérgeno Der p + Blo t que causou reaçao e sua gravidade. As manifestaçoes clínicas das reaçoes encontram-se resumidas na Tabela 3.
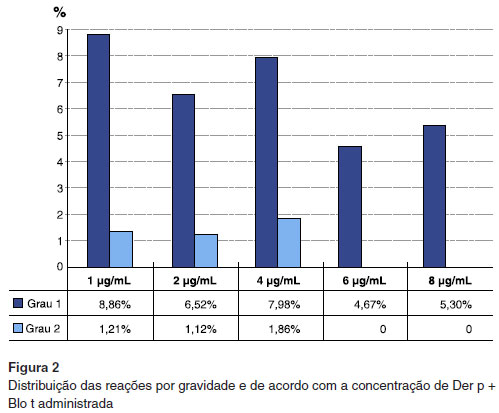
Figura 2 Distribuiçao das reaçoes por gravidade e de acordo com a concentraçao de Der p + Blo t administrada
DISCUSSAO
As reaçoes à ITSC manifestam-se com sintomas cutâneos (prurido, urticária, eritema e angioedema), oculares (lacrimejamento, prurido), respiratórios (sibilância, tosse e coriza) e podem chegar a ser reaçoes sistêmicas graves. O risco das reaçoes pode variar de acordo com o tipo de alérgeno, concentraçao da imunoterapia e modo de aplicaçao5. Em nossa amostra, foram utilizados os extratos contendo Dermatophagoides pteronyssinus (Der p) isolado e, também, associado com Blomia tropicalis (Blo t).
Observamos uma taxa de reaçao (87,3%) bem maior com o extrato isolado de Der p, quando comparamos com o grupo que recebeu a associaçao Der p + Blo t (37,4%). A menor taxa de reaçao com a associaçao de extratos pode ser devido ao fato de que, embora a dose de manutençao continuasse com 8 µg/mL de alérgenos, os mesmos foram divididos entre Der p e Blot (4 µg/mL de cada um). Os sintomas sistêmicos ocorreram com concentraçoes de extrato que variaram de 1 a 8 µg/mL de alérgeno por aplicaçao.
A literatura descreve que 29% das reaçoes sao leves, 57% sao moderadas, e 14% sao graves5,6, dados semelhantes aos descritos neste estudo. Ainda, 12,5% e 14% das reaçoes graves e nao graves, respectivamente, ocorrem após 30 minutos da injeçao, o que também foi observado em nossa casuística, reforçando a orientaçao para que o paciente permaneça em observaçao pelo menos até 30 minutos após a administraçao da dose. Manifestaçoes cutâneas ocorrem com maior frequência nas reaçoes nao fatais (70%) quando comparadas às fatais (29%). A obstruçao das vias aéreas superiores e broncoespasmo sao relatadas frequentemente nas reaçoes fatais e nao fatais, e a falência respiratória foi descrita em 94% das reaçoes fatais5. A asma nao controlada é um fator de risco para reaçao, e a maioria dos pacientes com PEF < 70% tem risco de reaçao5,6.
Os sintomas cutâneos como eritema e prurido foram os mais prevalentes no estudo, tanto na imunoterapia com extrato isolado de Der p quanto na associaçao deste com Blo t, reforçando que as reaçoes de grau 1 sao, de fato, comuns no tratamento com imunoterapia. Na sequência, aparecem os respiratórios, especialmente, a exacerbaçao da rinite e a sibilância. Esses dados estao de acordo com a literatura.
Como observado em nossa amostra e já descrito previamente na literatura7,8, as reaçoes locais nao foram preditivas de reaçoes sistêmicas posteriores, o que nos permitiu manter a conduta de nao ajustar a dose na administraçao subsequente a uma reaçao local, pois tal ajuste nao garante proteçao contra possíveis reaçoes futuras, acarretando em prolongamento do tempo de tratamento e do custo do mesmo9.
Conforme estudo da literatura, menos de 6% dos pacientes nao recebem adrenalina nas reaçoes nao fatais, quando comparado com 43% das reaçoes fatais. A administraçao da adrenalina em até 20 minutos ocorreu em 94% dos pacientes com reaçao nao fatal versus 82% de reaçoes fatais5.
No nosso estudo, a maioria das reaçoes ocorreu durante a fase de manutençao e sempre dentro de 30 minutos após aplicaçao, salvo raras exceçoes, com desenvolvimento de reaçao leve de Grau 1, geralmente eritema local, após 24 horas da aplicaçao. Uma boa parte das reaçoes (41%) resultou em uso de adrenalina, e nestes casos os pacientes estavam recebendo a dose de manutençao de 8 µg/mL. Este dado nos faz refletir sobre a individualizaçao da dose de manutençao e os ajustes necessários para alérgenos perenes aos quais o paciente encontrase continuamente exposto. Após medicados, todos os pacientes evoluíram bem, com melhora rápida e progressiva dos sintomas causados pelas reaçoes.
Concluímos entao que, embora seja um tratamento seguro, a IT pode levar ao aparecimento de reaçoes sistêmicas, e a equipe médica precisa estar preparada para reconhecer rapidamente a reaçao e tratá-la. Nossos dados mostram, também, a necessidade de manter o paciente em observaçao após a aplicaçao da IT por, pelo menos, 30 minutos devido ao aparecimento de eventuais reaçoes. Portanto, reforçamos que a indicaçao e realizaçao do tratamento das doenças alérgicas com a IT deve ser realizada pelo médico especialista, em ambiente adequado e equipado para tratamento de reaçoes sistêmicas, além de dispor de equipe treinada para dar este suporte ao paciente.
REFERENCIAS
1. Simons FER, Ardusso LRF, Bilo MB, Dimov V, Ebisawa M, El-Gamal YM, et al. 2012 Update: World Allergy Organization Guidelines for the assessment and managementof anaphylaxis. www.co-allergy. com 2012;12(4):381-99.
2. Abramson MJ, Puy RM, Weiner JM. Allergen immunotherapy for asthma. Cochrane Database Syst Rev. 2003;(4):CD001186.
3. Cox L, Nelson H, Lockey R, Calabria C, Chacko T, Finegold I, et al. Allergen immunotherapy: a practice parameter third update. J Allergy Clin Immunol. 2011;127(1):S1-S55.
4. Tankersley MS, Butler KK, Butler WK, Goets DW. Local reactions during allergen immunotherapy do not require dose adjustment. J Allergy Clin Immunol. 2000;106:840-3.
5. Bernstein DI, Simons FER, Feldweg AM. Anaphylaxis induced by subcutaneous allergen immunotherapy - UpToDate 2013;6(16).
6. Greineder DK. Risk management in allergen immunotherapy. J Allergy Clin Immunol. 1996;98:S330-4.
7. Nesselroad TD, Parker A, Calabria C. Systemic reactions to skin prick testing are not associated with an increased risk of systemic reactions to subcutaneous immunotherapy. J Allergy ClinImmunol. 2010;125(2)S37.
8. Cox L, Larenas-Linnemann D, Lockey RF, Passalacqua G. Speaking the same language: The World Allergy Organization subcutaneous immunotherapy systemic reaction grading system. J Allergy ClinImmunol. 2010;125:569-74.
9. Coop CA, Tankersley MS. Dose adjustment practices among allergists for local reactions to immunotherapy. Ann Allergy Asthma Immunol. 2007;99:77-81.