Número Atual: Setembro-Outubro 2013 - Volume 1 - Número 5
Editorial
Dermatite atópica e filagrina: restaurando barreiras para o controle da doença
Atopic dermatitis and filaggrin: restoring barriers to control the disease
Renata N. Cardili1; Janaina M.L. Melo1; Ana M. Roselino1; Adriana S. Moreno1; Ana Paula M. Castro2; L. Karla Arruda1
DOI: 10.5935/2318-5015.20130033
1. Departamento de Clínica Médica, Faculdade de Medicina de Ribeirao Preto, Universidade de Sao Paulo, FMRP-USP
2. Instituto da Criança, Faculdade de Medicina, Universidade de Sao Paulo, IC-FMUSP
Endereço para correspondência:
Luisa Karla Arruda
E-mail: karla@fmrp.usp.br
A dermatite atópica (DA) é elencada como uma das dermatoses inflamatórias mais comuns, com prevalência mundial variando entre 1% e 20%1. Na América Latina, incluindo o Brasil, a prevalência média da DA entre adolescentes e crianças, avaliada pelo International Study of Asthma and Allergies in Childhood (ISAAC), está entre 10,6% e 11,3%, respectivamente2. O impacto desta doença na qualidade de vida dos pacientes e suas famílias é marcante1.
Defeitos na barreira cutânea em pacientes com DA, que poderiam constituir a alteraçao primária na doença, tem sido identificados em estudos recentes. Esses defeitos levariam à maior penetraçao de alérgenos, micro-organismos, particularmente Staphylococus aureus e substâncias irritantes, que por sua vez estimulariam a resposta imune na direçao de um perfil Th2. Suporte para esta teoria vem da descoberta da associaçao da DA com mutaçoes no gene da Filagrina (Filaggrin, filament-aggregating protein/FLG), proteína essencial para a formaçao e manutençao da integridade da barreira cutânea3.
Muitos dos defeitos da barreira cutânea que têm sido descritos na DA têm origem no estrato córneo. Neste contexto, é importante ressaltar que a epiderme apresenta estruturaçao altamente organizada, cuja proliferaçao celular se inicia na camada basal, com progressao ascendente para originar o estrato córneo, configurando as camadas intermediárias - espinhosa e granulosa. As células na camada granulosa liberam precursores lipídicos incluindo glicosilceramida, esfingomielina e fosfolípides, que sao processados enzimaticamente para formarem colesterol, ácidos graxos e principalmente ceramidas, os lipídeos predominantes na pele humana. As células entao perdem o seu núcleo, para constituir lamelas ricas em lipídeos e proteínas, que, organizadamente, serao empilhadas para constituir o estrato córneo. Lipídios hidrofóbicos em dupla camada fortalecem a integridade do estrato córneo e auxiliam na manutençao da hidrataçao na pele eutrófica4 (Figura 1). Pelo menos 60 genes presentes em um cluster no cromossomo 1q21 designado como Epidermal differentiation complex (EDC) foram identificados, os quais codificam proteínas importantes para a diferenciaçao terminal da pele. Dentre estas proteínas, destaca-se a Filagrina, além de outras proteínas incluindo Serine protease inhibitor, Kazal type 5 (SPINK5), Loricrina (LOR), e Involucrina3,5.
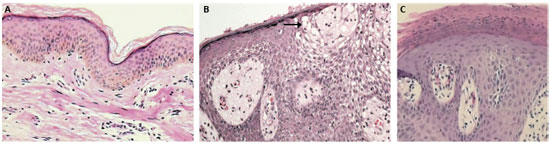
Figura 1 A) Fotomicrografia de biópsia de pele normal, demonstrando a organizaçao da epiderme em camadas basal, espinhosa, granulosa e estrato córneo. B) Biópsia de lesao de dermatite atópica aguda, mostrando dermatite espongiótica acentuada e formaçao de vesículas (seta) na epiderme. C) Corte de pele com psoríase revelando acantose regular, paraceratose, presença de debris neutrofílicos na camada córnea (microabscessos) e dilataçao das papilas dérmicas. Coloraçao por hematoxilina eosina (X100). Histopatologia e imagens por Dr. Marcus Vinícius de Castro Barros, médico assistente do Serviço de Patologia do Hospital da Clínicas da Faculdade de Medicina de Ribeirao Preto - USP
A patogênese da DA inclui ativaçao de linfócitos de perfil Th2, e produçao de citocinas IL-4, IL-5, IL-13, e IL-31, particularmente nas fases iniciais e exacerbaçoes da doença. Resposta Th1 tem sido também identificada nas fases crônicas, em conjunto com a resposta Th2. A produçao de citocinas por queratinócitos, particularmente TSLP (Thymus stromal lymphopoietin) e IL-33, contribuem para a patogênese da doença5,6. Está bem estabelecido que a inflamaçao crônica tem papel importante em desencadear as manifestaçoes clínicas, incluindo prurido e lesoes cutâneas características da DA, e em promover alteraçoes na barreira cutânea6.
Estudo recente avaliou a eficácia do Dupilumabe em pacientes adultos com DA moderada a grave7. O Dupilumabe é um anticorpo monoclonal humanizado que bloqueia a cadeia alfa do receptor da IL-4 compartilhada com IL-13, e dessa forma leva à supressao da sinalizaçao intracelular por IL-4 e IL-13. O bloqueio da açao de IL-4 e IL-13 por Dupilumabe, prescrito por 4 ou 12 semanas, resultou em melhora marcante das lesoes cutâneas e na reduçao substancial do prurido em pacientes com DA. A melhora clínica foi acompanhada da reduçao nos níveis de biomarcadores de ativaçao Th2, como TARC (Thymus and activation-regulated chemokine) e IgE total, e de proliferaçao como Queratina-16, além de melhora do transcriptoma nas lesoes cutâneas. Os resultados expandem o benefício potencial desta nova terapia biológica além da asma, para uma segunda doença alérgica, a DA. Estudo prévio demonstrou a eficácia do Dupilumabe em pacientes com asma moderada a grave, com níveis elevados de eosinófilos8.
A contribuiçao relativa da disfunçao de barreira e da desregulaçao imunológica para o fenótipo de DA permanece em debate6. Mutaçoes no gene da Filagrina estao associadas à formaçao do estrato córneo desorganizado, com estrutura errática e arquitetura anormal da dupla camada; à alteraçao no perfil de distribuiçao de lipídeos; a aumento do pH cutâneo, da proteólise e da perda transepitelial de água; e à maior susceptibilidade a infecçoes por bactérias, vírus e fungos3. De forma interessante, em modelos de pele humana e culturas de queratinócitos foi demonstrado que histamina e uma variedade de citocinas, incluindo IL-4, IL-17, IL-22, IL-25 e IL-31, têm a capacidade de diminuir a produçao de Filagrina ou mesmo reprimir a expressao do gene da Filagrina5, sugerindo um papel integrado desses mecanismos no desenvolvimento da doença.
Na pele normal, a Filagrina é sintetizada como uma pro-proteína (pro-filagrina) de alto peso molecular, com aproximadamente 400 kDa, nas células da camada granulosa. Sua estrutura é composta de 10 a 12 monômeros repetitivos de peso molecular de 37 kDa, além de uma porçao N-terminal que contém domínio de ligaçao ao cálcio S-100, e uma porçao C-terminal de funçao desconhecida. Como pro-proteína, nao tem atividade biológica, entretanto, um processo de defosforilaçao causa liberaçao dos monômeros individuais, que sao a forma ativa da proteína. Monômeros da Filagrina têm importante açao no agrupamento das lamelas que constituirao a camada córnea, de forma que elas fiquem organizadas de maneira paralela e compacta. Após realizarem esta funçao, os monômeros sao posteriormente degradados por cisteina-peptidases, gerando Natural Mosturizing Factors (NMFs), que incluem aminoácidos livres, ácido urocânico (UCA) e ácido pirrolidônico carboxílico (PCA). Os NMFs promovem captaçao e aprisionamento da água, e manutençao do pH ácido da pele, essencial para prevenir a adesao e penetraçao de micro-organismos3.
Pelo menos 47 mutaçoes com perda de funçao já foram identificadas no gene que codifica a Filagrina em pacientes com DA. As duas mutaçoes originalmente descritas, R501X e 2282del4, mostraram frequência de 80% em pacientes irlandeses com DA, entretanto perfis distintos de mutaçoes foram identificados em pacientes da Europa e da Asia3. Nao há estudos publicados descrevendo mutaçoes no gene da Filagrina em amostragem brasileira de indivíduos saudáveis ou em pacientes com DA. Embora a descoberta de mutaçoes no gene da Filagrina represente um grande avanço no entendimento da DA, ela nao explica toda a patogênese. Mesmo entre pacientes com DA grave, mutaçoes na Filagrina têm sido identificadas em 50% dos pacientes3,9. É possível que a reduçao da expressao de outras proteínas estruturais como Involucrina, Loricrina, Filagrina-2 e Hornerina na pele de pacientes com DA, quando comparada à pele normal, tenha papel relevante5. Além disso, outras alteraçoes encontradas em pacientes com DA podem comprometer a funçao da barreira cutânea, incluindo deficiências na imunidade inata, com diminuiçao de peptídeos antimicrobianos como as beta-defensinas e catelicidinas; níveis diminuídos de ceramidas ou mudanças na composiçao das ceramidas; e diminuiçao de proteínas importantes na integridade das tight junctions na epiderme com as da família das claudinas. Entender como esses eventos acontecem ao longo do tempo será primordial para identificar novos alvos terapêuticos a serem usados na DA5.
IMPLICAÇOES PARA O TRATAMENTO DA DERMATITE ATOPICA
O tratamento da DA, particularmente de pacientes com formas moderadas e graves da doença, ainda permanece um desafio. É possível restaurar a barreira cutânea na DA? Tem sido demonstrado que o tratamento anti-inflamatório da DA com corticosteroides tópicos ou inibidores da calcineurina leva ao aumento da expressao da Filagrina, e diminuiçao da infecçao por S. aureus. Além do tratamento medicamentoso, estratégias voltadas à identificaçao de fatores causais e desencadeantes da reaçao inflamatória na DA para cada paciente em particular poderiam ter papel importante na restauraçao da barreira cutânea. É possível se usar hidratantes e emolientes com formulaçao que inclui produtos da degradaçao da Filagrina, como PCA ou NMFs, e/ou ceramidas e outros elementos lipídicos em sua composiçao, promovendo açao direcionada à restauraçao da barreira cutânea na DA4,5.
Vários estudos documentam de forma consistente que, mesmo a pele de pacientes com DA que tem aspecto macroscópico normal, apresenta alteraçoes da barreira cutânea, além de infiltraçao de linfócitos Th2 e produçao de citocinas pró-inflamatórias3-5. A implicaçao destes achados é que o tratamento proativo diário em longo prazo (hidrataçao, prevençao de infecçoes, uso profilático de corticoide ou inibidor de calcineurina tópicos, duas vezes por semana, em áreas previamente afetadas, atençao a aspectos psicossociais, etc.), deve ser encorajado junto aos pacientes e suas famílias, em oposiçao ao tratamento reativo, apenas quando os sintomas aparecem5. Estudos mostram que é frequente a demora em iniciar o tratamento após o início dos sintomas, por razoes incluindo falta de um plano de açao sistemático, nao disponibilidade de medicamentos, medo do uso de certos medicamentos como corticosteroides tópicos, dentre outros5. É importante orientaçao detalhada sobre a doença, sua história natural, e tratamento precoce e adequado das exacerbaçoes.
O papel da Vitamina D na dermatite atópica e em outras doenças alérgicas tem sido extensamente investigado, e estudos têm demonstrado potenciais efeitos da Vitamina D em aumentar a atividade dos peptídeos antimicrobianos e suprimir a resposta inflamatória, que poderiam indiretamente contribuir para restaurar a barreira cutânea10. Neste número do BJAI, Robl et al. discutem estudos atuais sobre o impacto da deficiência de Vitamina D no diagnóstico e gravidade da dermatite atópica11. Os autores concluem que a suplementaçao da Vitamina D pode trazer benefícios no tratamento da DA, entretanto que mais estudos se fazem necessários para determinar se existe alguma relaçao entre os níveis de Vitamina D e a gravidade da DA.
Por fim, em estudo recente, foi testada a construçao de monômero de Filagrina ligado de forma covalente a peptídeo que promove penetraçao celular na epiderme (RMR). A aplicaçao in vitro de FLG+RMR recombinante em modelo de tecido de epiderme humana reconstruída resultou na penetraçao no estrato granuloso, camada responsável pela deficiência de Filagrina12. Além disso, aplicaçao tópica in vivo de FLG+RMR em camundongos flaky tail deficientes em Filagrina levou à internalizaçao e processamento de FLG+RMR, com restauraçao do fenótipo normal. Estes resultados encorajadores sugerem que monômeros de Filagrina conjugados a RMR, aplicados topicamente, sao capazes de penetrar na epiderme, serem internalizados e processados em tamanho semelhante aos peptídeos encontrados na barreira cutânea natural, para restaurar a funçao necessária da barreira cutânea, podendo ter utilidade terapêutica em pacientes com DA.
CONCLUSOES
Há evidências consistentes de que defeitos na barreira cutânea contribuem para a patogênese da DA. Tratamentos tópicos que restaurem a barreira cutânea constituem uma importante estratégia no manejo de pacientes com DA. Mutaçoes no gene que codifica a Filagrina constituem-se no fator genético mais importante associado ao risco aumentado nao só de ocorrência de DA, mas também de desenvolvimento de formas mais graves e de início mais precoce de DA, e de surgimento de asma e de alergia a certos alimentos, particularmente amendoim, em pacientes com DA3,13. É possível que a análise de mutaçoes no gene da Filagrina em pacientes com DA possa ser útil clinicamente, ao identificar um subgrupo de pacientes que se beneficiarao com as novas terapêuticas para restauraçao da barreira cutânea baseadas na reposiçao da Filagrina. Essas novas terapêuticas têm potencial de fornecer uma soluçao mais permanente do que se dispoe atualmente.
REFERENCIAS
1. Bieber T. Atopic dermatitis. N Engl J Med. 2008;358(14):1483-94.
2. Solé D, Mallol J, Wandalsen GF, Aguirre V; Latin American ISAAC Phase 3 Study Group. Prevalence of symptoms of eczema in Latin America: results of the International Study of Asthma and Allergies in Childhood (ISAAC) Phase 3. J Investig Allergol Clin Immunol. 2010;20(4):311-23.
3. Irvine AD, McLean WH, Leung DY. Filaggrin mutations associated with skin and allergic diseases. N Engl J Med. 2011;365(14):1315-27.
4. Agrawal R, Woodfolk JA. Skin barrier defects in atopic dermatitis. Curr Allergy Asthma Rep. 2014;14(5):433.
5. Czarnowicki T, Krueger JG, Guttman-Yassky E. Skin barrier and immune dysregulation in atopic dermatitis: an evolving story with important clinical implications. J Allergy Clin Immunol Pract. 2014;2(4):371-9.
6. Eyerich K, Novak N. Immunology of atopic eczema: overcoming the Th1/Th2 paradigm. Allergy. 2013;68(8):974-82.
7. Beck LA, Thaçi D, Hamilton JD, Graham NM, Bieber T, Rocklin R, et al. Dupilumab treatment in adults with moderate-to-severe atopic dermatitis. N Engl J Med. 2014;371(2):130-9.
8. Wenzel S, Ford L, Pearlman D, Spector S, Sher L, Skobieranda F, et al. Dupilumab in persistent asthma with elevated eosinophil levels. N Engl J Med. 2013;368(26):2455-66.
9. Mohiuddin MS, Ramamoorthy P, Reynolds PR, Curran-Everett D, Leung DY. Increased compound heterozygous filaggrin mutations in severe atopic dermatitis in the United States. J Allergy Clin Immunol Pract. 2013;1(5):534-6.
10. Muehleisen B1, Gallo RL. Vitamin D in allergic disease: shedding light on a complex problem. J Allergy Clin Immunol. 2013;131(2):324-9.
11. Robl R, Carvalho VO, Uber M, Abagge KT, Pereira RM. Vitamina D e dermatite atópica: o que há de novo? Braz J Allergy Immunol. 2013;1(5):261-6.
12. Stout TE, McFarland T, Mitchell JC, Appukuttan B, Stout JT. Recombinant filaggrin is internalized and processed to correct filaggrin deficiency. J Invest Dermatol. 2014;134(2):423-9.
13. McAleer MA, Irvine AD. The multifunctional role of filaggrin in allergic skin disease. J Allergy Clin Immunol. 2013;131:280-91.



