Número Atual: Julho-Setembro 2021 - Volume 5 - Número 3
- Imprimir
- Indicar
- Estatísticas
- (0)
Comentários - Como Citar
- Download da Citação
- Artigos Relacionados
-
Outros dos
Autores
Artigo Original
Avaliação do emprego da imunoglobulina humana endovenosa sobre a densidade de infecções em pacientes com mieloma múltiplo
Evaluation of the use of human intravenous immunoglobulin on the incidence density of infections in patients with multiple myeloma
Elisângela Aparecida Galdino Menezes1,2; Guilherme Moreira Borges Araújo2; Isadora Andrade Rabelo2; Beatriz Julião Vieira Aarestrup3; Paula Fonseca Aarestrup4; Edir Paula Cordeiro Cheloni5; Matheus Fonseca Aarestrup5; Fernando Monteiro Aarestrup6,7
DOI: 10.5935/2526-5393.20210043
1. Faculdade de Ciências Médicas e da Saúde de Juiz de Fora - SUPREMA - Juiz de Fora, MG, Brasil
2. Centro Universitário de Patos de Minas - UNIPAM - Patos de Minas, MG, Brasil
3. Universidade Federal de Juiz de Fora - UFJF - Instituto de Ciências Biológicas - Juiz de Fora, MG, Brasil
4. Universidade Federal do Estado do Rio de Janeiro - UNIRIO - Rio de Janeiro, RJ, Brasil
5. Centro Universitário Presidente Tancredo de Almeida Neves - UNIPTAN - São João del-Rei, MG, Brasil
6. Universidade Federal de Juiz de Fora - UFJF - Juiz de Fora, MG, Brasil
7. Hospital Maternidade Therezinha de Jesus, Serviço de Alergia e Imunologia - Juiz de Fora, MG, Brasil
Endereço para correspondência:
Elisângela Aparecida Galdino Menezes
E-mail: elisangela@unipam.edu.br
Submetido em: 24/03/2021
Aceito em: 18/04/2021
Não foram declarados conflitos de interesse associados à publicação deste artigo
RESUMO
INTRODUÇÃO: O mieloma múltiplo (MM) é uma neoplasia hematológica que cursa com hipogamaglobulinemia e consequente imunodeficiência secundária. Uma das principais causas de morbimortalidade desses pacientes são infecções. Objetivou-se com esse estudo avaliar o impacto da reposição de imunoglobulina endovenosa (IgIV) na taxa de infecções em pacientes portadores de MM.
MÉTODOS: Trata-se de um estudo de análise documental, com variáveis qualitativas e quantitativas, com objetivo de realizar análise retrospectiva dos prontuários de pacientes com MM que receberam tratamento com imunoglobulina humana endovenosa em um hospital privado na cidade de Patos de Minas, MG, Brasil, no período de 01/05/2016 a 31/12/2020. Foram coletados dados epidemiológicos, resultados de exames, episódios de infecções, eventos adversos da medicação e desfecho dos pacientes nos prontuários analisados.
RESULTADOS: Foram identificados 10 pacientes com diagnóstico de MM, todos receberam IgIV na dose de 300 a 400 mg/kg/mês. Nenhuma reação adversa relacionada ao uso da IgIV foi registrada nos prontuários. Foram identificados seis quadros infecciosos que ocorreram em quatro pacientes. Nenhum diagnóstico de sepse foi registrado. A densidade de incidência de infecções foi de 0,28 episódios/pacientes-ano.
CONCLUSÃO: A densidade de incidência de infecções observada no presente estudo foi significativamente menor em comparação ao que se tem registro na literatura, sugerindo importante papel da IgIV na prevenção de infecções em pacientes com MM.
Descritores: Idiótipos de imunoglobulina, síndromes de imunodeficiência, mieloma múltiplo.
INTRODUÇÃO
O mieloma múltiplo (MM) é responsável por 1% dos casos totais de neoplasia e por mais de 10% das neoplasias hematológicas, sendo a segunda forma mais comum neste grupo, atrás apenas do linfoma não Hodgkin1-4. Caracteriza-se pela proliferação de células plasmáticas clonais na medula óssea e tipicamente é acompanhado pela secreção de imunoglobulinas monoclonais que são detectáveis no soro ou na urina. As células malignas encontram-se, geralmente, na medula óssea, mas podem ser encontradas no sangue periférico, em órgãos e em tecidos moles1. Clinicamente, o MM é caracterizado por hipercalcemia, insuficiência renal, anemia e/ou lesões líticas, e frequentemente se associa à doença óssea e ao aumento do risco para infecções, fatores associados à morbimortalidade. Sua incidência no Brasil é desconhecida, porém dados americanos estimam incidência de 4-5 indivíduos por 100.000, com pico entre 60 e 70 anos, sendo incomum apresentar-se antes dos 40 anos1,3,4.
A doença faz parte de uma série de distúrbios referidos como gamopatias monoclonais. A frequência de hipogamaglobulinemia está associada à progressão da doença e acomete de 45% a 83% dos pacientes, comprometendo o funcionamento do seu sistema imunológico. Soma-se a isso a característica de que a maioria dos pacientes é idosa e vulnerável a infecções oportunistas e a possibilidade de as novas opções terapêuticas para a doença levarem à imunossupressão cumulativa. De fato, atualmente são descritos patógenos que antes não eram relacionados ao MM, como, por exemplo, varicela-zoster, citomegalovírus e infecções graves causadas por fungos como os Aspergillus spp5. Além disso, o Streptococcus pneumoniae, juntamente com as bactérias Gram negativas, como Haemophilus influenzae continuam tendo importante papel nestas infecções6. Dessa forma, múltiplos fatores são responsáveis pelo aumento da susceptibilidade às infecções, que têm caráter variante de acordo com a evolução da doença2.
As infecções são uma das principais causas de morbimortalidade em pacientes com MM, e afetam com maior frequência os tratos respiratório e urinário, podendo ou não levar à sepse6. Além disso, o MM é um conhecido fator preditivo de recorrência de infecções, especialmente pelo pneumococo, o que se correlaciona a quadros graves, resistência a antimicrobianos e mortalidade elevada6. Desta forma, a profilaxia é uma importante aliada para evitar infecções que podem evoluir com desfecho negativo. Deve-se lembrar ainda que tais pacientes, embora necessitem ser imunizados, desenvolvem respostas inadequadas às vacinações devido ao quadro de imunossupressão3.
Apesar de escassos, estudos mostraram redução da ocorrência de infecções com o uso de IgIV em paciente com distúrbios linfoproliferativos que cursam com hipogamaglobulinemia7. Dados norte-americanos sugerem que a imunoglobulina humana intravenosa (IgIV) pode ser útil no tratamento de pacientes com infecções bacterianas recorrentes graves em caso de imunodeficiência secundária. Além disso, para pacientes com hipogamaglobulinemia, é preconizado o uso de IgIV3.
Estudos das décadas de 1980 e 1990 apontam que a reposição de Ig é eficaz em pacientes portadores de mieloma multiplo7,8. Desde então, o uso de IgIV é tido como uma importante opção terapêutica profilática em pacientes na fase tardia da doença.
Ensaio inicial randomizado e controlado por placebo mostrou que IgIV diminuiu a prevalência de infecções em pacientes com MM durante a fase de platô da doença. Nenhum episódio de sepse ou de pneumonia ocorreu no grupo tratado contra 10 no grupo placebo (P 5,002), e de 57 infecções graves, 38 ocorreram em 470 pacientes-mês com placebo versus 19 em 449 pacientes-mês com IgIV (P 5 .019). A IgIV também protegeu contra infecções recorrentes (p = 0,021) em 60 pacientes que completaram um ano8.
Revisão sistemática e metanálise de dados de 9 ensaios clínicos randomizados avaliaram medidas de resultados de mortalidade por todas as causas e infecções graves em pacientes com CLL e MM que receberam profilaxia com IgIV comparado ao grupo controle. Os dados evidenciaram uma diminuição significativa na ocorrência de infecções graves, com um risco relativo de 0,45 e uma diminuição significativa nas infecções clínicas documentadas, levando os investigadores a recomendar a consideração de IgIV em MM para casos devidamente selecionados. O estudo não demonstrou aumento da sobrevida nestes pacientes9.
A Associação Europeia de Hematologia (EHA) e a Associação Europeia de Oncologia Médica (ESMO), em suas diretrizes, não recomendam a utilização de IgG profilática rotineiramente, porém pode ser usada em pacientes devidamente selecionados, com níveis séricos de IgG baixos (< 400-500 mg) e pelo menos duas infecções graves com necessidade de hospitalização no último ano10.
A American Academy of Allergy, Asthma and Immunology (AAAI) recomenda o uso de IgIV em pacientes com MM com infecções bacterianas graves recorrentes, que possuem níveis séricos insuficientes de anticorpos para difteria, tétano e pneumococo após imunização11.
O protocolo da ANVISA quanto ao uso de IgIV segue as mesmas recomendações, apesar de não especificar a definição de uma infecção secundária grave e infecções recorrentes, e sugere mais estudos para uma indicação formal desse hemoderivado2,12. Podemos encontrar na literatura diversos protocolos de utilização de Ig em imunodeficiências secundárias, incluindo MM13-16. Assim, considerando a relevância do tratamento profilático para infecções em pacientes com mieloma múltiplo, esse estudo objetivou avaliar a incidência de infecções em pacientes com diagnóstico de MM que fizeram uso de IgIV durante o tratamento.
METÓDOS
Trata-se de um estudo de análise documental, com variáveis qualitativas e quantitativas, com objetivo de realizar uma análise retrospectiva dos prontuários de pacientes que receberam tratamento com imunoglobulina humana endovenosa em um hospital privado na cidade de Patos de Minas, MG, no período de 01/05/2016 a 31/12/2020. O presente estudo foi aprovado pelo comitê de ética da instituição, sob o parecer 4.049.608 / CAAE 31550020.4.0000.5549.
Por meio do software de gerenciamento da farmácia do referido hospital, foram pesquisadas todas as dispensações de IgIV durante o período do estudo. Após identificação dos indivíduos que receberam o hemoderivado, foram solicitados junto ao Serviço de Arquivamento Médico e Estatística do hospital todos os prontuários desses indivíduos e selecionados aqueles em que o diagnóstico que justificou a prescrição da IgIV foi o MM. Desses prontuários foram colhidas informações como: identificação do paciente (idade e sexo), dados sobre a utilização de IgIV (número de dias que recebeu a medicação, quantidade, data de início do uso), número de meses de acompanhamento, dosagens laboratoriais de imunoglobulinas (A, G e M) no momento da indicação da IgIV, infecções diagnosticadas durante o tratamento, registro de eventos adversos relacionados ao uso do hemoderivado e desfecho dentro do período estudado. Para notificação das infecções, não foi ponderada a gravidade, sendo consideradas quaisquer intercorrências infecciosas anotadas no prontuário.
Utilizou-se amostra de conveniência, composta pela totalidade de pacientes que preencheram os critérios de inclusão nos anos propostos para o estudo (Figura 1). Os dados foram tabulados em planilha do software Microsoft Excel®, analisados e apresentados também com o auxílio do Microsoft Excel®. A análise dos dados se deu por meio da estatística descritiva.
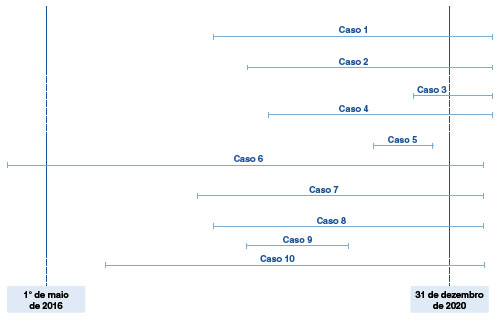
Figura 1
Distribuição dos pacientes/ano avaliados pelo estudo
Para levar em conta os períodos variáveis de seguimento e aproveitar o máximo de informação possível, foi utilizada uma medida chamada densidade de incidência. O cálculo apresenta como numerador o número de casos novos detectados durante um determinado período de tempo e, como denominador, a soma do tempo que cada indivíduo foi observado estando livre da doença (Figura 2). Neste cálculo, fica subentendido que pacientes com tempo de acompanhamento diferente podem contribuir com uma mesma quantidade de pessoas-tempo, nome dado ao valor obtido17.

Figura 2
Fórmula utilizada para calcular a densidade de incidência
RESULTADOS
Foram identificados 10 pacientes com diagnóstico de MM, sendo três mulheres e sete homens, com amplitude de idade entre 55 e 93 anos (71,8±10,4 anos). Considerando-se a população de 152.488 habitantes estimada pelo IBGE para 2019 no município de Patos de Minas, cidade em que se localiza o serviço de saúde que sediou a pesquisa, este estudo demonstra taxa de incidência de 6,5 indivíduos por 100.000 habitantes.
A média de tempo de acompanhamento dos pacientes foi de 25,2 meses. Todos receberam IgIV na dose de 300 a 400 mg/kg/mês. Nenhuma reação adversa relacionada ao uso do hemoderivado foi relatada em prontuário. Oito pacientes apresentaram redução sérica de imunoglobulinas (IgA, IgG ou IgM), em pelo menos um exame laboratorial, sendo a deficiência de IgM a mais prevalente (valores de normalidade). Não foram encontrados registros de dosagem de imunoglobulinas séricas em dois dos prontuários analisados. Não foi possível estabelecer relação entre os níveis de imunoglobulinas séricas e a incidência de infecções devido à inconstância dessa informação, nos prontuários analisados.
Quatro pacientes foram a óbito durante o período de acompanhamento, um deles devido a sepse relacionada a infecção do cateter de diálise, um de tromboembolismo pulmonar e dois de MM associado a senilidade. Foram identificados seis quadros infecciosos que ocorreram em quatro dos pacientes. Dessas infecções, três foram diarreia aguda, uma pneumonia, uma infecção do trato urinário e uma sepse. Tais episódios de infecções não foram estratificados quanto a sua gravidade. A densidade de incidência de infecções foi de 0,02/pacientes-mês.
DISCUSSÃO
A frequência de infecções em pacientes com MM varia de 1,29 a 2,22 episódios por paciente-ano. Durante os dois primeiros meses da quimioterapia inicial o risco de infecções é particularmente alto, podendo atingir até 4,68 infecções por paciente-ano. Estas infecções precoces são graves, com quase um terço delas provando serem fatais e muitas outras levando a aumento substancial da morbidade dos pacientes2.
A amostra estudada apresentou dados epidemiológicos compatíveis com o descrito na literatura acerca do MM, como idade média de 71,8 anos e maior incidência em homens. Considerando-se a baixa incidência da doença, a amostra é representativa.
A densidade de incidência de infecções apresentou-se significativamente reduzida (78,2% menor) na amostra analisada em relação ao que se tem registro na literatura, sugerindo importante papel da IgIV na prevenção de infecções em pacientes com MM. Por tratar-se de estudo retrospectivo e devido à coleta de informações acerca dos episódios de infecções ter sido feita em prontuário hospitalar, pode-se inferir que infecções leves, tratadas apenas em âmbito ambulatorial, não foram contabilizadas, assim como os possíveis efeitos colaterais do medicamento. Assim, é provável que a densidade de incidência de infecções esteja subestimada. No entanto, há de se considerar que as infecções que mais impactam sobre a morbimortalidade desses pacientes são aquelas que demandam internações, sendo, provavelmente, mais graves.
A baixa densidade de incidência de infecções encontrada por este trabalho foi ao encontro a um ensaio randomizado, placebo-controlado, duplo cego, conduzido na Inglaterra, que encontrou significativa diminuição nas taxas de infecções graves em pacientes com MM que fizeram uso de IgIV em relação ao grupo placebo. Diferentemente do grupo controle, nenhum dos pacientes em uso do tratamento profilático apresentou pneumonia grave ou sepse7.
Além disso, o uso de IgIV também mostrou reduzir significativamente a incidência de infecções graves de acordo com uma metanálise que avaliou pacientes com hipogamaglobulinemia e/ou infecções recorrentes portadores de MM e leucemia linfocítica9. Para pacientes com infecções recorrentes a IgIV já figura, inclusive, como uma recomendação profilática nas diretrizes de diagnóstico e manejo do MM de 2005 para pacientes na fase platô (recomendação nível A, evidência grau Ib) e em outros grupos de pacientes com MM (recomendação nível C, evidência grau IV)18.
Apesar do elevado custo da IgIV, há de se considerar os inestimáveis custos humanos e financeiros decorrentes das complicações clínicas infecciosas que atingem os pacientes com MM, dentre elas atraso na administração de quimioterapia, internações prolongadas, e até mesmo a morte.
O uso de IgIV tem sido sugerido como parte da abordagem terapêutica de pacientes com hipogamaglobulinemia secundária e infecções recorrentes e/ou graves7, no entanto a indicação formal desse hemoderivado como parte do protocolo de tratamento do MM e em protocolos clínicos e diretrizes terapêuticas para dispensação desse hemoderivado pelo MS ainda não é bem determinada.
Por ser tratar de um estudo retrospectivo de analise de prontuário, realizado em um serviço que utiliza IgIV como protocolo em todos os pacientes portadores de MM, não foi possível formar um grupo controle, uma melhor análise comparativa foi inviabilizada devido à falta de dados nos prontuários. Entretanto, esta limitação do estudo não inviabiliza sua contribuição sobre o assunto escasso na literatura científica.
CONCLUSÃO
O presente estudo visa contribuir para a elucidação dos efeitos do uso de IgIV em pacientes com MM independente dos níveis de Ig. Os resultados mostram um número de infecções inferior ao relatado na literatura, sugerindo o efeito profilático da IgIV em pacientes com diagnóstico de MM.
Novos estudos com o intuito de determinar melhor o papel da IgIV na prevenção de quadros infecciosos em pacientes com imunodeficiências secundárias, incluindo-se o MM, precisam ser delineados para que haja adequação dos protocolos e das diretrizes para o uso desse hemoderivado.
REFERÊNCIAS
1. Röllig C, Knop S, Bornhäuser M. Mieloma múltiplo. Lancet. 2015;385(9983):2197-208.
2. Kumar SK, Rajkumar V, Kyle RA, van Duin M, Sonneveld P, Mateos MV, et al. Multiple myeloma. Nat Rev Dis Primers. 2017;3:17046.
3. Kyle RA, Rajkumar V. Treatment of multiple myeloma: a comprehensive review. Clin Lymphoma Myeloma. 2009;9(4):278-88.
4. Júnior PAS, Carvalho HJ, Rabelo IB, Velano CEE. Mieloma múltiplo aos 30 anos: o avesso da epidemiologia. Rev Soc Bras Clin Med. 2015; 13(3):210-2.
5. Oliveira AL, Nucci M. Infecção em mieloma múltiplo. Rev Bras Hematol Hemoter. 2007;29(1):77-85.
6. Paradisi F, Corti G, Cinelli R. Infections in multiple myeloma. Infect Dis Clin North Am. 2001;15(2):373-84.
7. Chapel HM, Lee M. The use of intravenous immune globulin in multiple myeloma. Clin Exp Immunol. 1994;97(1):21-4.
8. Chapel HM, Lee M, Hargreaves R, Pamphilon DH, Prentice AG. Randomised trial of intravenous immunoglobulin as prophylaxis against infection in plateau-phase multiple myeloma. The UK Group for Immunoglobulin Replacement Therapy in Multiple Myeloma. Lancet. 1994 Apr 30;343(8905):1059-63.
9. Raanani P, Gafter-Gvili A, Paul M, Ben-Bassat I, Leibovici L, Shpilberg O. Immunoglobulin prophylaxis in chronic lymphocytic leukemia and multiple myeloma: Systematic review and meta-analysis. Leuk Lymphoma. 2009;50(5):764-72.
10. Dimopoulos MA, Moreau P, Terpos E, Mateos MV, Zweegman S, Cook G, et al. Multiple myeloma: EHA-ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2021;32(3):309-22.
11. Perez EE, Orange JS, Bonilla F, Chinen J, Chinn IK, Dorsey M, et al. Update on the use of immunoglobulin in human disease: A review of evidence. J Allergy Clin Immunol. 2017;139(3):S1-46.
12. Goudouris ES, Silva AMR, Ouricuri AL, Grumach AS, Condino-Neto A, Costa-Carvalho BT, et al. II Consenso Brasileiro sobre o uso de imunoglobulina humana em pacientes com imunodeficiências primárias. Einstein. 2017;15(1):1-16.
13. Na IK, Buckland M, Agostini C, Edgar JDM, Friman V, Michallet M, et al. Current clinical practice and challenges in the management of secondary immunodeficiency in hematological malignancies. Eur J Haematol. 2019;102(6):447-56.
14. Jolles S, Chapel H, Litzman J. When to initiate immunoglobulin replacement therapy (IGRT) in antibody deficiency: a practical approach. Clin Exp Immunol. 2017 Jun;188(3):333-41.
15. Shapiro RS, Borte M. 7th International Immunoglobulin Conference: Immunoglobulin in Clinical Practice. Clin Exp Immunol. 2014;178(1):65-6.
16. Ludwig H, Zojer N. Supportive care in multiple myeloma. Best Pract Res Clin Haematol. 2007;20(4):817-35.
17. Wagner MB. Medindo a ocorrência da doença: prevalência ou incidência? J pediatr (Rio J). 1998;74(2):157-62.
18. Smith A, Wisloff F, Samson D. Guidelines on the diagnosis and management of multiple myeloma. British Journal of Haematology. 2005;132(4):410-51.



