Número Atual: Julho-Setembro 2020 - Volume 4 - Número 3
- Imprimir
- Indicar
- Estatísticas
- (0)
Comentários - Como Citar
- Download da Citação
- Artigos Relacionados
-
Outros dos
Autores
ARTIGO ESPECIAL
Guia prático de aerossolterapia na criança e no adolescente: documento conjunto da associação brasileira de alergia e imunologia e sociedade brasileira de pediatria
Practical guide to aerosol therapy in children and adolescents: joint document from the brazilian association of allergy and immunology and the brazilian society of pediatrics
Débora Carla Chong-Silva1; Antonio Carlos Pastorino2,3; Maria de Fátima Bazhuni Pombo Sant Anna1; Gustavo F. Wandalsen2,3; Herberto Jose Chong-Neto2,3; Regina Terse-Ramos1; Nelson Augusto Rosário Filho3; Luciana Rodrigues Silva4; Flavio Sano3; Dirceu Solé3,5
DOI: 10.5935/2526-5393.20200044
1. Departamento Científico de Pneumologia - Sociedade Brasileira de Pediatria
2. Departamento Científico de Alergia - Sociedade Brasileira de Pediatria
3. Associação Brasileira de Alergia e Imunologia
4. Sociedade Brasileira de Pediatria
5. Coordenador dos Departamentos Científicos - Sociedade Brasileira de Pediatria
Endereço para correspondência:
Dirceu Solé
E-mail: dirceu.sole@unifesp.br
Submetido em: 15/06/2020
Aceito em: 22/06/2020
Não foram declarados conflitos de interesse associados à publicação deste artigo
RESUMO
A via inalatória é a mais adequada para o tratamento das doenças respiratórias. Muitos fatores influenciam na deposição pulmonar do fármaco inalado, e, consequentemente, no sucesso terapêutico, desde fatores relacionados ao indivíduo, como questões anatômicas das vias aéreas, dinâmica respiratória, doença de base e técnica correta, até situações relacionadas às questões aerodinâmicas das partículas que compõem o aerossol, como o tamanho (diâmetro aerodinâmico mediano de massa) e a homogeneidade das partículas (desvio padrão geométrico). Nos últimos anos os dispositivos inalatórios se aperfeiçoaram, buscando atender às características necessárias que garantam uma deposição pulmonar satisfatória dos fármacos. A escolha do dispositivo inalatório deve ser individualizada, e o conhecimento das particularidades de cada dispositivo e das vantagens e desvantagens instrumentaliza o profissional na decisão, e impacta diretamente no sucesso terapêutico da medicação utilizada.
Descritores: Via inalatória, deposição pulmonar, aerossol, dispositivos inalatórios.
POR QUE UTILIZAR A VIA INALATÓRIA?
O racional
A via inalatória é a mais adequada para o tratamento das doenças respiratórias, especialmente quando comparada às demais vias de administração de fármacos, como a via enteral e parenteral1.
O racional para a escolha da via inalatória na administração de medicações é esta via combinar o menor risco e o maior benefício1,2.
A ação direta sobre a mucosa respiratória possibilita o efeito mais rápido dos fármacos em quantidades menores o que leva a baixas concentrações séricas e, com isso, menos efeitos adversos. A exemplo, o início rápido de ação dos broncodilatadores e a menor frequência de efeitos adversos dos corticosteroides, quando comparados ao seu uso enteral e parenteral3,4.
A relação risco-benefício dos fármacos administrados por aerossóis é determinada pelo índice terapêutico, ou seja, pela razão entre o efeito farmacológico desejável versus efeito sistêmico indesejável. O fármaco inalado ideal deve apresentar índice terapêutico elevado, absorção pulmonar baixa, biodisponibilidade oral baixa e clearance sistêmico elevado5. A biodisponibilidade do fármaco e o seu índice terapêutico podem ser influenciados pelas características do dispositivo gerador, pelas propriedades do fármaco veiculado, e pela técnica inalatória5.
A asma e a doença pulmonar obstrutiva crônica (DPOC) foram as primeiras doenças tratadas pela via inalatória. Até hoje são as principais condições que motivam a pesquisa e o desenvolvimento de novos dispositivos inalatórios1,2.
FATORES QUE INFLUENCIAM A DEPOSIÇÃO NA VIA INALATÓRIA
Para que os fármacos escolhidos apresentem o efeito terapêutico desejado é necessário que haja deposição pulmonar adequada e suficiente nas vias respiratórias mais periféricas6,7.
São muitos os fatores que influenciam essa deposição, desde fatores relacionados ao indivíduo, como questões anatômicas das vias aéreas, a dinâmica respiratória, a doença de base e o uso correto dos dispositivos, até situações relacionadas às questões aerodinâmicas das partículas que compõem o aerossol6,7.
a) Aspectos relacionados ao indivíduo
Os princípios físicos da deposição da medicação inalatória são semelhantes nos seres humanos de qualquer idade, porém características da fisiologia respiratória de cada faixa etária, bem como níveis cognitivos, levando ao entendimento e colaboração adequados, variam entre lactentes, pré-escolares, escolares, adultos e idosos8.
Uma proporção significante de partículas do medicamento inalado passa pela parte superior e central das vias aéreas e vai se depositar nos pulmões antes de ser exalada, sendo as pequenas partículas as mais propensas a atingir vias aéreas periféricas8,9.
Mecânica respiratória na criança
As crianças têm a distribuição do aerossol influenciada por características próprias, como a idade e a anatomia das vias aéreas, cujo diâmetro é menor do que no adulto. O diâmetro reduzido das vias aéreas aumenta a deposição na via aérea central, ocasionado pelo alto impacto das partículas nessa região. Ainda nesta faixa etária o fluxo inspiratório é menor, o que tende a reduzir a possibilidade de impactação8.
Quando se trata de lactentes, a fisiologia respiratória é caracterizada por alta velocidade e fluxo aéreo, que se torna turbulento, acarretando aumento da deposição de partículas nas regiões proximais8,10. Ainda a taquipneia, própria da idade, pode diminuir o tempo de permanência da partícula no pulmão e a sua deposição8,10.
A predominância do padrão respiratório nasal também prejudica a deposição da medicação nas vias mais distais. Como o nariz é um filtro muito eficiente, a maior parte do aerossol inalado pelos lactentes e crianças jovens não chega aos pulmões. Partículas maiores que 10 µm são, na sua maioria, retidas com o padrão de respiração nasal, apenas as pequenas partículas estão propensas a vencer a passagem nasal e se depositarem em vias aéreas mais distais, quando comparadas às partículas maiores10,11. Verificou-se que aerossóis inspirados por via nasal apresentam deposição pulmonar me-nor nos lactentes em comparação às crianças mais velhas. Os lactentes apresentam a capacidade vital e residual menores e os ciclos respiratórios mais curtos, quando comparados aos adultos11.
O choro, comum em crianças submetidas à terapia inalatória, acarreta o aumento e a irregularidade da frequência respiratória, com aumento do fluxo inspiratório em cerca de seis a sete vezes. Estudos já comprovaram que apenas uma fração da medicação inalatória é depositada nos pulmões quando a criança chora, acarretando drástico decréscimo do potencial terapêutico dos fármacos10,11. Durante o sono, a redução da capacidade residual funcional e variações na relação ventilação/perfusão também acarretam menor deposição das partículas inaladas12,13.
Outros fatores como a cooperação, a cognição e o desenvolvimento emocional influenciam a eficácia da terapia inalatória. Sem o entendimento adequado torna-se inviável o uso de bocais sendo a máscara facial uma opção utilizada, uma vez que propicia o uso passivamente, devendo-se estar atento ao encaixe no rosto, para que não haja escape e que não abranja os olhos10-12.
Idosos e doenças pulmonares crônicas
Indivíduos idosos também apresentam redução de capacidade cognitiva e têm maior dificuldade para o uso de dispositivos inalatórios que dependam da colaboração e coordenação13.
Pacientes com doenças obstrutivas graves têm a deposição reduzida dos fármacos administrados por via inalatória, devido ao comprometimento substancial da fisiologia respiratória, com redução da capacidade vital13.
Doenças associadas, como baixa acuidade visual ou déficits cognitivo-motores, podem dificultar o uso de dispositivos que necessitam de disparo manual ou preparo de doses10,13.
De maneira geral, inspirações rápidas propiciam a deposição por impacto na orofaringe e nas vias aéreas de grande calibre, tanto maior quanto maior o volume inalado. Por outro lado, a inalação lenta e profunda, com pausa inspiratória final de 5 a 10 segundos é apontada como facilitadora da deposição intrabrônquica. Vale lembrar que a inalação pela boca deve ser sempre preferida à inalação nasal, uma vez que esta reduz em até 50% a quantidade de fármaco que atinge os pulmões5-7,10,11.
b) Aspectos relacionados à dinâmica de deposição de partículas
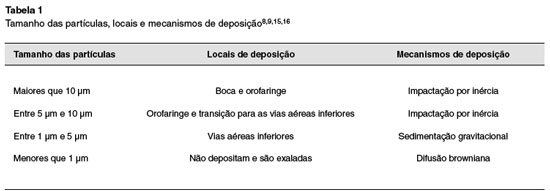
A deposição de partículas no pulmão pode ocorrer por diferentes mecanismos influenciados especialmente pela propriedade das partículas geradas (diâmetro aerodinâmico mediano de massa - DAMM), pelo fluxo aéreo (alto ou baixo) e pelo calibre da via aérea. São eles, deposição por impactação, sedimentação, intercepção ou difusão8,9 (Figura 1).
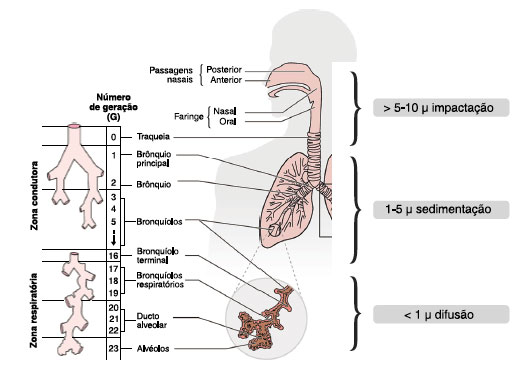
Figura 1
Representação gráfica das vias aéreas e dos mecanismos de deposição de partículas conforme o diâmetro aerodinâmico mediano de massa (DAMM)
Modificado de Kleistreureuer et al.14
A impactação das partículas por inércia, ocorre especialmente no caso de partículas de grande tamanho, maiores que 5 µm, que impactam na orofaringe e na bifurcação das vias aéreas, principalmente quando das mudanças no fluxo de ar8,9.
No caso da sedimentação gravitacional, a deposição ocorre quando a força gravitacional supera a força do fluxo de ar. O assentamento de partículas ocorre durante a sustentação da respiração. Esse mecanismo ocorre com partículas de 1 a 5 µm de tamanho. Partículas de natureza higroscópica podem aumentar de tamanho à medida que passam por correntes de ar e outros sedimentos8,9.
A intercepção de partículas ocorre devido ao tamanho físico ou forma das partículas (ex.: sílica e amianto), sendo comum ocorrer este tipo de deposição em pequenas vias aéreas8,9.
A difusão browniana ocorre no caso de partículas menores que 0,5 µm de diâmetro, onde estas partículas são inaladas e logo em seguida exaladas. Habitualmente, a difusão ocorre quando há baixo fluxo de ar e o movimento browniano ocorre no princípio da difusão8,9.
Tamanho das partículas
O diâmetro de cada partícula liberada pelo dispositivo influencia diretamente as propriedades aerodinâmicas desse aerossol, e é um fator determinante na deposição do fármaco ao longo das vias aéreas. A medida fundamental para o cálculo da eficiência da inalação é o diâmetro aerodinâmico médio de massa (DAMM).
O DAMM de um aerossol nos fornece o tamanho médio das partículas que atingem as vias aéreas8,9,15,16.
Devido à variabilidade no tamanho das partículas de cada aerossol gerado pelos diferentes dispositivos, as partículas se dispersam e se depositam com graus variados ao longo das vias aéreas, conforme descrito na Tabela 1. O tamanho ideal de partícula necessário para uma entrega pulmonar eficiente é de 1 a 5 µm8,9,15,16 (Tabela 1).
Buscando obter o tamanho de partícula ideal, os métodos utilizados para a fabricação dessas particulas são micronização, secagem por pulverização, secagem por congelamento por pulverização (liofilização), cristalização por fluido supercrítico e método de emulsão dupla17-19.
OS DISPOSITIVOS INALATÓRIOS
A via inalatória é conhecida de médicos e pacientes, desde a Antiguidade, há mais de quatro mil anos, quando raízes e folhas de Datura sp., com efeito anticolinérgico, eram inaladas com fins medicinais. Esta via de administração consolidou-se para tratamento de doenças obstrutivas há aproximadamente 50 anos, com o aprimoramento dos nebulizadores há mais de um século, e o surgimento dos aerossóis dosimetrados (AD), em 195620.
Além dos AD, os inaladores de pó (IPO) desempenham um papel significativo no tratamento de doenças respiratórias. Foram criados na década de 1960, e em 1987 foi usado o primeiro dispositivo IPO multidose com budesonida20,21.
Os avanços continuaram ocorrendo na eficiência de administração de medicamentos por via inalatória, principalmente com o surgimento dos espaçadores, inaladores em pó (IPO) diferenciados e especialmente desde a substituição dos propelentes com a troca do clorofluorcarbonado (CFC) pelo hidrofluoralcano (HFA) (Tabela 2).
Hoje, vários dispositivos para liberação de partículas inaladas são produzidos e comercializados largamente, sempre em busca da partícula ideal com a melhor deposição20.
Aerossóis dosimetrados (AD)
São os dispositivos mais usados para terapia inalatória até hoje. Neste dispositivo o fármaco encontra-se misturado a propelente (HFA), surfactante e lubrificantes. A pressão no interior do dispositivo chega a ser quatro vezes maior do que a da atmosfera. Após o disparo do aerossol as partículas são liberadas com diâmetro elevado de aproximadamente 40 µm de diâmetro e com velocidade de 100 km/ hora. Com a evaporação do propelente as partículas adquirem diâmetro respirável (3-4 µm)22,23.
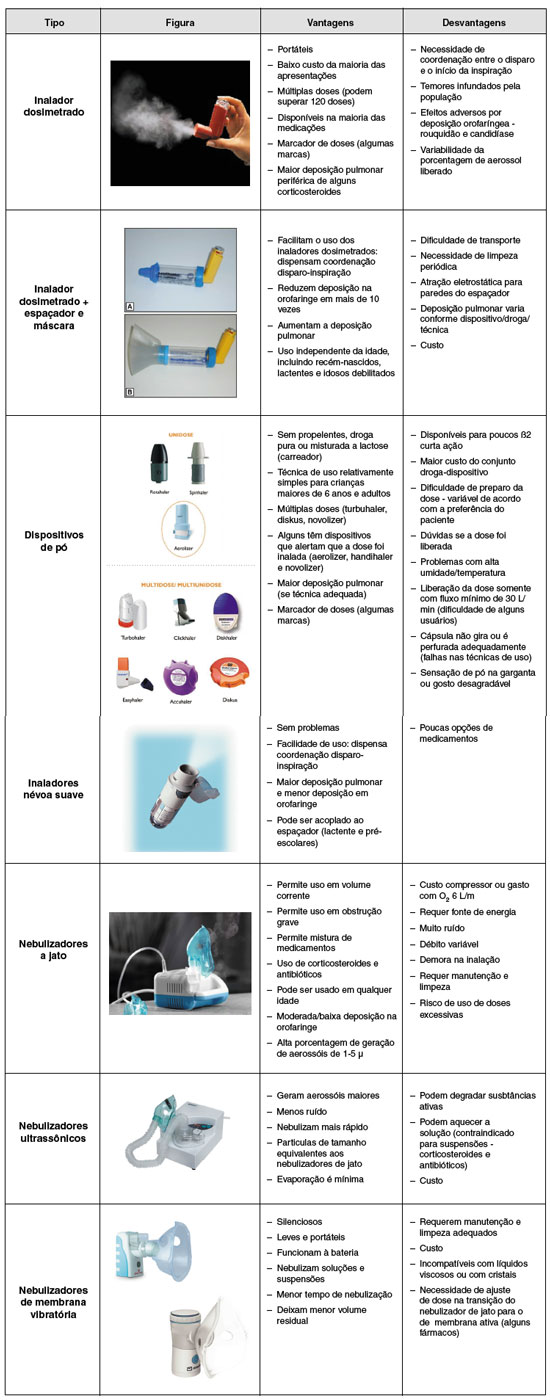
Uma das maiores vantagens deste dispositivo é a disponibilidade para uso de quase todos broncodilatadores e corticosteroides. Entre as desvantagens, está o fato de que seu uso adequado requer uma técnica coordenada. Para as crianças e pacientes com dificuldade de coordenação entre o disparo do aerossol e início da inspiração, o uso das aerocâmaras (espaçadores) se faz imprescindível22-24 (Figura 2).
Com o propelente HFA e com a otimização da técnica, especialmente com espaçadores, a deposição pulmonar aumenta consideravelmente, variando de 10% até 55% nas vias inferiores. A maior parte se deposita na orofaringe (pode chegar até 80%), uma parte permanece junto à válvula do dispositivo, e até 1% das partículas é exalada22,23.
Estudos comprovam que mais da metade dos adultos não utilizam os AD por técnica adequada, cometendo erros graves que comprometem consideravelmente a deposição pulmonar. Não agitar o dispositivo (perda de 36% da dose de aerossol), inspirar pelo nariz, inspirar após acionamento, não inspirar profundamente e não fazer pausa pósinspiratória são os erros mais citados22,23.
Espaçadores
Os espaçadores são acessórios criados para facilitar o uso dos AD, e otimizar a deposição pulmonar dos fármacos utilizados22-24.
Os espaçadores comerciais variam em formato, material, volume, durabilidade, presença de sinalizadores de fluxo (apito) e presença de válvula. Espaçadores de grande volume (500 a 800 mL), valvulados, facilitam a técnica de uso dos AD por eliminar a necessidade de coordenação entre o disparo e a inspiração, o mesmo se percebe com espaçadores de menor volume (200 a 300 mL), que têm sido igualmente eficientes e práticos, muito apropriados para crianças, as quais não precisariam respirar muitas vezes para vencer todo o volume do medicamento que está na câmara23,24.
A associação de máscara aos espaçadores é a opção adequada para o uso dos AD em lactentes e crianças pequenas, idosos e pacientes com déficit cognitivo. Tubos extensores de pequeno volume são úteis, porém menos eficientes do que os espaça dores valvulados de maior volume, não têm técnica padronizada de uso e não dispensam a coordenação entre o disparo e inspiração23,24.
As principais indicações para o uso de espaçadores são: pacientes sem o entendimento para utilizar os IPO e sem a coordenação suficiente para utilizar os AD, o que ocorre especialmente com crianças pequenas e idosos; pacientes que referem tosse ao utilizar os AD, fato comumente visto em pacientes com as vias aéreas hipersensíveis. Os espaçadores são escolha também para o uso de broncodilatadores durante a crise de asma ou exacerbação da DPOC em pronto-socorro e durante hospitalização23.
Diversos modelos de espaçadores e máscaras faciais foram idealizados por pesquisadores para adaptação adequada à face da criança, volumes compatíveis com a capacidade respiratória e melhora da eficiência na deposição das partículas.
Nesta linha, máscaras de material macio e alguns deles até com local para adaptação de chupetas, como é o caso da SootherMask® ou InspiraMask® se mostram interessantes por manterem as crianças tranquilas durante a administração do aerossol, lembrando que podem ter a desvantagem de favorecer a respiração exclusivamente nasal25.
A prática de utilizar detergentes durante a higienização dos espaçadores tem se tornado rotina nas recomendações dos especialistas após estudos que mostraram que o revestimento interno das aerocâmaras com detergente impactou, de forma positiva, a deposição pulmonar dos fármacos, em crianças de diferentes idades. O detergente reduziria a carga eletrostática nas paredes do espaçador e com isso disponibilizaria maior quantidade do fármaco para a inalação, deposição e melhores resultados terapêuticos24,26.
Inaladores de pó (IPO)
Os IPO apresentam boa relação de custobenefício em relação aos demais dispositivos inalatórios, e, apesar de necessitar colaboração e entendimento do paciente para sua execução, não exigem a coordenação do disparo com a inspiração, fato que facilita a técnica e justifica a escolha para os pacientes adultos. Nos modelos de IPO atualmente mais utilizados, o aerossol é gerado e disparado pela inspiração do paciente. O medicamento não necessita de propelentes para ser inalado, e está disponível puro ou misturado a carreadores, como lactose27,28. Neste caso, devemos ter especial atenção aos pacientes com história de anafilaxia ao leite de vaca, pela possível contaminação das partículas de lactose com proteína do leite de vaca.
Para inalar a dose do aerossol é necessário que o paciente gere um fluxo inspiratório mínimo de 20 a 30 L/min, dependendo do dispositivo, por isso o uso por crianças pequenas e idosos é difícil27,28.
Desde que foi criado, a cada ano, novos dispositivos IPO chegam ao mercado, utilizando tecnologias capazes de aumentar a deposição pulmonar de fármacos. Estudos confirmam diferenças na deposição pulmonar dos diversos IPO, variando em média de 10 a 30%27,28.
As vantagens de utilizar um IPO são a não necessidade de propelente; técnica relativamente simples para adultos; dispositivos multidoses; muitos sinalizam que a dose foi realmente inalada; maior deposição pulmonar se a técnica estiver correta; marcadores do número de doses; e alguns exigem fluxo inspiratório mínimo, podendo ser utilizado em pacientes graves. Além disso, são dispositivos compactos e de fácil portabilidade27,28. No Brasil, os IPO mais largamente comercializados são: turbuhaler, aerolizer, diskus, pulvinal, handihaler, elipta, entre outros (Figura 2).
O desempenho do IPO depende fundamentalmente do seu desenho, resistência ao fluxo e da capacidade do paciente em gerar e manter alto fluxo inspiratório27,28.
Orientações simples, como guardar o dispositivo em ambiente com pouca umidade, bem como orientar o usuário a não exalar dentro do dispositivo, são importantes, buscando evitar o acúmulo de umidade no sistema e possibilitando que o pó, seco, seja melhor disponibilizado no acionamento27,28.
Nebulizadores
Mesmo diante da facilidade de uso dos AD e das inovações dos IPO, os nebulizadores ainda ocupam espaço considerável no receituário de pediatras e especialistas.
Seu uso justifica-se pelo fato de alguns medicamentos estarem disponíveis somente na forma de solução, pela facilidade técnica em qualquer idade, por depender o mínimo da colaboração do paciente, e a constatação, na prática clínica, de que o uso do nebulizador faz parte da cultura da nossa população29-31 (Figura 2).
As vantagens apontadas para o seu uso são: a possibilidade de nebulizar mistura de medicamentos e a possibilidade de inalação mesmo com respiração em volume corrente, o que facilita o uso em qualquer idade, e permite o uso durante exacerbações das doenças obstrutivas graves29,30. Outro ponto importante é o fato dos nebulizadores possibilitarem a administração concomitante de oxigênio em casos de hipoxemia (Figura 2).
Os nebulizadores convencionais têm grande perda de medicamento devido ao seu débito constante durante a inspiração e a expiração. O mecanismo de formação do aerossol se dá pela passagem do ar ou oxigênio através de um pequeno orifício (Venturi) e, ao alcançar o recipiente contendo o fármaco, o gás se expande, havendo queda brusca de sua pressão e grande aumento de sua velocidade. Diante disso, o líquido do reservatório é sugado, e assim são gerados aerossóis. As partículas maiores do aerossol são retidas em anteparos (parede do reservatório, entre outros) e se juntam ao restante do líquido, para serem renebulizadas, e as menores são inaladas29,30.
Nebulizadores pneumáticos ou a jato (NJ)
São os nebulizadores mais populares e os primeiros a serem desenvolvidos. O fluxo recomendado para que os nebulizadores pneumáticos produzam partículas com DAMM < 5 µm é de 6 a 8 L/min, sendo recomendado volume de 4 a 5 mL de solução a ser nebulizada. Apesar de recomendado um tempo máximo de nebulização de 10 a 15 minutos (10 minutos para criança), quando o NJ funciona adequadamente, 80% da solução é nebulizada em 5 minutos, não se justificando prolongar o processo29,30 (Figura 3).
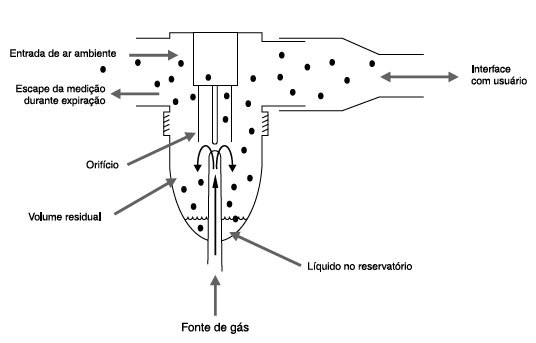
Figura 3
Desenho esquemático do funcionamento dos nebulizadores a jato de ar
Adaptado de Hess D.30
Os nebulizadores pneumáticos permitem nebulizar soluções (como soro fisiológico e salbutamol) ou suspensões (mistura de sólidos em líquidos, como corticosteroides e antibióticos), recomendando-se sempre que a respiração seja feita pela boca durante a nebulização29,30.
Os principais determinantes de eficácia dos nebulizadores a jato são: débito adequado e constante do aerossol, fluxo adequado de oxigênio/ar utilizado, quantidade pequena do volume residual (líquido perdido para as paredes do reservatório de nebulização em geral 0,6 a 1 mL), padrão da respiração (nasal reduz em 50% da deposição pulmonar, respiração muito rápida e com fluxo turbilhonado aumenta a impactação em vias aéreas superiores), propriedades da solução/suspensão: concentração, viscosidade, tensão superficial e temperatura, carga eletrostática do recepiente de nebulização e condições ambientais29,30.
Sistemas inteligentes, que otimizam e controlam o fornecimento do aerossol baseado em dados individuais, a chamada inalação controlada indivi-dualizada (ICI), ocorre por meio de pressão de ar positiva fornecida por compressor controlado por computador, programado com base nos dados individuais da função pulmonar do paciente. Estudos realizados com a marca AKITA JET® mostraram melhor desempenho na deposição de medicamentos. Além destes dispositivos utilizarem bocais, sem possibilidade de acoplar máscaras, exigem uma mínima colaboração do usuário, o que limita o uso em lactentes e pré-escolares32.
Nebulizadores ultrassônicos (NU)
Os nebulizadores ultrassônicos têm como princípio a energia gerada por vibrações rápidas de um cristal de quartzo (piezoelétrico), transmitida à superfície da solução do fármaco. O processo gera gotículas que são liberadas da superfície da lâmina do líquido na forma de aerossóis33 (Figura 4).
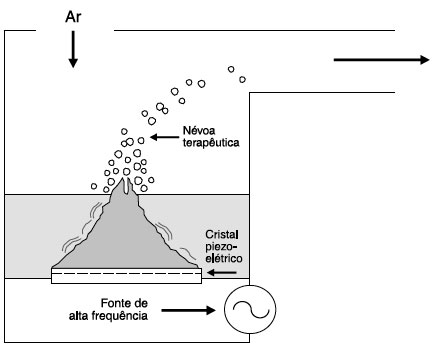
Figura 4
Desenho esquemático do funcionamento dos nebulizadores ultrassônicos
Adaptado de Hess D.30
Estes equipamentos usualmente geram aerossóis maiores, fazem menos ruído e nebulizam mais rápido33.
A frequência das ondas ultrassônicas determina o tamanho das partículas do aerossol. O fluxo gerado pelo nebulizador ultrassônico é superior aos dos nebulizadores a jato, e por isso estão indicados para maiores volumes. É importante reforçar que os nebulizadores ultrassônicos estão indicados apenas para nebulizar soluções e não suspensões, ou seja, apropriados para nebulizar broncodilatadores, mas contraindicados para nebulizar corticosteroides, antibióticos, como a budesonida, ou outros fármacos que possam sofrer inativação por aquecimento33.
Nebulizadores com tecnologia da membrana vibratória
Os nebulizadores que utilizam a tecnologia da membrana vibratória ou oscilatória representam a novidade neste grupo de equipamentos. São nebulizadores eletrônicos que contêm uma membrana microperfurada no topo do reservatório de líquido. No caso dos nebulizadores de membrana vibratória, a oscilação dessa membrana gera um gradiente de pressão que permite a passagem da solução através das microperfurações, gerando o aerossol31,34 (Figura 5).
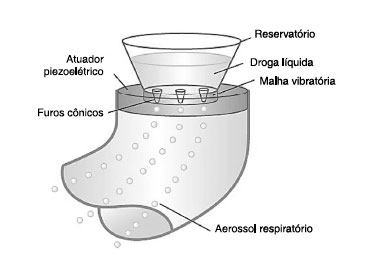
Figura 5
Desenho esquemático do funcionamento dos nebulizadores de membrana vibratória
Adaptado de Vecellio L.36
Os nebulizadores de membrana vibratória apresentam vantagens quando comparados aos nebulizadores de jato, pois são considerados mais silenciosos, mais leves (excelente portabilidade), não necessitam de fonte de oxigênio ou ar comprimido e funcionam também à bateria e em diferentes posições do paciente. Quando comparados aos nebulizadores ultrassônicos, estes novos equipamentos permitem a nebulização de soluções e também de suspensões. Ainda, funcionalmente, apresentam tempo de nebulização mais curto, e deixam menor volume residual31,34,35.
Os nebulizadores de membrana representam um avanço tecnológico em um campo com poucas mudanças nas últimas décadas. Suas características, tanto na geração de partículas quanto na portabilidade, representam maior eficácia e eficiência que os nebulizadores convencionais31,34,35.
QUAL DISPOSITIVO DEVO INDICAR PARA MEU PACIENTE?
A escolha do dispositivo inalatório deve ser individualizada e levando em conta as recomendações existentes, assim como as vantagens e desvantagens de cada dispositivo. A decisão deve ser discutida e compartilhada com o paciente e/ou os familiares. Algumas questões, listadas abaixo, podem auxiliar na escolha37.
- Quais dispositivos são disponíveis e apropriados para a medicação desejada?
- O dispositivo pensado é adequado para a idade e condições do paciente?
- Qual será o custo para o paciente/família?
- A medicação e o dispositivo são aprovados pelos órgãos regulatórios?
- O dispositivo pensado é capaz de ser utilizado para outras medicações que o paciente necessite?
- Qual dispositivo é mais conveniente, portátil e econômico para o paciente?
- Qual é a preferência do paciente e/ou da família?
O pediatra e o clínico têm papel fundamental na orientação da escolha e da técnica de uso dos dispositivos inalatórios para seus pequenos pacientes.
O conhecimento das particularidades de cada dispositivo na geração do aerossol, bem como das vantagens e desvantagens, instrumentaliza o profissional na decisão e impacta diretamente no sucesso terapêutico da medicação inalatória utilizada.
REFERÊNCIAS
1. Ravichandiran V, Masilamani K, Satheshkumar S, Joseprakash D. Drug delivery to the lungs. Int J Pharm Sci Rev Res. 2011;10(2):85-9.
2. Aguiar R, Lopes A, Ornelas C, Ferreira R, Caiado J, Mendes A, et al. Terapêutica inalatória: Técnicas de inalação e dispositivos inalatórios. Rev Port Imunoalergologia. 2017;25(1):9-26.
3. Pereira LFF.Como administrar drogas por via inalatória.J Pneumol. 1998;24:133-43.
4. Ariyananda PL, Agnew JE, Clarke SW. Aerosol delivery systems for bronchial asthma. Posgrad Med J. 1996;72:151-56.
5. Witek TJ Jr. The fate of inhaled drugs: the pharmacokinetics and pharmacodynamics of drugs administered by aerosol.Respir Care. 2000;45(7):826-30.
6. Feenstra TL, Rutten-Van Mölken MP, Jager JC, Van Essen-Zandvliet LE. Cost effectiveness of guideline advice for children with asthma: a literature review. Pediatr Pulmonol. 2002;34(6):442-54.
7. Skoner DP. Balancing safety and efficacy in pediatric asthma management. Pediatrics. 2002;109(2 Suppl):381-92.
8. Pandey Shivanand, Sweta B, Binal P, Mahalaxmi R, Viral D, Jivani P. Local and Systemic Pulmonary Drug Delivery of Small Molecules. J Pharm Res. 2009;2(8):1200-2.
9. Mortonen T, Yang Y. Deposition mechanics of pharmaceutical particles in human airways. In: Hickey AJ, ed. Inhalation Aerosols: Physical and Biological Basis for Therapy. New York: Marcel Dekker;1996. p. 1-21.
10. Santos CIS, Rosa GJ, Shiratori AP, d'Aquino AG, Bueno, Okuro RT. Influência do choro e de padrões respiratórios na deposição de medicação inalatória em crianças. Rev Paul Pediatr. 2010;28(4):394-7.
11. Schüepp KG, Straub D, Möller A, Wildhaber JH. Deposition of aerosols in infants and children. J Aerosol Med. 2004;17:153-6.
12. Janssens HM, Tiddens HA. Aerosol therapy: the special needs of young children. Paediatr Respir Rev. 2006;7 (Suppl 1):S83-5.
13. Pauwels R, Newman S, Borgstrom L.Airway deposition and airway effects of antiasthma drugs delivered from metered-dose inhalers. Eur Respir J. 1997;10:2127-38.
14. Kleinstreuer C, Zhang Z, Donohue JF. Targeted drug-aerosol delivery in the human respiratory system. Annu Rev Biomed Eng. 2008;10:195-220.
15. O'Callagan C, Barry PW. The science of nebulized drug delivery. Thorax. 1997;52(2):S31-S34.
16. Eixarch H, Haltner-Ukomadu E, Beisswenger C, Bock U. Drug delivery to the lung:permeability and physicochemical characteristics of drugs as the basis for a pulmonary biopharmaceutical classification system (pBCS). J Epith Biol Pharmacol. 2010;3(9):1-14.
17. Threlfall T. Crystallization of polymorphs: Thermodynamic insight into the role of solvent. Org Proc Res Dev. 2000;4(5):384-90.
18. Rabbani NR, Seville PC.The influence of formulation components on the aerosolisation properties of spray-dried powders. J Contr Release. 2005;110(1):130-40.
19. Mansour HM, Rhee Y, Wu X. Nanomedicine in pulmonary delivery. Int J Nanomed. 2009;4:299-319.
20. Stein SW, Thiel CG. The History of Therapeutic Aerosols: a chronological review. J Aerossol Med Pulm Drug Deliv. 2017;30(1):20-40.
21. Cochrane M, Bala MV, Downs KE, Mauskopf J, Ben-Joseph RH. Inhaled corticosteroids for asthma therapy. Chest. 2000;117:542-50.
22. Newman SP. Metered dose pressurized aerosols and the ozone layer. Eur Resp J. 1990;3(10):495-7.
23. Ram FS.Clinical efficacy of inhaler devices containing beta 2 agonist bronchodilators in the treatment of asthma: cochrane systematic review and meta-analysis of more than 100 randomized, controlled trials. Am J Respir Med. 2003;2:349-65.
24. Abreu S, Silva L, Teixeira S, Marques R, Ramalhete N, Antunes H. Avaliação do desempenho de três câmaras de expansão. Acta Med Port. 2012;25:4-9.
25. Amirav I, Newhouse MT, Luder A, Halamish A, Omar H, Gorenberg M.Feasibility of aerosol drug delivery to sleeping infants: a prospective observational study. BMJ Open. 2014;4:e004124.
26. Wildhaber JH, Janssens HM, Piérart F, Dore ND, Devadason SG, LeSouëf PN. High-percentage lung delivery in children from detergent-treated spacers. Pediatr Pulmonol. 2000;29:389-93.
27. ones BE. A history of DPI capsule filling. Inhalation. 2009;3(3):20-3.
28. Haidl P, Heindl S, Siemon K, Bernacka M, Cloes RM. Inhalation device requirements for patients' inhalation maneuvers.Resp Med. 2016;118:65-75.
29. McCallion ONM, Taylor KMG, Bridges PA, Thomas M, Taylor AJ.Jet nebulizers for pulmonary delivery. Int J Pharm. 1996;130:1-11.
30. Hess DR. Aerossol delivery devices in the treatment of asthma. Respir Care. 2008;54:699-725.
31. Hess DR. Nebulizers: principles and performance. Respir Care. 2000;45(6):609-22.
32. Fischer A, Stegemann J, Scheuch G, Siekmeier R. Novel devices for individualized controlled inhalation can optimize aerosol therapy in efficacy, patient care and power of clinical trials. Eur J Med Res. 2009;14(Sup.4):71-7.
33. Ari A.Jet, ultrasonic, and mesh nebulizers:an evaluation of nebulizers for better clinical outcomes. Euras J Pulmonol. 2014;16:1-7.
34. Lass JS, Sant A, Knoch M. New advances in aerosolised drug delivery: vibrating membrane nebuliser technology. Expert Opin Drug Deliv. 2006 Sep;3(5):693-702.
35. Ehrmann S.Vibrating mesh nebulisers - can greater drug delivery to the airways and lungs improve respiratory outcomes? Eur Resp Pulm Dis. 2018;4(1):33-43.
36. Vecellio L. The mesh nebuliser: a recent technical innovation for aerosol delivery. Breathe. 2006;2(3):253-60.
37. Geller D.Comparing clinical features of the nebulizer, metered-dose inhaler, and dry powder inhaler. Respir Care. 2005;50:1313-21.