Número Atual: Julho-Agosto 2014 - Volume 2 - Número 4
- Imprimir
- Indicar
- Estatísticas
- (0)
Comentários - Como Citar
- Download da Citação
- Artigos Relacionados
-
Outros dos
Autores
Artigo Original
Eficácia da terapia Anti-IgE no controle da asma
Effectiveness of anti-IgE therapy for asthma control
Faradiba Sarquis Serpa1; Mariana Pandolfi Piana2; Firmino Braga Neto2; Fernanda Lugao Campinhos2,3; Marina Gaburro da Silveira2; Joseane Chiabai4; Eliana Zandonade5
1. MD, MSc. Escola Superior de Ciências da Santa Casa de Misericórdia de Vitória, Vitória, ES
2. MD. Escola Superior de Ciências da Santa Casa de Misericórdia de Vitória, Vitória, ES
3. MD. Faculdade Brasileira-MULTIVIX, Vitória, ES
4. MD, MSc. Universidade Federal do Espírito Santo, Vitória, ES
5. PhD. Universidade Federal do Espírito Santo, Vitória, ES
Endereço para correspondência:
Faradiba Saquis Serpa
E-mail: faradibasarquis@uol.com.br
Submetido em: 22/03/2015
Aceito em: 10/04/2015
Nao foram declarados conflitos de interesse associados à publicaçao deste artigo.
RESUMO
OBJETIVO: Avaliar parâmetros de resposta à terapia anti-IgE com omalizumabe em pacientes com asma de difícil controle.
MÉTODOS: Foram avaliados 24 pacientes com asma de difícil controle, em uso de omalizumabe há pelo menos 32 semanas e considerados como respondedores à terapia. Avaliou-se a pontuaçao do teste de controle de asma (TCA), a presença de sintomas de asma, a frequência de uso de ß2-agonista de curta açao, as doses de corticoide inalatório e oral e o percentual previsto do volume expiratório forçado no 1º minuto (VEF1), antes e com 16 e 32 semanas de tratamento.
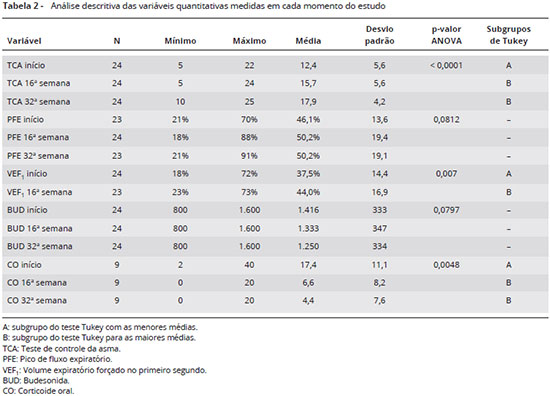
RESULTADOS: Na avaliaçao da pontuaçao do TCA foram obtidas as médias 12,4 para o momento inicial, 15,7 e 17,9 para a 16ª semana e 32ª semana respectivamente (p < 0,0001). A dose média de corticoide inalatório diminuiu ao longo das 32 semanas, de 1.416 mcg para 1.250 mcg na 32ª semana (p = 0,0797). O número de idas à emergência e de sintomas noturnos também diminuíram. Observou-se reduçao da dose de corticoide oral, sendo inicialmente a dose média de 17,4 mg e após 16 e 32 semanas 6,7 mg e 4,4 mg, respectivamente (p < 0,0001). Houve aumento na média do VEF1(% do previsto), de 37,5% no início do tratamento para 44,0% na 16ª semana (p = 0,007).
CONCLUSOES: O omalizumabe como terapia adjuvante no tratamento de pacientes com asma de difícil controle foi eficaz na melhora de parâmetros clínicos e funcionais, contribuindo para o controle da asma e diminuiçao dos riscos futuros.
Descritores: Omalizumabe, anti-IgE, asma grave, eficácia.
INTRODUÇAO
O uso da terapia anti-IgE na asma se consolidou nos últimos anos como uma opçao terapêutica para o tratamento de pacientes com asma de difícil controle (ADC). O primeiro agente biológico com esta propriedade, o omalizumabe, é um anticorpo monoclonal humanizado (IgG) que liga-se seletivamente à cadeia pesada da IgE livre, impedindo sua ligaçao com o receptor de alta afinidade (FcεRI) em mastócitos e basófilos, interrompendo assim, a cascata inflamatória envolvida na patogênese da asma alérgica1.
Sao considerados candidatos à terapia com omalizumabe os pacientes que nao obtêm controle da doença na etapa 4 de tratamento da Global Initiative for Asthma (GINA), ou seja, que nao alcançam o controle com doses elevadas de corticosteroide inalatório (budesonida acima de 800 mcg/dia ou equivalente), associadas a ß2-agonista de longa açao, após serem descartadas causas de nao controle2-5.
Diversos estudos de vida real comprovam a eficácia do omalizumabe no tratamento da ADC, e os benefícios da terapia ocorrem, na maioria dos casos, até 16 semanas de tratamento5,6. Para avaliaçao da resposta ao tratamento, nao existe critério clínico e laboratorial específico. Recomenda-se o uso de parâmetros considerados marcadores indiretos da melhora da inflamaçao como o número de exacerbaçoes, o uso de medicaçao de resgate, limitaçao para atividades diárias, avaliaçao da funçao pulmonar e questionários validados para avaliar o controle da asma e a qualidade de vida2,3,7.
No Brasil, estudos de vida real para avaliar resposta ao uso de omalizumabe sao escassos. Assim, este estudo teve como objetivo avaliar parâmetros de resposta à terapia com omalizumabe em pacientes considerados como respondedores ao tratamento.
MÉTODOS
Estudo longitudinal e retrospectivo realizado no período de 30 de abril a 30 de agosto de 2014 no Centro de Referência em Asma do Hospital Santa Casa de Misericórdia de Vitória (HSCMV), ES. A populaçao do estudo foi composta por pacientes com diagnóstico de asma alérgica de difícil controle, em terapia com omalizumabe. Todos os 24 pacientes em tratamento há 32 ou mais semanas foram convidados a participar da pesquisa, mediante os esclarecimentos necessários e assinatura do Termo de Consentimento Livre e Esclarecido.
Os pacientes responderam a um questionário com questoes referentes à idade atual, sexo, idade de início da asma, história familiar de asma, tabagismo ativo ou passivo, presença de comorbidades (rinite alérgica, doença do refluxo gastroesofágico [DRGE], hipertensao arterial sistêmica [HAS], diabetes mellitus [DM]), uso de medicamentos, eventos adversos ao uso do omalizumabe, idas à emergência, limitaçao para atividades diárias, asma noturna e sintomas diurnos, antes e durante o tratamento.
Dados adicionais, clínicos e de exames complementares, antes e após 16 e 32 semanas do início do tratamento foram obtidos através de revisao dos prontuários médicos. Foram registrados o nível de IgE total, o resultado do teste cutâneo com aeroalérgenos, o índice de massa corpórea (IMC), o percentual previsto do volume expiratório forçado no 1º minuto (VEF1), o pico de fluxo expiratório (PFE), a pontuaçao do teste de controle de asma (TCA), a presença de sintomas de asma, frequência de uso de ß2-agonista de curta açao (ß2), a dose de corticoide inalatório (budesonida inalada - BUD) e a dose de corticoide oral (CO) dos três momentos, com exceçao do VEF1 que nao foi avaliado na 32ª semana. Foram levantados também relatos de eventos adversos ocorridos durante todo o período de tratamento.
Na avaliaçao do TCA considerou-se melhora no controle clínico da asma quando ocorreu um aumento de 2 ou mais pontos na pontuaçao final do teste que compreende cinco questoes, que avaliam sinais, sintomas e uso de medicaçao de resgate nas últimas quatro semanas8,9.
O projeto foi aprovado pelo Comitê de Ética em Pesquisa com Seres Humanos da Escola Superior de Ciências da Santa Casa de Misericórdia de Vitória (EMESCAM), sob o número 632.158.
Os dados obtidos foram alocados nos programas SPSS Statistics v20.0 e v10.0. Foi aplicado o teste ANOVA para medidas repetidas e, quando necessário, o teste Tukey HSD para comparaçao das médias entre os momentos. Os testes Kappa e McNemar, foram utilizados para verificar a concordância das respostas das variáveis qualitativas e se houve mudança significativa de opiniao entre os pacientes, respectivamente. Um valor de p inferior a 0,05 foi considerado significativo.
RESULTADOS
Características clínicas e demográficas
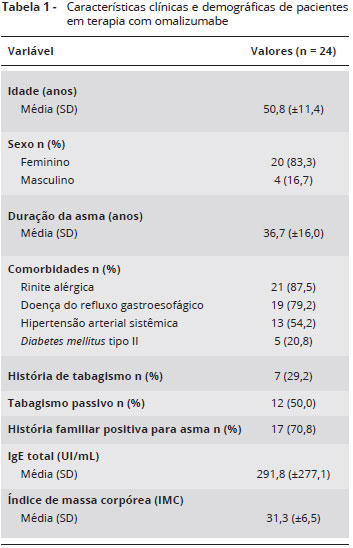
Foram avaliados 24 pacientes, 20 (83,3%) do sexo feminino e 4 (16,7%) do masculino. A idade variou de 34 a 72 anos (média: 50,8 ± 11,4 anos). O tempo de duraçao da asma variou de 6 a 65 anos (média: 36,7 ± 16,0). A dosagem de IgE sérica total prévia ao tratamento variou de 32 a 1.341 (média: 291,8 ± 277,1 UI/mL). Todos os pacientes apresentavam IgE específica ou teste cutâneo de hipersensibilidade imediata (prick test) positivo para pelo menos um aeroalérgeno. O IMC variou de 23,1 a 44,4 kg/m2 (média: 31,3 ± 6,5) e 18 pacientes foram considerados com sobrepeso ou obesos segundo a Organizaçao Mundial da Saúde10. Os dados clínicos e demográficos sao apresentados na Tabela 1.
Avaliaçao de parâmetros clínicos e funcionais relacionados ao controle da asma
A avaliaçao da pontuaçao do TCA revelou médias de 12,4 no momento inicial, 15,7 na 16ª semana e 17,9 na 32ª semana. Na 16ª semana, 14 pacientes (58,3%) aumentaram dois ou mais pontos acima do valor inicial, e na 32ª semana, 20 pacientes (83,3%) haviam aumentado a pontuaçao do TCA (Figura 1). Houve um aumento significante na média do TCA entre o início do tratamento e a 16ª semana (Tabela 2).
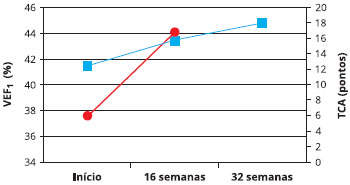
Figura 1 - Médias do teste de controle da asma (TCA) e do volume expiratório forçado no primeiro segundo (FEV1) nos três momentos avaliados
Foi observado também um aumento significante na média do VEF1 (% do predito) que era de 37,6% no início do tratamento, com aumento para 44% na 16ª semana (p = 0,007) (Figura 1). Nas medidas de PFE, observou-se um aumento nos valores absolutos ao longo do tempo, mas nao houve significância estatística entre as médias (Tabela 2).
A dose média de corticoide inalatório (em mcg de budesonida) diminuiu ao longo das 32 semanas, pois 10 (40%) pacientes conseguiram reduzir a dose do medicamento, mas esta reduçao nao foi estatisticamente significante (p = 0,0797) (Tabela 2, Figura 2).

Figura 2 - Médias das doses de budesonida e corticoide oral nos três momentos avaliados
Ao longo do período estudado, a maioria dos pacientes conseguiu suspender o uso de CO. Inicialmente a dose média (em mg de prednisona) foi de 174, e após 16 e 32 semanas 6,7 e 4,4, respectivamente (Figura 2). Entretanto, ao aplicar o teste Tukey, nao foi observada diferença entre médias em 16 e 32 semanas. Concluise entao que houve de fato uma reduçao significativa da dose de CO até a 16ª semana, e que a partir deste momento, a reduçao nao alcançou significância estatística (Tabela 2).
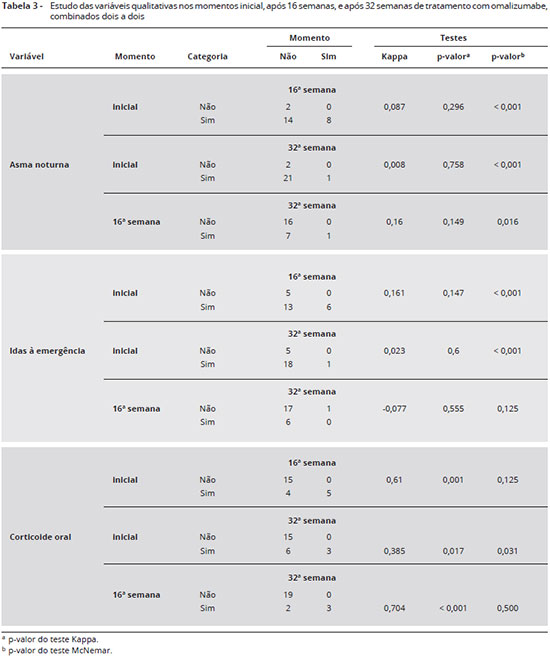
Na avaliaçao dos critérios clínicos de controle da asma, inicialmente 22 pacientes apresentavam asma noturna, na 16ª semana 8 mantiveram-se com o sintoma, e na 32ª semana, apenas 1 paciente persistiu com o sintoma. O mesmo ocorreu para a variável idas à emergência, no início 19 pacientes necessitavam ir à emergência durante as exacerbaçoes. Até a 16ª semana 6 foram à emergência, e na 32ª semana apenas 1 tinha essa necessidade. É importante ressaltar que a alteraçao no intervalo da 16ª para a 32ª semana nao apresentou significância estatística (p = 0,125), o que leva à interpretaçao de que a terapia anti-IgE foi eficaz na reduçao da necessidade de ida à emergência até a 16ª semana (Tabela 3).
Todos os pacientes referiram limitaçao para atividades diárias no início do tratamento. Na 16ª semana, 14 mantinham esta queixa, e na 32ª semana apenas 5 pacientes ainda apresentavam limitaçoes para atividades do cotidiano, indicando que um grupo de pacientes ainda pode alcançar benefícios clínicos ao longo do tratamento.
Quanto ao uso de ß2-agonista de curta açao, no início do tratamento todos os pacientes necessitavam usar mais de duas vezes por semana. Na 16ª semana 23 pacientes usavam, e na 32ª semana de tratamento 19 ainda usavam mais de duas vezes por semana, o que nao foi considerado significante (p = 0,125).
No início do tratamento, 9 pacientes necessitavam usar CO, na 16ª semana 5 pacientes mantinham o uso, e na 32ª apenas 3. Na comparaçao entre o momento inicial e final, houve uma diminuiçao estatisticamente significante do uso de CO, sugerindo que a terapia com o omalizumabe contribuiu para reduçao do número de pacientes que utilizam esta medicaçao ao longo das 32ª semanas (Tabela 3).
Segurança
Durante as 32 semanas de tratamento, 6 (25%) pacientes apresentaram algum tipo de evento adverso. O mais frequente foi reaçao no local da aplicaçao, caracterizada por dor, eritema e prurido, que ocorreu em 3 (12,5%) pacientes. Outros 3 pacientes apresentaram isoladamente: cefaleia, hipotensao e parestesia em dimídio esquerdo. Nenhuma das ocorrências impediu a continuidade do tratamento e nao se repetiu nas aplicaçoes subsequentes.
DISCUSSAO
Este estudo comprovou a segurança e a eficácia do omalizumabe em controlar limitaçoes atuais e reduzir os riscos futuros, quando prescrito como terapia adicional em pacientes com asma alérgica nao controlada, apesar do uso de corticoide inalatório em altas doses associado a ß2-agonista de longa duraçao. Parâmetros de reposta ao tratamento, tais como pontuaçao do TCA, funçao pulmonar, avaliaçao de sintomas e do uso de medicamentos como ß2-agonista de curta duraçao, uso de corticoide inalatório e sistêmico, mostraram-se úteis na avaliaçao dos pacientes considerados como respondedores ao tratamento, assim como em outros estudos de vida real5,6,8,11-15.
A média do TCA mostrou um aumento significante na 16ª semana de tratamento, mas alguns pacientes só alcançaram este aumento ao longo das 32 semanas, quando a maioria (83,3%) aumentou a pontuaçao, indicando que, conforme observado por Bousquet et al., podem ocorrer benefícios clínicos após as 16 primeiras semanas de tratamento para um grupo de pacientes considerados como respondedores tardios16. Em um estudo espanhol, também foi observado benefício clínico adicional no decorrer do tratamento, o que se traduziu por aumento significativo do TCA após a 16ª semana17.
Outro desfecho positivo observado durante o tratamento com o omalizumabe foi a melhora da funçao pulmonar com aumento do PFE e do VEF1 (% do previsto). O aumento da média do VEF1 em 17,2%, obtido na 16ª semana, foi maior que a de um estudo britânico (12,8%), e de um estudo multicêntrico no qual houve um aumento de 8,6%, no mesmo período11,16. Outros autores observaram aumento significante do VEF1 ao longo do tratamento apenas nos pacientes abaixo de 50 anos, possivelmente pela presença de obstruçao fixa de vias aéreas nos mais velhos17,18. Em nossa casuística a média de idade foi 50,8 anos, e observamos melhora do VEF1 na maioria dos pacientes com idade superior a 50 anos, indicando que mesmo neste grupo de pacientes também é possível melhorar a funçao pulmonar, assim como observado por Tzortzaky et al.19. Existem evidências de que os pacientes com 50 anos ou mais melhoram os desfechos clínicos tanto quanto os mais jovens, entretanto, apresentam uma taxa de abandono de tratamento maior18,20.
Na avaliaçao do uso de corticoide inalalatório, observamos uma reduçao da dose média ao longo das 32 semanas, sem alcançar significância estatística. Por outro lado, a reduçao do uso de corticoide sistêmico foi significante e maior do que a observada por outros autores. No presente estudo, 44,4% dos pacientes suspenderam o CO e a reduçao da dose média utilizada foi de 61,7% na 16ª semana de tratamento. Ao final de 32 semanas, apenas 3 pacientes ainda necessitavam fazer uso de CO, mesmo assim em doses mais baixas do que aquelas do início do tratamento. No estudo PERSIST5, também foi observada reduçao significativa apenas na dose do corticoide sistêmico e, em outro estudo de vida real, Molimard et al.21 observaram que 30,1% dos pacientes reduziram e 20,5% pararam de usar corticoide oral ao longo do tratamento. Resultados semelhantes foram encontrados em estudo do Reino Unido, onde 24,2% dos pacientes conseguiram suspender o corticoide oral, e a reduçao média na dose foi de 49%22.
O impacto da terapia anti IgE na reduçao do número de exacerbaçoes, visitas à emergência e hospitalizaçoes está bem estabelecido13,16,22-24. Em um estudo de 52 semanas os autores observaram que 58,7% dos pacientes diminuiram o número de visitas aos serviços de saúde em relaçao ao ano anterior após o inicio do tratamento com omalizumabe. Um estudo mexicano mostrou que 95,7% dos pacientes tiveram pelo menos uma consulta de emergência no ano anterior a terapia anti-IgE, e após 3 anos apenas 19,1% apresentaram necessidade de procurar emergência15. Em nossa casuística, houve uma reduçao significante no número de pacientes que procuraram a emergência até a 16ª semana, e na 32ª semana de tratamento apenas 4,2% dos pacientes necessitou desse tipo de atendimento.
Com a evoluçao favorável de todos os parâmetros utilizados para avaliar o controle da asma, era esperado melhora na qualidade de vida dos pacientes tratados, conforme observado por outros autores23,25,26. Entretanto, nao tivemos a possibilidade de comparar o questionário de qualidade de vida (AQLQ) antes e após o início da terapia, pois nem todos os pacientes haviam respondido ao mesmo no início do tratamento, o que impossibilitou a utilizaçao deste desfecho.
A observaçao de que a maioria dos pacientes tinham sobrepeso ou eram obesos, 50% hipertensos e 20% diabéticos reforça a necessidade de intervençao terapêutica precoce na tentativa de evitar os efeitos adversos da corticoterapia sistêmica prolongada. Fatores ambientais como a própria obesidade e a corticoterapia podem ocasionar resistência a insulina com consequente hiperinsulinemia e ativaçao simpática, predispondo ao diabetes e hipertensao arterial, condiçoes clínicas que podem ser melhor controladas ou até mesmo prevenidas com a identificaçao de potenciais candidatos e instituiçao da terapia anti-IgE.
Na avaliaçao da segurança, o tratamento com omalizumabe foi bem tolerado e nenhum evento adverso sério foi registrado. Os eventos adversos descritos com mais frequência sao cefaleia, reaçao no local da aplicaçao e infecçoes de vias aéreas superiores27-29. No grupo estudado, o evento mais comum foi reaçao no local da aplicaçao, o que nao impediu a continuidade do tratamento e nao se repetiu nas aplicaçoes posteriores. Existe relato de que o número de eventos adversos diminuem significativamente ao longo do tratamento com omalizumabe17.
A terapia anti-IgE com omalizumabe mostrou-se importante adjuvante no tratamento deste grupo de pacientes com asma alérgica de difícil controle, pois proporcionou melhora significativa em parâmetros clínicos e funcionais utilizados para avaliaçao do controle da doença, possibilitando o controle das limitaçoes atuais e, possivelmente, a reduçao dos riscos futuros.
REFERENCIAS
1. Holgate ST, Polosa R. Treatment strategies for allergy and asthma. Nat Rev Immunol. 2008;8(3):218-30.
2. Global Initiative for Asthma [home page na internet]. GINA report, global strategy for asthma management and prevention. Update 2012. Disponível em: http://ginasthma.org/guidelines-gina-report-global-strategy-for-asthma.html. [Acesso em 2014 Mar 10].
3. Sociedade Brasileira de Pneumologia e Tisiologia. Diretrizes da Sociedade Brasileira de Pneumologia e Tisiologia para o manejo da asma - 2012. J Bras Pneumol. 2012;38(Supl 1):S1-46.
4. Consenso Latinoamericano sobre el Asma de Difícil Control. Actualización 2008. Drugs of Today. 2008;44(Suppl 3):1-43.
5. Brusselle G, Michils A, Louis R, Dupont L, Can de Maele B, Delobbe A, et al. "Real-life" effectiveness of omalizumab in patients with severe persistent allergic asthma: the PERSIST study. Respir Med. 2009;103:1633-42.
6. Grimaldi-Bensouda L, Zureik M, Aubier M, Humbert M, Levy J, Benichou J, et al. Does omalizumab make a difference to the real-life treatment of asthma exacerbations?: results from a large cohort of patients with severe uncontrolled asthma. Chest. 2013;143:398-405.
7. Humbert M, Busse W, Hanania NA, Lowe PJ, Canvin J, Erpenbeck VJ, et al. Omalizumab in Asthma: An Update on Recent Developments. J Allergy Clin Immunol Pract. 2014;2:525-36.
8. Thomson N, Niven R, Heaney L, Greening A. Development of an algorithm for the assessment of response to treatment with omalizumab. Thorax. 2007;62:(A99, P94).
9. Holgate S, Buhl R, Bousquet J, Smith N, Panahloo Z, Jimenez P. The use of omalizumab in the treatment of severe allergic asthma: A clinical experience update. Respir Med. 2009;103(8):1098-113.
10. WHO. Physical status: the use and interpretation of anthropometry. Report of a WHO Expert Committee. WHO Technical Report Series 854. Geneva: World Health Organization, 1995. Disponível em: http://www.who.int/childgrowth/publications/physical_status/en/. [Acesso em 2014 Mar 10].
11. Barnes N, Menzies-Gow A, Mansur AH, Spencer D, Percival F, Radwan A, et al. Effectiveness of omalizumab in severe allergic asthma: a retrospective UK real-world study. J Asthma. 2013;50(5):529-36.
12. Korn S, Thielen A, Seyfried S, Taube C, Kornmann O, Buhl R. Omalizumab in patients with severe persistent allergic asthma in a real-life setting in Germany. Respir Med. 2009;103(11):1725-31.
13. Bousquet J, Cabrera P, Berkman N, Buhl R, Holgate S, Wenzel S, et al. The effect of treatment with omalizumab, an anti-IgE antibody, on asthma exacerbations and emergency medical visits in patients with severe persistent asthma. Allergy. 2005;60(3):302-8.
14. Braunstahl GJ, Chen CW, Maykut R, Georgiou P, Peachey G, Bruce J. The eXpeRience registry: the 'real-world' effectiveness of omalizumab in allergic asthma. Respir Med. 2013;107(8):1141-51.
15. López Tiro JJ, Contreras EA, Del Pozo ME, Gómez Vera J, Larenas Linnemann D. Real life study of three years omalizumab in patients with difficult-to-controlasthma. Allergol Immunopathol (Madr). 2014 Apr 26. [Epub ahead of print] PubMed PMID: 24780091.
16. Bousquet J, Siergiejko Z, Swiebocka E, Humbert M, Rabe KF, Smith N, et al. Persistency of response to omalizumab therapy in severe allergic (IgE-mediated) asthma. Allergy. 2011;66(5):671-8.
17. Vennera MC, Llano LP, Bardagí S, Ausin P, Sanjuas C, González H, et al. Omalizumab Therapy in Severe Asthma: Experience from the Spanish Registry-Some New Approaches. J Asthma. 2012;49(4):416-22.
18. Korn S, Schumann C, Ktopf C, Stoiber K, Thielen A, Taube C, et al. Effectiveness of omalizumab in patients 50 years and older with severe persistent allergic asthma. Ann Allergy Asthma Immunol. 2010;105(4):313-9.
19. Tzortzaki EG, Georgiou A, Kampas D, Lemessios M, Markatos M, Adamidi T, et al. Long-term omalizumab treatment in severe allergic asthma: The South-Eastern Mediterranean "real-life" experience. Pulm Pharmacol Ther. 2012;25:77-82.
20 Verma P, Randhawa I, Klautesmayer WB. Clinical efficacy of omalizumab in an elderly veteran population with severe asthma. Allergy Asthma Proc. 2011;32:346-50.
21. Molimard M, Buhl R, Niven R, Le Gros V, Thielen A, Thirlwell J, et al. Omalizumab reduces oral corticosteroid use in patients with severe allergic asthma: real-life data. Respir Med. 2010;104:1381-5.
22. Niven R, Chung KF, Panahloo Z, Blogg M, Ayre G. Effectiveness of omalizumab in patients with inadequately controlled severe persistent allergic asthma: an open-label study. Respir Med. 2008;102:1371-8.
23. Humbert M, Beasley R, Ayres J, Slavin R, Hébert J, Bousquet J, et al. Benefits of omalizumab as add-on therapy in patients with severe persistent asthma who are inadequately controlled despite best available therapy (GINA 2002 step 4 treatment): INNOVATE. Allergy. 2005;60:309-16.
24. Weber EJ, Silverman RA, Callaham ML, Pollack CV, Woodruff PG, Clark S, et al. A prospective multicenter study of factors associated with hospital admission among adults with acute asthma. Am J Med. 2002;113:371-8.
25. Nowak D. Management of asthma with anti-immunoglobulin E: a review of clinical trials of omalizumab. Respir Med. 2006;100:1907-17.
26. Rubin AS, Souza-Machado A, Andradre-Lima M, Ferreira F, Honda A, Matozo TM; QUALITX Study Investigators. Effect of omalizumab as add-on therapy on asthma-related quality of life in severe allergic asthma: a Brazilian study (QUALITX). J Asthma. 2012;49:288-93.
27. Corren J, Casale TB, Lanier B, Buhl R, Holgate S, Jimenez P. Safety and tolerability of omalizumab. Clin Exp Allergy. 2009;39:188-97.
28. Vignola AM, Humbert M, Bousquet J, Boulet LP, Hedgecock S, Blogg M, et al. Efficacy and tolerability of anti-immunoglobulin E therapy with omalizumab in patients with concomitant allergic asthma and persistent allergic rhinitis: SOLAR. Allergy. 2004;59:709-17.
29. Molinard M, de Blay F, Didier A, Le Gros V. Effectiveness of omalizumab (Xolairr) in the first patients treated in real-life practice in France. Resp Med. 2008;102:71-6.