Número Atual: Abril-Junho 2018 - Volume 2 - Número 2
- Imprimir
- Indicar
- Estatísticas
- (0)
Comentários - Como Citar
- Download da Citação
- Artigos Relacionados
-
Outros dos
Autores
Comunicação Clínica e Experimental
Vasculite urticariforme e exantema: uma reação de hipersensibilidade tardia mista a dimenidrinato - relato de caso
Urticarial vasculitis and rash: a mixed delayed hypersensitivity reaction to dimenhydrinate - case report
Larissa Prando Cau; Danilo Gois Gonçalves; Rosana Camara Agondi; Pedro Giavina-Bianchi
Serviço de Imunologia Clínica e Alergia do HC-FMUSP, Sao Paulo, SP
Endereço para correspondência:
Larissa Prando Cau
E-mail: larissacau@yahoo.com.br
Submetido em: 11/04/2018
Aceito em: 16/04/2018
Nao foram declarados conflitos de interesse associados à publicaçao deste artigo.
RESUMO
Dimenidrinato é um anti-histamínico H1 do grupo das etanolaminas, com importantes propriedades anticolinérgicas, antisserotoninérgicas e sedativas. Relatamos um caso de uma mulher que após 14 dias de ter usado dimenidrinato, iniciou quadro de exantema e vasculite urticariforme, além de sintomas constitucionais. Avaliaçao laboratorial sem alteraçoes. Biopsia de pele evidenciou dermatite de interface do tipo vacuolar e púrpura com leucocitoclasia e derrame pigmentar. Imunofluorescência positiva para IgG, com presença de fluorescência dos núcleos dos queratinócitos da epiderme. Tratada com corticoide oral por 2 meses até remissao completa do quadro, e posterior realizaçao de teste intradérmico, que foi positivo na leitura de 48h. A reaçao de hipersensibilidade tardia observada foi relacionada a mecanismo misto de Gell e Coombs (III e IV), com positividade no teste cutâneo intradérmico de leitura tardia em 48h (reaçao tipo IV) e biópsia compatível com vasculite cutânea (reaçao tipo III); lesoes exantemáticas (reaçao tipo IV) e urticária vasculítica (reaçao tipo III). O teste cutâneo com dimenidrinato positivo reforça o diagnóstico de reaçao de hipersensibilidade.
Descritores: Vasculite, reaçao de hipersensibilidade tardia, dimenidrinato.
INTRODUÇAO
Dimenidrinato é um anti-histamínico H1 do grupo das etanolaminas, com importantes propriedades anticolinérgicas, antiserotoninérgicas e sedativas. É usado em vários distúrbios, como vertigem, doença de movimento, náuseas e vômitos1,2. As reaçoes de hipersensibilidade a medicamentos (RHM) podem ser divididas em alérgicas, quando sao mediadas por mecanismos imunológicos, e nao alérgicas, quando nao apresentam um mecanismo imunológico envolvido. Na RHM alérgica, os mecanismos imunológicos envolvem a participaçao de anticorpos (tipos I, II, ou III) e de célula T3.
A classificaçao da RHM, conforme o mecanismo imunológico envolvido, é desafiadora, pois a apresentaçao clínica pode, com frequência, mostrar sobreposiçao de lesoes cutâneas e, por outro lado, um medicamento pode desencadear uma reaçao de hipersensibilidade envolvendo mais de um mecanismo imunológico concomitante. A padronizaçao da classificaçao das RHM facilita a comparaçao de estudos e ajuda a aprimorar e validar técnicas de diagnóstico. Clinicamente, as RHM imediatas (tipo I de Gell e Coombs) se caracterizam por urticária, angioedema, broncoespasmo, sintomas gastrointestinais e anafilaxia. Geralmente, elas ocorrem dentro de 1 a 6 h após a última administraçao da droga, envolvendo desgranulaçao de mastócitos e basófilos, mediada pela IgE ou nao. Outras RHM nao imediatas podem ser exemplificadas por outros mecanismos descritos por Gell e Coombs: nefrites e citopenias (tipo II - citotóxica); vasculites e doença do soro (tipo III - por deposiçao de imunocomplexos); dermatite de contato alérgica (tipo IVa - Th1 e inflamaçao monocítica); DRESS (Drug reaction with eosinophilia and systemic symptoms) e exantemas (tipo IVb - Th2 e eosinófilos); necrólise epidérmica tóxica (NET) e síndrome de Stevens-Johnson (SSJ) (tipo IVc - Linfócitos T citotóxicos); e PEGA (pustulose exantemática generalizada aguda) (tipo IVd - Linfócitos T e inflamaçao neutrofílica)3. As reaçoes alérgicas após a administraçao de dimenidrinato sao raras, em vista da frequência do uso.
RELATO DO CASO
Paciente feminina, 27 anos, branca, solteira, natural e procedente de Sao Paulo, SP, professora, previamente hígida. Refere que após 14 dias de ter utilizado 1 comprimido de dimenidrinato para cinetose, apresentou exantema maculopapular pouco pruriginoso, fixo, com evoluçao em poucos dias para áreas com púrpura palpável, formando grandes placas confluentes, acometendo quase totalmente o abdome e membros; poupando mucosa, face, mao, pés e tronco superior; com discreta dor e calor local, e sem descamaçao até o momento da avaliaçao inicial (Figuras 1, 2 e 3). Apresentava sintomas associados de cefaleia, náuseas e febre baixa (T max.: 37,6 °C). Diagnosticada inicialmente com quadro de Varicela, recebeu aciclovir oral e anti-histamínicos, porém sem melhora. Negava uso de anti-inflamatórios ou outros medicamentos nas últimas quatro semanas que antecederam o quadro. Ao exame estava em bom estado geral, eupneica, hidratada, corada e com as lesoes já descritas.
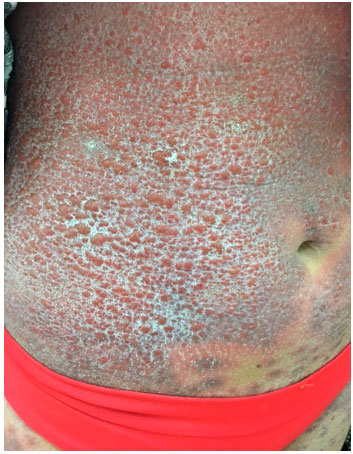
Figura 1 Placas maculopapulares confluentes com bordas purpúricas e eritematosas
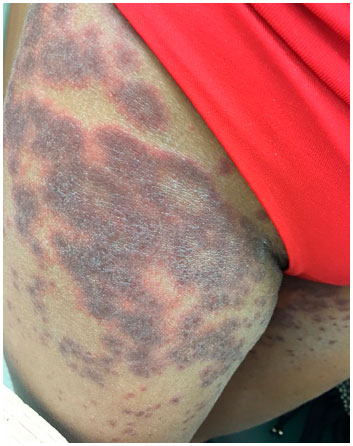
Figura 2 Lesoes purpúricas confluentes, com bordas eritematosas
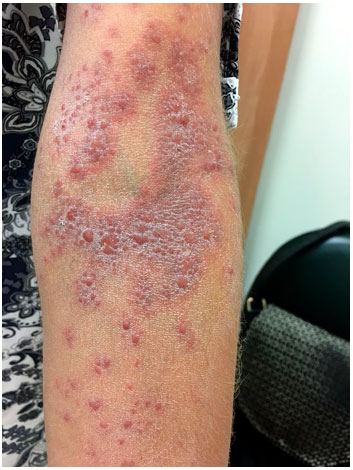
Figura 3 Placas urticariformes confluentes
O hemograma era normal, sem eosinofilia. PCR: 7 (valor de referência < 1), portanto, aumentado. Sem sinais de disfunçao renal ou hepática. Complemento e DHL: normais. Sorologias para HIV, vírus B e C, e sífilis negativas. Autoanticorpos, crioglobulinas, FAN e ANCA foram negativos. Ultrassonografia de abdome: normal. A lesao foi biopsiada em três locais diferentes do abdome e antebraço. Anatomopatológico evidenciou: Dermatite de interface do tipo vacuolar e púrpura com leucocitoclasia e derrame pigmentar. Imunofluorescência positiva para IgG, com presença de fluorescência dos núcleos dos queratinócitos da epiderme.
Iniciado tratamento com prednisona 1 mg/dia por um mês, seguido de reduçao gradual da dose em 2 meses, evoluindo com regressao completa do quadro (Figuras 4 e 5). Após 1 mês da suspençao do corticoide, foram realizados testes cutâneos com o medicamento suspeito na forma injetável. Prick test foi negativo. Teste intradérmico realizada em 3 concentraçoes, com leituras de 20 minutos e 6 horas negativas; positivo na concentraçao de 0,1 mg/ mL em 48h (controles negativos formados por 10 voluntários sadios: testes negativos). O patch test foi negativo.
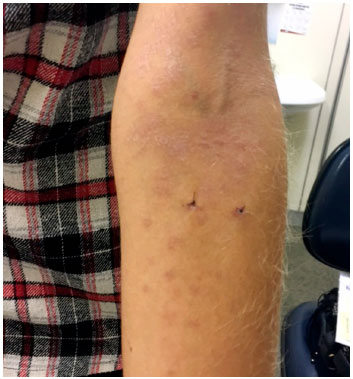
Figura 4 Lesoes em cicatrizaçao
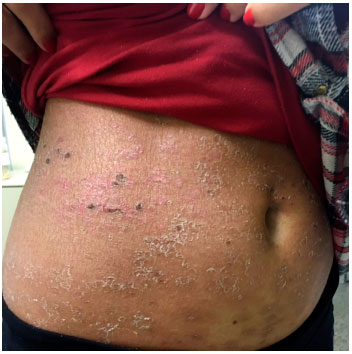
Figura 5 Lesoes em cicatrizaçao, com descamaçao e crostas
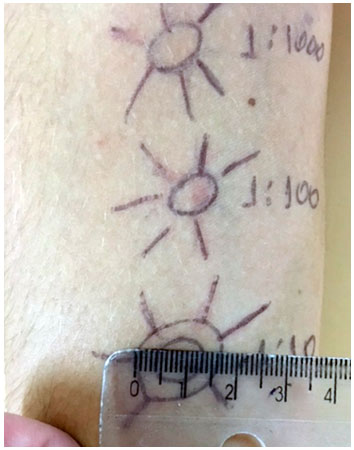
Figura 6 Positividade do teste cutâneo na concentraçao 0,3 mg/mL (1:10)
DISCUSSAO
A reaçao de hipersensibilidade tardia relatada mostrou-se estar relacionada a mecanismo misto de Gell e Coombs tipos III e IV, com positividade no teste cutâneo intradérmico de leitura tardia em 48h (reaçao tipo IV), porém com biópsia compatível com vasculite cutânea (reaçao tipo III). As lesoes exantemáticas sugerem reaçao tipo IV e a urticária vasculítica reaçao tipo III1,6. No caso relatado, observamos teste cutâneo com positividade para o medicamento, que reforça o diagnóstico de reaçao de hipersensibilidade a dimenidrinato.
A vasculite urticariforme é uma entidade clinicopatológica incomum que pode ser hipocomplementêmica (baixos níveis de C1q e C4 e níveis de C3 de diminuiçao variável, ocorrendo quase que exclusivamente em pacientes do sexo feminino), ou normocomplementêmica. Sua prevalência relatada é de cerca de 5 a 10% em pacientes com urticária crônica, nos quais os episódios de urticária estao caracteristicamente associados à vasculite leucocitoclástica1-3,6. No entanto, o infiltrado inflamatório misto, de linfócitos e eosinófilos, é observado com mais frequência do que a vasculite leucocitoclástica3,4,8. Permanece idiopática na maioria dos casos, ou é secundária a doenças do tecido conjuntivo, com prevalência de 20% no lúpus eritematoso sistêmico, e 32% na Síndrome de Sjögren. Doença do soro, neoplasias (leucemias ou tumores de mama, hipófise, tireoide, cólon e pâncreas) e infecçoes (hepatite B, hepatite C, HIV, sífilis e mononucleose infecciosa) sao comumente descritas. Clinicamente, as lesoes na vasculite urticariforme duram, geralmente, de 48 a 72 horas; o angioedema, envolvendo lábios, língua, pálpebras e maos, pode ocorrer adicionalmente em 40% dos casos. As lesoes diferem da urticária crônica espontânea em sua associaçao com queimaçao, dor ou sensibilidade aumentada, púrpura e endurecimento, que geralmente desaparecem com hiperpigmentaçao3,5.
A variedade hipocomplementêmica pode ser grave e estar associada a febre, mal-estar, mialgia, fadiga e organopatia (artralgia, artrite, serosite, glomerulonefrite e nefrite intersticial), fenômeno de Raynaud ou conjuntivite e episclerite4. No caso descrito, a paciente apresentou sintomas constitucionais, mas com complemento normal. Ulceras cutâneas ou danos em múltiplos órgaos (pulmoes, olhos e rins) nao sao incomuns na variedade secundária ou hipocomplementêmica.
Os casos com complemento normal ou idiopática geralmente respondem a anti-histamínicos ou antiinflamatórios nao esteroidais (AINEs), enquanto que pacientes com organopatia ou doença grave requerem corticosteroides sistêmicos ou outros medicamentos modificadores da doença (hidroxicloroquina, colchicina, dapsona, azatioprina ou ciclofosfamida). Embora a resoluçao espontânea ocorra geralmente em casos normocomplementêmicos ou idiopáticos, o prognóstico depende do grau de comprometimento sistêmico e/ou cutâneo adjacente.
Os medicamentos foram implicados em cerca de 10% dos casos de vasculite, e o diltiazem, a cimetidina, os antibióticos, o interferon, os AINEs e o iodeto de potássio permanecem como drogas comumente implicadas5. Glatiramer, glimepirida, enalapril, telmisartan e levetiracetam, também foram relatados como desencadeantes de vasculite urticariforme. Curiosamente, os fármacos parecem provocar vasculite urticariforme após um período variável, independentemente da dose e frequência de administraçao do fármaco. Por exemplo, uma mulher de 48 anos desenvolveu vasculite urticariforme histologicamente confirmada, 3 meses após o acetato deglatiramer ter sido administrado para esclerose múltipla7; vasculite urticariforme induzida por glimepirida em uma mulher de 72 anos ocorreu 6 semanas após o início da droga; e o mesmo quadro apareceu 8 dias após o tratamento com enalapril8.
O diagnóstico de vasculite urticariforme induzida por drogas, na maioria dos casos, é por exclusao de outras causas conhecidas, correlaçao temporal entre a ingestao de drogas e o surgimento de erupçoes cutâneas, correlaçao clinicopatológica e melhora dos sintomas após a suspensao do medicamento suspeito ou provocaçao com o medicamento (reexposiçao). No caso relatado, o diagnóstico foi confirmado pelo teste cutâneo.
REFERENCIAS
1. Paffumi I, Saitta S, Isola S, Gangemi S. Urticaria caused by dimenhydrinate. Allergol Immunopathol (Madr). 2012;40(4):253-4.
2. Tan DS, Sklar GE. Erythema multiforme secondary to dimenhydrinate in a patient with previous similar reactions to pamabrom. Ann Pharmacother. 2014 Mar;48(3):425-8.
3. Demoly P, Adkinson NF, Brockow K, Castells M, Chiriac AM, Greenberger PA, et al. International Consensus on drug allergy. Allergy. 2014 Apr;69(4):420-37.
4. Her MY, Song JY, Kim DY. Hypocomplementemic urticarial vasculitis in systemic lupus erythematosus. J Korean Med Sci. 2009;24:184-6.
5. Kulthanan K, Cheepsomsong M, Jiamton S. Urticarial vasculitis: Etiologies and clinical course. Asian Pac J Allergy Immunol. 2009;27:95-102.
6. Vikram K Mahajan, Ravinder Singh, Mrinal Gupta, Rashmi Raina. Telmisartan induced urticarial vasculitis. Indian Journal of Pharmacology. 2015;47:560-2.
7. Cicek D, Kandi B, Oguz S, Cobanoglu B, Bulut S, Saral Y. An urticarial vasculitis case induced by glatiramer acetate. J Dermatolog Treat. 2008;19:305-7.
8. Ben Salem C, Hmouda H, Bouraoui K. Glimepirideinduced vasculitis: A case report. Br J Clin Pharmacol. 2007;64:113-4.



