Número Atual: Abril-Junho 2017 - Volume 1 - Número 2
- Imprimir
- Indicar
- Estatísticas
- (0)
Comentários - Como Citar
- Download da Citação
- Artigos Relacionados
-
Outros dos
Autores- Adriana A. Antunes
- Dirceu Solé
- Vânia O. Carvalho
- Ana E. Kiszewski Bau
- Fábio C. Kuschnir
- Márcia C. Mallozi
- Jandrei R. Markus
- Maria G. Nascimento e Silva
- Mário C. Pires
- Marice E. El Achkar Mello
- Nelson A. Rosário Filho
- Emanuel S. Cavalcanti Sarinho
- Herberto J. Chong-Neto
- Norma P. M. Rubini
- Luciana R. Silva
ARTIGO ESPECIAL
Guia prático de atualização em dermatite atópica - Parte I: etiopatogenia, clínica e diagnóstico. Posicionamento conjunto da Associação Brasileira de Alergia e Imunologia e da Sociedade Brasileira de Pediatria
Updated practical guide on atopic dermatitis - Part I: etiopathogenesis, clinical features, and diagnosis. Joint position paper of the Brazilian Association of Allergy and Immunology and the Brazilian Society of Pediatrics
Adriana A. Antunes1,16; Dirceu Solé2,18,19; Vânia O. Carvalho3,17; Ana E. Kiszewski Bau4,17; Fábio C. Kuschnir5,16; Márcia C. Mallozi6,18; Jandrei R. Markus7,17; Maria G. Nascimento e Silva8,16; Mário C. Pires9,18; Marice E. El Achkar Mello10,17; Nelson A. Rosário Filho11,18,19; Emanuel S. Cavalcanti Sarinho12,17,19; Herberto J. Chong-Neto13,17,18; Norma P. M. Rubini14,18; Luciana R. Silva15,19
DOI: 10.5935/2526-5393.20170019
1. Professora Associada de Pediatria, Universidade de Pernambuco, PE
2. Professor Titular de Alergia, Imunologia Clínica e Reumatologia, Universidade Federal de Sao Paulo, SP
3. Professora Associada de Pediatria, Universidade Federal do Paraná (UFPR), PR
4. Professora Adjunta de Dermatologia, Universidade Federal de Ciências da Saúde de Porto Alegre, RS
5. Professor Adjunto de Pediatria, Universidade do Estado do Rio de Janeiro, RJ
6. Professora Assistente, Departamento de Pediatria, Faculdade de Medicina do ABC, SP
7. Professor de Pediatria e Dermatologia, ITPAC Porto Nacional, TO
8. Professora de Pediatria, Faculdade de Medicina Estácio de Juazeiro do Norte, CE
9. Doutor em Ciências da Saúde pelo Hospital do Servidor Público Estadual de Sao Paulo, Especialista em Dermatologia, e Alergia e Imunologia Clínica
10. Médica Especialista em Pediatra e Dermatologia, Universidade Federal de Santa Catarina, SC
11. Professor Titular de Pediatria, UFPR, PR
12. Professor Associado de Pediatria, Universidade Federal de Pernambuco, PE
13. Professor Adjunto de Pediatria, UFPR, PR
14. Professora Titular, Disciplina de Alergia e Imunologia, UNIRIO-EMC, RJ
15. Professora Titular de Pediatria, Universidade Federal da Bahia, BA
16. Departamento Científico de Alergia, Sociedade Brasileira de Pediatria (SBP)
17. Departamento Científico de Dermatologia, SBP
18. Associaçao Brasileira de Alergia e Imunologia (ASBAI)
19. Sociedade Brasileira de Pediatria (SBP)
Endereço para correspondência:
Dirceu Solé
E-mail: alergiaimunoreumatologia@unifesp.br
Submetido em: 10/01/2017
Aceito em: 15/02/2017.
Nao foram declarados conflitos de interesse associados à publicaçao deste artigo.
RESUMO
A dermatite atópica (DA) é uma doença crônica e recidivante que acomete principalmente pacientes da faixa etária pediátrica. A fisiopatologia inclui fatores genéticos, alteraçoes na barreira cutânea e imunológicas. A prevalência da DA no Brasil, entre adolescentes, oscila entre 7,1% e 12,5%, com tendência à estabilizaçao. O diagnóstico é clínico, e exames complementares auxiliam na determinaçao dos fatores desencadeantes. A identificaçao dos fatores irritantes e/ou desencadeantes envolvidos permite melhor controle das crises. Entre os fatores desencadeantes destacam-se os agentes infecciosos, alérgenos alimentares e aeroalérgenos. Tomando-se como ponto de partida o "Guia Prático para o Manejo da Dermatite Atópica - opiniao conjunta de especialistas em alergologia da Associaçao Brasileira de Alergia e Imunopatologia e da Sociedade Brasileira de Pediatria" publicado em 2006, foi realizada revisao e atualizaçao dos conceitos apresentados por grupo de alergologistas, dermatologistas e pediatras especializados no tratamento de pacientes com DA. O objetivo desta revisao foi elaborar um documento prático e que auxilie na compreensao dos mecanismos envolvidos na DA, assim como dos possíveis fatores de risco associados a sua apresentaçao, bem como sobre a avaliaçao subsidiária disponível para a identificaçao dos fatores associados à DA.
Descritores: Dermatite atópica, fatores de risco, diagnóstico clínico, Staphylococcus aureus, IgE específica, teste cutâneo, alergia alimentar.
DEFINIÇOES
A dermatite atópica (DA) é uma doença inflamatória cutânea crônica de etiologia multifatorial que se manifesta clinicamente sob a forma de eczema. As pessoas afetadas apresentam, em geral, antecedente pessoal ou familiar de atopia1-3. O eczema é caracterizado por eritema mal definido, edema e vesículas no estágio agudo e, no estágio crônico, por placa eritematosa bem definida, descamativa e com grau variável de liquenificaçao. O termo eczema atópico é aceito como sinônimo de DA3.
Os pacientes com DA compartilham as características de xerodermia (pele seca) e limiar diminuído para prurido. O eczema ocorre de maneira cíclica durante a infância, podendo prolongar-se até a fase adulta2,4,5. Em alguns pacientes, o prurido é constante e incontrolável, sendo um dos fatores responsáveis pela diminuiçao da qualidade de vida dos pacientes e de seus familiares3.
Os indivíduos atópicos apresentam predisposiçao hereditária para desenvolver resposta de hipersensibilidade imediata mediada por anticorpos da classe IgE6. Neste contexto, a presença de eczemas em topografia característica, o prurido, a história pessoal ou familiar de asma, rinite alérgica e conjuntivite, e/ou DA e o caráter recidivante das lesoes durante a infância sao os critérios maiores para o diagnóstico de DA2,3.
EPIDEMIOLOGIA
A prevalência da DA aumentou nas últimas três décadas. Embora possa se manifestar em qualquer período etário, 60% dos casos de DA ocorrem no primeiro ano de vida8,9. A DA assume forma leve em 80% das crianças acometidas10, e em 70% dos casos há melhora gradual até o final da infância11,12.
No primeiro ano de vida, a prevalência de diagnóstico médico de DA, em países da Europa e América Central, foi avaliada como parte do International Study of Wheezing in Infants (Estudio Internacional de Sibilancia en el Lactente, EISL)6. Observou-se variaçao ampla das taxas encontradas: 10,6% (Valência, Espanha) a 28,2% (San Pedro Sula, Honduras). Os valores médios obtidos na América Central foram significantemente mais elevados quando comparados aos da Europa: 18,2% e 14,2%, respectivamente13. A história familiar de DA foi o principal fator associado à expressao da doença13.
Dados mundiais sobre a prevalência da DA foram obtidos pela primeira vez pelo International Study of Asthma and Allergies in Childhood (ISAAC)9. Neste estudo foram avaliados escolares (6 e 7 anos de idade) e adolescentes (13 e 14 anos) de 153 centros localizados em 56 países9. A resposta afirmativa à questao sobre presença de lesoes eczematosas, pruriginosas e que acometiam áreas específicas do corpo caracterizou o diagnóstico de eczema flexural, quesito com elevada especificidade para o diagnóstico de DA. Os resultados observados mostraram-se variáveis, oscilando entre 1,5% (Ira) e 20,9% (Suécia) para os escolares, e entre 1,3% (China) e 19,4% (Etiópia) para os adolescentes. Na América Latina e no Brasil, os valores foram intermediários. No Brasil, a prevalência média de eczema flexural foi 6,8% para os escolares, e 4,7% para os adolescentes. Em todas as localidades a prevalência de DA foi maior entre os escolares9.
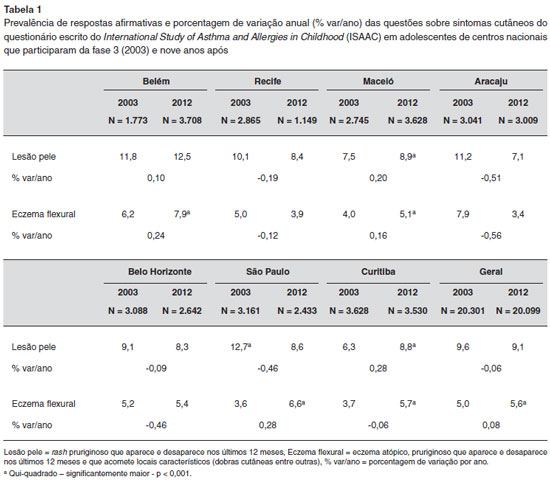
Houve aumento da prevalência de eczema flexural na reavaliaçao nove anos após a fase 3 do ISAAC, em alguns centros nacionais, tanto para os escolares quanto para os adolescentes (Tabela 1)14, apesar de o relato de problemas cutâneos ter se mantido estável.
Em adultos, estudos recentes estimaram prevalência de DA ao redor de 10%15, e persistência da doença cujo início ocorreu na idade adulta, maior do que se supunha16.
FATORES DE RISCO
Os fatores genéticos, apesar de muito importantes, nao explicam as diferenças existentes na prevalência da DA em localidades distintas, nem o aumento da prevalência observado nas últimas décadas em várias regioes do mundo. A interaçao entre fatores genéticos predisponentes à DA e fatores ambientais e/ou exacerbantes, tais como exposiçoes maternas durante a gestaçao, irritantes de contato com a pele, clima, poluentes, fumaça de tabaco, água dura, vida urbana e rural e dieta têm sido apontados como potenciais determinantes desse aumento da prevalência17-19. Estudos longitudinais têm demonstrado que a persistência da DA na idade adulta está relacionada a: idade precoce de início dos sintomas, formas graves de apresentaçao, história familiar de DA e sensibilizaçao alérgica precoce17,18. Além desses, destacam-se: ter sibilos no último ano, ter rinite alérgica, e o menor grau de escolaridade materna como fatores de risco associados à presença de DA, sobretudo grave, em nosso meio18.
Desse modo, é importante que os fatores de risco associados à expressao da DA sejam identificados para que intervençoes futuras possam ser tomadas de modo adequado.
Fatores ambientais
Exposiçoes maternas durante a gestaçao
Apesar de vários questionamentos, documentouse relaçao direta entre estresse materno e o possível desenvolvimento e/ou evoluçao para DA na infância, possivelmente por interferência no desenvolvimento do sistema imunológico do feto20. O mesmo foi observado com relaçao à exposiçao passiva ao fumo do tabaco21. Resultados controversos foram observados entre o consumo de antibióticos e de álcool e evoluçao para DA19,22.
Irritantes e agentes que causam prurido
Alguns agentes ambientais, como saboes e detergentes, agridem a pele, interferem com a barreira cutânea e facilitam a interaçao entre irritantes e alérgenos e o sistema imunológico, promovendo inflamaçao. Destaca-se lauril sulfato de sódio e hidróxido de sódio23.
Mudanças climáticas
Alguns estudos têm associado mudanças de prevalência de DA a alteraçoes climáticas, entretanto, deve-se ter em mente que o clima de uma regiao envolve temperatura, umidade e precipitaçao, além de fatores relacionados como a exposiçao à radiaçao ultravioleta (UV)19.
Temperatura - Há relatos de melhora da DA com o aumento da temperatura, e cogita-se ser decorrente do menor uso de sistemas de aquecimento no interior do domicílio, ou pelo fato de os pacientes passarem mais tempo fora de casa, sendo mais expostos aos raios UV. Estudo nacional documentou menor controle da DA em localidades com maior temperatura24. O calor aumenta a perspiraçao, que funciona como irritante, acentuando a inflamaçao na DA.
Os resultados díspares entre efeitos protetores da temperatura na populaçao e efeitos danosos aos pacientes com DA necessitam de consideraçoes. Pode ser que uma temperatura mais alta proteja direta ou indiretamente indivíduos nao afetados de desenvolver DA, enquanto que temperaturas mais altas nao sao bem toleradas por pacientes com DA estabelecida19.
Umidade - Embora haja relato de que a umidade relativa baixa intradomiciliar seja associada a baixas taxas de DA, há resultados conflitantes, e mais estudos sao necessários19.
Radiaçao ultravioleta - Estudos norte-americanos documentaram menor prevalência de DA em locais com alta exposiçao à radiaçao ultravioleta (UV)25. Supoe-se que seja decorrente de açao imunossupressora local, ou pela maior transformaçao de vitamina D19.
Precipitaçao -Estudos norte-americano e europeu evidenciaram menor prevalência de DA em localidades com índice pluviométrico elevado. Os autores acreditam que tal efeito seja decorrente da menor exposiçao à radiaçao UV que ocorre nessas localidades, além de alteraçao na regulaçao da filagrina como resultado da persistência da inflamaçao cutânea19,25.
Poluentes atmosféricos
Os poluentes atmosféricos ainda nao foram identificados como fatores de risco para a DA. Admite-se que atuariam diretamente na pele por ligar-se ao estrato córneo, sendo metabolizados ou mesmo penetrando a epiderme e ganhariam a circulaçao sistêmica via capilares dérmicos26. De maneira geral, há associaçao entre exposiçao a poluentes externos e maior gravidade da DA. Viver em casas próximas a ruas de tráfego intenso associou-se à maior prevalência de DA e a formas mais graves27,28.
Poluentes intradomiciliares
Vários poluentes intradomiciliares sao apontados como possivelmente relacionados à expressao e/ou agravamento da DA: material de combustao (fogoes, lareiras), material de construçao, fontes biológicas e produtos de limpeza. Entretanto, os resultados sao controversos, e mais estudos sao necessários19,29.
Exposiçao à fumaça de tabaco
Embora seja muito clara a açao do tabagismo sobre a asma, na DA essa açao é discutida. Revisao sistemática e metanálise de 86 estudos documentou que o tabagismo ativo e o passivo sao associados a maior risco de DA, fato nao observado com o tabagismo materno durante a gestaçao21.
Água dura
A exposiçao à água dura (concentraçao elevada de minerais: cálcio e magnésio) tem sido associada com piora da DA30, mas nao de modo unânime. Admitese que isto ocorreria por irritaçao direta dos íons cálcio e magnésio e/ou necessidade de quantidades maiores de saboes para a limpeza da pele com uso dessa água19. Estudo inglês que promoveu a retirada desses íons da água nao documentou mudanças na prevalência de DA31.
Dieta
Metanálise de estudos com dieta de restriçao materna de alimentos "alergênicos" durante a gestaçao nao documentou efeito protetor para a prole até os 18 meses de idade32. Entretanto, o consumo materno de peixe durante a gestaçao associou-se à reduçao na prevalência de DA no primeiro ano de vida, possivelmente pelo consumo de ácidos graxos poli-insaturados ômega 333.
Em crianças e adolescentes o uso de dieta pobre em vegetais, frutas, peixes, e azeite tem sido associado a maior prevalência de AD e outras doenças alérgicas34.
Aleitamento materno
Embora haja estudos longitudinais de aleitamento materno prolongado que mostram efeito protetor sobre o aparecimento de DA, sobretudo nos primeiros anos de vida35, estudos posteriores nao confirmaram tais observaçoes36. A relaçao entre aleitamento materno e introduçao de alimentos sólidos precisa ser alvo de estudos no futuro.
Probióticos e prebióticos
O uso de probióticos tem sido estudado com a finalidade de proteçao e terapêutica. Duas metanálises avaliaram estudos controlados por placebo e documentaram reduçao na prevalência de DA entre os tratados com probióticos19,37, mas a sua açao no tratamento da DA ainda merece estudos39. As evidências sobre o uso de prebióticos sobre o desenvolvimento de DA ainda sao limitadas.
Marcha atópica
O conceito de marcha atópica refere-se à história natural das doenças alérgicas. Há muito se observa que estas doenças podem se manifestar de forma variável em diferentes períodos da vida em um mesmo paciente. Isto ocorre por que as doenças atópicas compartilham aspectos genéticos e fisiopatológicos, destacando-se a sensibilizaçao a alérgenos e o predomínio Th239; entretanto, recentemente têm-se mostrado que as diferentes manifestaçoes clínicas de alergia apresentam uma progressao característica.
Tipicamente a criança desenvolve a DA nos primeiros meses de vida, que pode ser acompanhada pela sensibilizaçao às proteínas do leite de vaca, ovo ou amendoim, eventualmente manifestando vômitos, diarreia ou anafilaxia relacionados à ingestao destes alimentos, por volta dos 6-12 meses de vida. Este quadro é sucedido pela sensibilizaçao aos aeroalérgenos (ácaros domiciliares, epitélios animais), até que a criança manifeste episódios de sibilância de repetiçao antes dos dois anos de idade, em geral associados às infecçoes virais das vias aéreas superiores40,41.
Estudos epidemiológicos demonstraram que estas doenças apresentam diferentes períodos de prevalência, e quando uma destas melhora, a outra começa a se manifestar39. No caso da DA, estudos longitudinais mostraram picos de prevalência nos primeiros anos de vida de até 20%, e com o passar dos anos há diminuiçao significativa, chegando aos 5% na segunda década de vida. Em geral, a DA precede a asma e a rinite, e a prevalência de alergias respiratórias é muito maior entre os pacientes que apresentam ou apresentaram DA, chegando a 45%11. Um outro aspecto a ser ressaltado é a maior frequência de asma e rinite conforme a gravidade da dermatose, atingindo 70% entre pacientes com DA grave42.
Todas estas evidências contribuem para que a DA se torne um fator de risco importante para a asma. Estudo de coorte que avaliou 1.314 crianças, desde o nascimento até completarem sete anos de idade, observou que 69% das nascidas em famílias com dois membros atópicos ou que tinham IgE total elevada em sangue de cordao apresentaram DA. Destas, 50% desenvolveram alergia respiratória aos cinco anos de idade39.
O prognóstico da asma é pior entre os pacientes com DA. Estudo longitudinal de 10 anos em pacientes com asma demonstrou que entre os com DA houve 11% de asma grave ou morte por exacerbaçao aguda quando comparados a 5% de asma grave sem morte entre os pacientes sem DA. O estabelecimento desta relaçao direta entre asma e DA suscita a possibilidade do desenvolvimento de estratégias de prevençao. Coorte australiana, recentemente publicada, demonstrou que a sensibilizaçao aos aeroalérgenos e aos alérgenos alimentares nos primeiros dois anos de vida estao associadas ao desenvolvimento das alergias respiratórias (asma e rinite alérgicas a partir da idade escolar)43.
Genética
Muitos estudos realizados com famílias têm demonstrado que a DA é uma doença de caráter hereditário44,45. Inicialmente foram apresentados cinco estudos de linkage, observando uma possível associaçao genética entre as inúmeras variáveis descritas46. Foram realizados dois estudos sobre o genoma de crianças com DA: um em famílias na Alemanha e Escandinávia, e outro em crianças inglesas. O primeiro encontrou linkage com uma regiao do cromossoma 3q21, e o segundo encontrou relaçao entre DA ou DA associada à asma com três regioes: 1q21, 17q25 e 20p. Além disto, estes estudos mostraram também associaçao da IgE sérica total com as seguintes regioes: 3q21, 5q31 e 16q. Um outro estudo sobre genoma da DA, realizado em adultos suecos, encontrou associaçao com o cromossoma 3p (24-22). Utilizando o escore de gravidade da DA, os pesquisadores observaram associaçao com as regioes: 3q14,13q14, 15q14-15 e 17q21. O cromossoma 13q14 também tem sido associado à criança com DA, atopia e asma47. Outro aspecto interessante é que as regioes 1q21, 17q25 e 20p associadas à DA também apresentam genes de susceptibilidade para a psoríase. Estes achados sugerem que regioes contendo genes polimórficos, que afetam a inflamaçao cutânea e a imunidade, podem ser compartilhados por DA e psoríase, sendo responsáveis por aspectos comuns a ambas doenças.
Nos últimos anos, as novas tecnologias de sequenciamento genético foram utilizadas nas pesquisas envolvendo DA, incluindo duas análises de exoma, com o propósito de identificar variantes genéticas raras, sobretudo nos casos sem um padrao familiar conhecido48. Entre os estudos descritos, 65 genes foram associados à DA, na sua grande maioria relacionados à mutaçao do gene da filagrina (FLG).
Os genes da via de sinalizaçao do tipo Th2 representam a segunda associaçao mais documentada nos estudos independentes: interleucina (IL)-4, IL-13, IL-4RA, IL-13RA1, IL-13RA2 e STAT6, além do gene da linfopoetina tímica (TSLP), seus receptores IL-7R e TSLPR49, e IL-3150. Na categoria dos genes de barreira cutânea, foi observada uma associaçao com os genes LAMA351, TMEM79, filagrina-2 (FLG2)52 e LELP153. Recentemente, a via de sinalizaçao da vitamina D tem sido estudada, e alguns polimorfismos no seu receptor e no CYD27A1 têm sido associados à gravidade da DA54,55.
ETIOPATOGENIA
Na etiopatogenia da DA, duas hipóteses vêm sendo discutidas sistematicamente. Na primeira, de fora para dentro (outside-inside), a DA seria produzida primariamente por uma disfunçao de barreira, e na segunda, de dentro para fora (inside-outside), seria produzida primariamente por uma alteraçao imune que desencadearia uma resposta inflamatória a irritantes e alérgenos ambientais19. É provável que todos os pacientes apresentem uma combinaçao de desregulaçao imunológica e disfunçao da barreira da pele e que ambas as hipóteses de fora para dentro e de dentro para fora sejam relevantes em diferentes subgrupos de pacientes19,56.
Barreira cutânea e mecanismos alterados
A barreira cutânea é composta por um conjunto de sistemas que protegem a pele da penetraçao de substâncias químicas alergênicas e irritantes, assim como contra as infecçoes (bacterianas e virais). Os sistemas (Figura 1) estao intimamente relacionados e o desequilíbrio de um pode gerar a ruptura dos mecanismos de barreira cutânea, desencadeando o processo inflamatório. Estes sistemas sao19,57,58: a) barreira mecânica celular: composta por corneócitos; b) manto lipídico: lipídios produzidos pelos corpos lamelares da camada granulosa; c) manto ácido: pH ácido da superfície cutânea, entre 4,5 e 5,5, que dificulta a multiplicaçao de bactérias; e d) flora residente: flora bacteriana cutânea normal dificulta a colonizaçao por bactérias patogênicas.
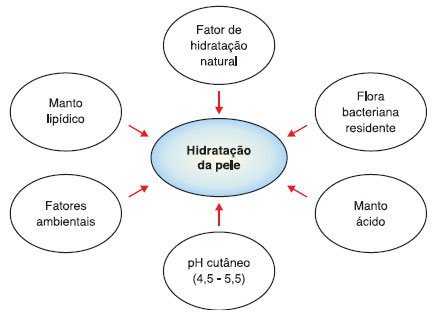
Figura 1 As inter-relaçoes e interdependências entre os fatores que influenciam na barreira cutânea e no controle da hidrataçao da pele
A barreira cutânea mecânica está localizada na camada superior da pele, o estrato córneo. A sua integridade é importante, pois além de evitar a penetraçao de alérgenos, evita a perda excessiva de água transepidérmica (Transepidermal Water Loss - TEWL). O estrato córneo é formado por corneócitos e lipídios19. O modelo referido por Michaels et al., em 1975, como "tijolo e argamassa" foi revisado e confirmado por Johnson et al., em 1997, e ainda hoje é um modelo adequado para a compreensao do arranjo celular e dos canais de permeabilidade cutânea1,58,59. Neste modelo, os corneócitos representam os tijolos e os lipídios intercelulares representam a argamassa. O corneócito é um envelope cornificado, constituído por proteínas densamente reticuladas, tais como filagrina, loricrina e involucrina. Os lipídios intercelulares estao constituídos por ceramidas (40%), colesterol (25%), sulfato de colesterol (10%) e ácidos graxos livres (25%). Dos lipídios intercelulares, as ceramidas sao as principais responsáveis pela retençao de água no espaço intercelular.
Na DA há reduçao do conteúdo de ceramidas no estrato córneo e as subfraçoes 1 e 3 das ceramidas estao reduzidas2,59. Isto pode ser decorrente do aumento da atividade enzimática (esfingomielinadesacilase) ou ser consequente à reduçao da produçao de ceramidas pelos queratinócitos do estrato granuloso57. A matriz lipídica (conhecida como manto lipídico) atua como principal via de penetraçao de substâncias através da pele, e é fundamental para a integridade da barreira cutânea. Por outro lado, a filagrina, uma proteína importante para a estrutura do envelope cornificado, é crucial para o alinhamento da queratina58. Os metabólitos da filagrina fazem parte do Fator de Hidrataçao Natural (FHN), que é necessário para a hidrataçao do estrato córneo7,58.
O FHN foi descrito pela primeira vez em 1959, e representa de 15 a 20% do peso do estrato córneo. É composto por diversas moléculas de baixo peso molecular, higroscópicas, orgânicas ou nao, que interagem entre si e atraem água do ambiente para o corneócito57,60. Sua composiçao contém 40% de aminoácidos; ácido carboxílico da pirrolidona (PCA) 12%; lactato 12%, ureia 7%; amônia, ácido úrico, glucosamina, creatinina e citrato 1,5%; sódio 5%, potássio 4%, cálcio 1,5%; magnésio 1,5%; fosfato 0,5%; cloreto 6%; açúcar, ácidos orgânicos, peptídeos e outras substâncias 8,5%. Na pele, a degradaçao da filagrina gera aminoácidos higroscópicos, incluindo ácido urocânico (UCA) e ácido pirrolidona carboxílico (PCA). UCA e PCA sao componentes do FHN que hidratam e ajudam a manter o pH ácido do estrato córneo.
A filagrina e seus produtos de degradaçao (PCA e UCA) sao muito importantes na manutençao do FHN, sendo fundamental para a manutençao da integridade da barreira cutânea, e consequentemente da hidrataçao da pele57,58. Nos últimos anos, estudos mostraram que as mutaçoes com perda de funçao no gene da filagrina afetam 20% a 50% dos pacientes com DA, produzindo nestes pacientes reduçao importante dos seus metabolitos, como o PCA e a UCA19,58,59. Por este motivo, pacientes com mutaçoes no gene da filagrina apresentam risco maior para desenvolver DA, assim como maior gravidade. As alteraçoes nos lipídios do estrato córneo sao independentes das mutaçoes do gene da filagrina e também se correlacionam com maior gravidade da doença57.
O pH ácido da pele ajuda a reduzir a expressao de duas proteínas estafilocócicas de superfície: o fator de aglutinaçao B e a proteína de ligaçao à fibronectina (que se ligam no hospedeiro à citoqueratina e à fibronectina, respectivamente). Além disso, UCA e PCA podem inibir diretamente a proliferaçao de S. aureus 61. A funçao da filagrina na prevençao de infecçoes da pele é dupla: como uma barreira física e de modulaçao da proliferaçao do S. aureus61.
O pH cutâneo ácido (4,5 a 5,5) propicia a manutençao da flora bacteriana residente normal, que é constituída por bactérias Gram-positivas (Staphylococcus sp, S.epidermidis, Micrococcus luteus, Corynebacterium, Streptococcus sp). Associados, o pH ácido e a presença da flora residente dificultam a colonizaçao por bactérias patógenas, principalmente S. aureus. Enquanto aproximadamente 10% da populaçao geral é colonizada pelo S. aureus, 90% dos pacientes com DA apresentam colonizaçao por S. aureus em área lesional, e 55% a 75% em pele nao afetada62. A pequena diversidade bacteriana da pele do indivíduo atópico contribui junto com outros fatores para a maior colonizaçao por S. aureus 63. Entre os outros fatores estao a reduçao de peptídeos antimicrobianos (PAM), que ajudam na defesa do hospedeiro contra bactérias, fungos e vírus; a deficiência de defensinas B e diminuiçao no recrutamento de neutrófilos. Além disso, as citocinas IL-4 e IL-13 podem inibir a produçao de PAM e reduzir a imunidade inata anti-S. aureus62.
Revisao sistemática recente documentou abundância de S. aureus e S. epidermidis na pele de pacientes com DA, e diminuiçao de outros patógenos, incluindo Propiobacterium. Além disso, Streptococcus, Acinetobacter e Malassezia têm sido envolvidos no desequilíbrio da flora cutânea encontrada na DA3,64. Corynebacterium é uma bactéria abundante na pele humana saudável e parece estar inversamente relacionada ao S. aureus3.
Há preocupaçao crescente com o aumento de S. aureus resistentes à meticilina em pacientes com DA, uma vez que estes sao colonizados muito frequentemente pelo S. aureus em comparaçao à populaçao geral61,64.
A disfunçao da barreira cutânea pode ser adquirida após exposiçao a irritantes e perturbaçoes mecânicas, como ocorre após exposiçao a substâncias alcalinas (como por exemplo, sabonetes), cloro das piscinas, banho com água aquecida e fricçao exagerada. Estes fatores podem desencadear a inflamaçao pela liberaçao de citocinas por meio dos queratinócitos danificados57.
Alteraçoes imunológicas
A partir da ruptura da barreira física, se inicia uma resposta imune inata rápida para evitar invasao e replicaçao microbiana65. Os queratinócitos e as células apresentadoras de antígenos da pele expressam uma série de receptores imunes inatos, entre os quais os receptores Toll like (TLRs) sao os mais conhecidos. A estimulaçao de TLRs por agentes microbianos ou lesoes teciduais induz a liberaçao de peptídeos antimicrobianos, citocinas e quimiocinas que aumentam a força da junçao intercelular com o intuito de limitar a penetraçao de alérgenos e micro-organismos.
Estudos têm demonstrado que os pacientes com DA têm a funçao dos TLR reduzida65,66. Um desequilíbrio do sistema imune adaptativo mediado por várias células T desempenha papel fundamental na patogênese da DA. Clinicamente a pele nao lesada de pacientes com DA, apesar de "aparência saudável", exibe infiltraçao de células T que produzem mediadores inflamatórios responsáveis pela diminuiçao da diferenciaçao epidérmica67,68.
Tradicionalmente, a exposiçao prolongada a agentes patogênicos adapta as respostas imunes e impulsiona o desenvolvimento de um ambiente de citocinas T helper (Th) 2 especializado: IL-4, IL-13 e IL-31. Células dendríticas (DCs) e células de Langerhans (LCs) tornam-se ativadas pelo reconhecimento de antígenos derivados de agentes patogênicos e, por consequência, promovem a induçao de resposta imune Th1, Th2, Th17 e Th22 em lesoes agudas de DA68.
O mecanismo de troca de classe (switching) de classe IgE também induz a maturaçao de DCs/ LCs que expressam receptor de alta afinidade para IgE e sua capacidade de formar respostas imunes adaptativas e de induzir o recrutamento de células inflamatórias. As citocinas derivadas de vários subtipos de células T modificam gradualmente a doença, de fase nao-lesional para fase crônica65. A linfopoietina estromal tímica (TSLP) é um fator importante como indutor das propriedades de polarizaçao Th2 impulsionadas por DCs na DA aguda69. Ao início da doença aguda, as citocinas Th2 e Th22, tais como IL-4, IL-13 e IL-22, de modo sinérgico com a IL-17 de Th17, contribuem para a inibiçao da diferenciaçao epidérmica de produtos génicos (tais como, filagrina [FLG], loricrina e corneodesmosina)70.
O aumento abrupto de IL-31 induz prurido grave, para além dos seus efeitos inibitórios na diferenciaçao epidérmica, seguido da açao de um arranhao por coçadura que agrava a deficiência da barreira71. A IL-22 também contribui para a hiperplasia epidérmica e impulsiona o aumento de alguns peptídeos antimicrobianos (AMPs), tais como S100 e proteínas de beta-defensina humana (hBD), juntamente com IL-1772.
Embora a DA seja conhecida como uma doença inflamatória da pele mediada por linfócitos Th2 e Th22, enquanto a psoríase é conhecida como mediada por células Th1 e Th17, pode haver outros subtipos de DA. De fato, a expressao de IL-17 foi relatada em modelos de eczema murinos. Análise transcriptômica comparativa de DA e psoríase revelou evidência de aumento da expressao de genes de IL-17 e de inflamaçao neutrofílica partilhada nestas duas doenças de pele70.
Na fase crônica da DA, predomina a resposta de tipo Th1. As células Th1 polarizadas produzem IFN-γ, que confere proteçao contra agentes patogênicos intracelulares ativando células fagocíticas. IL-12 e IFN-γ desempenham papéis centrais na diferenciaçao Th1 via STAT4 e STAT1, respectivamente. STAT4 e STAT1 ativados promovem a expressao de T-bet, um regulador da diferenciaçao de células Th173. O IFN-γ está envolvido na manutençao da funçao barreira da pele, induz a expressao regulada de hBD-2/3 e da quimiocina CCL20 em queratinócitos em cultura, sugerindo seu papel na maturaçao/diferenciaçao de queratinócitos e, portanto, na regulaçao da funçao barreira.
Foi demonstrada a reduçao do espessamento da camada dérmica na pele sensibilizada de ratos IFN-γ -/-, indicando que o IFN-γ pode estar envolvido na hipertrofia da pele na DA74. Além disso, o IFN-γ aumenta a síntese de ceramida pela ativaçao da expressao da esfingomielina fosfodiesterase e da β-glucocerebrosidase e, consequentemente, reforça o envelope lipídico assim como suprime a TEWL74. No entanto, a produçao predominante e persistente de IFN-γ nas lesoes cutâneas da DA resulta na funçao modificada dos queratinócitos. Na presença de IFN-γ, os queratinócitos tornam-se mais sensíveis aos sinais de ligaçao de CD40 ou fator de necrose tumoral (TNF), que por sua vez induz o processo inflamatório75. A superproduçao de IFN-γ também resulta em apoptose de queratinócitos pela induçao da expressao de FasL, causando disfunçao da barreira cutânea e formaçao de espongiose75.
Fatores desencadeantes
Agentes infecciosos
Nos pacientes com DA as infecçoes representam a principal complicaçao, com frequência maior do que na populaçao geral. Na pele do paciente com DA há suscetibilidade a infecçoes e também a colonizaçoes por microrganismos que agravam a doença. Inúmeros fatores estao associados, entre eles as alteraçoes do pH da pele, a deficiência de peptídeos antimicrobianos que normalmente sao sintetizados na epiderme e sao um componente do sistema imunológico inato necessário ao funcionamento rápido e efetivo da defesa do hospedeiro contra bactérias, fungos e vírus. Além disso, alguns agentes atuam como superantígenos desencadeando doença grave, causam falha terapêutica e promovem complicaçoes.
Staphylococcus aureus
O S. aureus coloniza entre 5% e 30% da populaçao geral e mais de 90% dos pacientes com DA, e podem exacerbar ou manter a doença. Além disso, tem sido isolado na pele nao lesada, especialmente nas áreas intertriginosas e vestíbulo nasal. Recentemente, demonstrou-se que entre 50% e 60% dos S. aureus que colonizam a pele do paciente com DA sao produtores de toxinas, e o aumento da frequência de colonizaçao está relacionado à gravidade da doença. Um estudo demonstrou que a presença de S. aureus ocorre em 70% das lesoes ativas, mesmo sem infecçao aparente, e na pele sem lesoes 39% apresentavam a colonizaçao76. Sinais clínicos de aumento da exsudaçao, fissuras periauriculares, pústulas superficiais e crostas melicéricas (Figura 2), sao indicadores clínicos de DA infectada77,78.
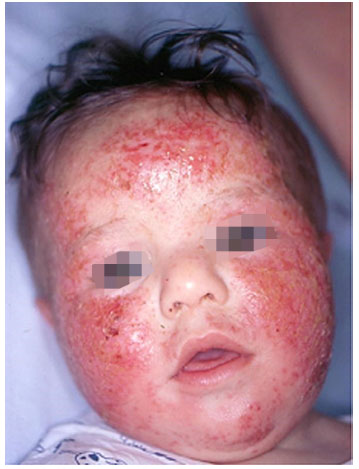
Figura 2 Paciente com dermatite atópica com exsudaçao e crostas melicéricas na face característica de infecçao secundária
O ato de coçar facilita a colonizaçao bacteriana por provocar soluçao de continuidade na barreira cutânea e expor a laminina e a fibronectina. Estas vao fixar as adesinas, que sao receptores localizados na parede bacteriana, promovendo maior aderência.
Os S. aureus produzem hemolisinas (α-toxina e δ-toxinas), leucocidina panton-valentine, toxinas esfoliativas, enterotoxinas e superantígenos (toxina 1 da síndrome do choque tóxico e enterotoxina B estafilocócica) na superfície da pele, atuando na piora ou mesmo na manutençao da doença. Os superantígenos têm a capacidade de penetrar na pele, ligando-se a receptores do complexo principal de histocompatibilidade humana (MHC) e provocando a ativaçao policlonal de linfócitos T, com consequente liberaçao de citocinas. Induzem a diferenciaçao dos linfócitos em Th2, aumentando a secreçao da IL-31, que atua intensificando o prurido e controlando a expressao da filagrina79. Atuam, também, diretamente nos queratinócitos, levando à induçao da expressao de moléculas de adesao e liberaçao do TNF-α78,80.
Os S.aureus também atuam como superantígenos, ou seja, desencadeiam uma resposta IgE específica. Muitos pacientes com DA apresentam IgE específica contra as toxinas estafilocócicas presentes na pele. A síntese de IgE contra estas toxinas bacterianas está relacionada à gravidade da DA81.
Os S. aureus também aumentam os receptores β nao funcionantes, induzem apoptose de células e podem inibir a açao dos corticosteroides82. Por esta razao, a colonizaçao bacteriana e a liberaçao de enterotoxinas podem interferir na resposta de alguns pacientes com DA aos corticosteroides e contribuírem para a falha terapêutica83.
A reduçao da colonizaçao por S. aureus, principalmente nas narinas e regioes flexurais, demonstrou benefícios em alguns pacientes, provavelmente relacionado à perda da açao do estafilococo como um superantígeno78.
Fungos
Os fungos também atuam como fatores desencadeantes de DA, principalmente os do gênero Malassezia. Embora sua açao ainda nao esteja bem esclarecida, há relatos de casos em que essa relaçao é evidente, sobretudo com formas de DA de difícil tratamento, principalmente na presença de lesoes na face e regiao cervical, em que há maior concentraçao do fungo84, e nos adolescentes, faixa etária em que inicia a secreçao de ácidos graxos pela pele, o que propicia o desenvolvimento deste micro-organismo85.
Estudos recentes tentam explicar essa relaçao com a Malassezia spp., e alguns demonstraram que este agente pode produzir proteínas que sao imunogênicas, o que desencadeia a produçao de IgE e podem, até mesmo, induzir a liberaçao de citocinas inflamatórias86.
Os fungos do gênero Malassezia pertencem à microbiota habitual da pele, mas podem causar dermatoses como a pitiríase versicolor e a foliculite por Malassezia, e contribuir com a dermatite seborreica. Por ser lipofílico, é mais frequentemente encontrado nas áreas com maior concentraçao de glândulas sebáceas, entretanto também pode estar presente em outras áreas, como membros superiores, membros inferiores e regiao genital. Emolientes e loçoes que alterem o conteúdo lipídico da pele podem alterar a quantidade e o tipo de Malassezia presente na pele87. Demonstrou-se ainda que as diferentes espécies de Malassezia apresentam preferência por diferentes localizaçoes na superfície corporal, com correlaçao com a gravidade da DA87,88.
A IgE específica à Malassezia pode ser encontrada em indivíduos saudáveis, contudo, este agente normalmente nao sensibiliza estes indivíduos. Em pacientes com DA observa-se com maior frequência e quantidade os anticorpos contra a Malassezia, além disso, o teste cutâneo de hipersensibilidade imediata com extratos de Malassezia em pacientes com DA demonstra positividade de 30% a 80%. O teste ainda nao está padronizado, sendo difícil realizar uma comparaçao adequada. A pesquisa de anticorpos anti-Malassezia spp. e mais recentemente a introduçao da pesquisa de anticorpos contra várias espécies do fungo aparentemente aumentaram a sensibilidade, sendo observado IgE em 5% a 27% das crianças e 29% a 65% dos adultos com DA. Outro aspecto observado é que a sensibilizaçao ocorre com maior frequência em pacientes com DA com lesoes localizadas na regiao cefálica e no pescoço86.
A sensibilizaçao por Malassezia apresentou correlaçao com a gravidade da doença em adultos. IgE sérica específica positiva para Malassezia foi observada em 92% dos pacientes com DA grave e em 83% dos pacientes com DA moderada, porém isto nao foi observado em crianças até o momento89. Estudo in vitro demonstrou que o aumento do pH cutâneo ocasiona maior produçao de substâncias alergênicas pela Malassezia86.
Desde modo, demonstra-se que o fungo tem participaçao na doença, principalmente em adultos sensibilizados, mas até o momento nao se elucidou a sua correlaçao com a doença nas crianças.
Alérgenos alimentares
A associaçao entre DA e alergia alimentar (AA) tem sido observada há décadas, mas até hoje o tema é motivo de discussao. Observa-se discordância entre a taxa de positividade encontrada em exames, a história clínica e o resultado obtido com a retirada do alimento suspeito. Estudos atuais apontam evidências positivas a favor da associaçao, dentre estas o conhecimento de que as alteraçoes existentes na barreira cutânea facilitam a penetraçao de alérgenos, inclusive os alimentares, e os que mostram a prevalência de alergia alimentar em cerca de 30% de crianças com DA moderada e grave, principalmente lactentes, e que nao respondem ao tratamento habitual90-92. Os principais alérgenos envolvidos para a maioria dos pacientes sao clara de ovo, leite de vaca e trigo, e, segundo alguns autores, a clara de ovo é o alimento mais implicado como desencadeante de DA. Entretanto, estes dados nao podem ser generalizados para outras faixas etárias, em que o alimento nao é apontado como um desencadeante importante da DA59.
Nos casos de suspeita de DA desencadeada por alimentos, é de fundamental importância a comprovaçao diagnóstica pelo teste de provocaçao duplo cego controlado por placebo. As Diretrizes NIAD (The National Institute of Allergy and Infectious Diseases) definem duas indicaçoes para a realizaçao de testes para identificar possível AA em menores de cinco anos com DA moderada-grave: DA persistente ou história confiável de reaçao imediata após ingestao de um alimento específico93.
A limitaçao da aplicabilidade dos desencadeamentos orais na prática clínica diária, impoe a necessidade de outros métodos de pesquisas de IgE sérica específica que permitam ao médico continuar a investigaçao. Neste sentido, os testes cutâneos de leitura imediata (puntura) ou a pesquisa de IgE sérica especifica in vitro, continuam recomendados e utilizados, tendo alto valor preditivo negativo. Quando positivos mostram apenas sensibilizaçao e nao necessariamente diagnóstico clínico de AA, devendo ser analisados de forma associada com história clinica confiável de relaçao causa e efeito, confirmados com o teste de exclusao e reintroduçao do alimento suspeito e, sempre que possível pelo teste de provocaçao oral duplo cego controlado por placebo. Testes intradérmicos para alimentos nao sao recomendados. O teste de contato para atopia (atopy patch test, APT) tem sido proposto nos últimos anos como um teste adicional para a detecçao de alergia alimentar nos pacientes com DA, mas ainda necessita de padronizaçao94.
Aeroalérgenos
As observaçoes clínicas e os estudos experimentais indicam que os aeroalérgenos sao fatores desencadeantes relevantes em pacientes com DA95. Em uma porcentagem elevada de pacientes com DA, o APT com ácaros é positivo (30 a 50%)96. O mecanismo imunológico na etiologia da DA apresenta diferenças significativas em relaçao às outras doenças alérgicas. A inalaçao de alérgenos exacerba as lesoes da DA, e as queixas dos pacientes com DA diminuem nos ambientes em que haja reduçao do nível de ácaros da poeira, revelando a importância dos alérgenos inalantes97.
Os aeroalérgenos mais comumente relacionados à DA sao derivados de ácaros da espécie Dermatophagoides pteronyssinus e D. farinae. Também a exposiçao ao mofo em ambiente úmido foi associada a aumento do risco de eczema98,99.
Estudo em crianças entre 2 e 15 anos de idade com DA verificou que os com reatividade intensa aos ácaros em teste cutâneo de leitura imediata (TCLI) apresentavam maior SCORAD (Scoring atopic dermatitis) e embora nao houvesse correlaçao significante entre os parâmetros de APT e SCORAD, os pacientes com teste de contato positivo aos ácaros apresentaram, em geral, maiores parâmetros de SCORAD100. Outro estudo avaliou anticorpos IgE para alérgenos alimentares e inalantes em crianças com DA ativa, com e sem história de sibilância, sendo observado que enquanto os anticorpos IgE para alimentos persistiram com uma prevalência e título semelhantes ao longo da infância, os anticorpos IgE contra todos os aeroalérgenos aumentaram bruscamente na adolescência101.
Como ainda nao há um procedimento padrao viável para a provocaçao de eczema mediado por aeroalérgenos na DA, estratégias específicas para diminuir o contato com aeroalérgenos devem ser consideradas em pacientes altamente sensíveis com sintomas crônicos moderados a graves da doença102.
Autoantígenos
A ideia de que um mecanismo de autoimunidade poderia desempenhar papel na fisiopatologia da DA é apoiada na observaçao de que esses pacientes exibem reatividade de IgE a uma variedade de antígenos proteicos humanos, vários deles caracterizados do ponto de vista molecular103. A autorreatividade mediada por IgE foi implicada como um fator na imunopatogênese da DA. Análises moleculares de alérgenos têm revelado similaridades entre antígenos ambientais e proteínas humanas, sugerindo a possibilidade de reaçao de autoimunidade104. A exposiçao de indivíduos alérgicos a alérgenos exógenos leva à inflamaçao de tipo imediato causada pela degranulaçao de mastócitos por complexos imunes IgE-alérgenos e liberaçao de mediadores inflamatórios, proteases e citocinas pró-inflamatórias. No entanto, inflamaçao alérgica pode ocorrer e persistir na ausência de exposiçao a alérgenos exógenos, e pode, paradoxalmente, se assemelhar à resposta Th1 mediada por reaçao inflamatória crônica.
O reconhecimento de autoantígenos pela IgE específica pode aumentar a inflamaçao alérgica na ausência de exposiçao alergênica exógena. Além disso, os autoantígenos que ativam as respostas imunes Th1 poderiam contribuir para a inflamaçao crônica na alergia, ligando assim a alergia à autoimunidade104. Estes autoantigênos foram denominados Hom s 1 a Hom s 5 e representam proteínas intracelulares que sao expressas em diferentes tipos de células e tecidos. Verificou-se que Hom s 1 era idêntico a um antigêno tumoral previamente identificado que induz respostas fortes de células T citotóxicas105.
Fatores neuro-psico-imunológicos
A DA piora com alguns fatores externos tais como: estímulos emocionais, físicos, químicos e biológicos, que provocam uma resposta mais acentuada nestes pacientes. Em até 70% dos pacientes com DA existe uma associaçao comprovada com estresse106. Demonstrou-se que o sistema neuroendócrino se apresenta aumentado na pele dos pacientes com DA, onde a ligaçao das células endócrinas com a inervaçao da pele está mais desenvolvida e apresenta maior penetraçao na epiderme. Esta inervaçao na DA, pode desregular a produçao de citocinas e outros fatores que resultam na reduçao da defesa do hospedeiro. Níveis plasmáticos elevados de fator de crescimento neural (NGF), do peptídeo relacionado ao gene da calcitonina (CGRP) e da substância P (SP) podem ser observados em pacientes com DA e se relacionam positivamente com a atividade da doença. Em estudos em animais, a aplicaçao de anticorpos anti-NGF reduziu o prurido e as lesoes cutâneas, reduzindo também a inervaçao observada na pele. Os inibidores de calcineurina e mesmo a fototerapia promovem a mesma reduçao107.
Ainda na pele, a filagrina é um dos mais importantes hidratantes naturais no estrato córneo, e alteraçoes no gene de síntese da filagrina estao presentes em até 50% dos pacientes com DA. Além disso, demonstrou-se que o nível de percepçao do prurido pela aplicaçao de corrente elétrica varia de acordo com a xerose determinada pelas alteraçoes da filagrina. Deste modo, a interaçao entre a alteraçao da filagrina e o sistema neuroendócrino na pele ocasiona uma piora da sensaçao de prurido ao menor estímulo107. Assim, na DA existe uma complexa interaçao entre disfunçao da barreira cutânea, alteraçoes neuroendócrinas, imunológicas e alérgicas associadas a alteraçoes na percepçao do prurido107.
QUADRO CLINICO
A apresentaçao clínica da DA varia desde formas localizadas até as disseminadas. Sao características clínicas, prurido, lesoes crônicas ou recidivantes, com distribuiçao e morfologia variável conforme a idade. A lesao clássica é o eczema, definido como uma inflamaçao cutânea, com os seguintes achados clínicos: eritema, pápula, seropápula, vesículas, escamas, crostas e liquenificaçao e achados histológicos inespecíficos, como espongiose, acantose, paraqueratose, infiltrado linfocitário e exocitose. As características clínicas variam de acordo com a faixa etária do paciente, porém um considerável número de pacientes apresenta lesoes características simultâneas de mais de uma faixa etária108,109.
Fase infantil
Do nascimento até o sexto mês de vida é caracterizada por prurido intenso e lesoes cutâneas com eritema, pápulas, vesículas e formaçao de crostas, que se localizam na face e poupam o maciço central (Figura 3). Outros locais como face extensora dos membros e tronco podem ser acometidos. Infecçao secundária é comum e caracterizada por exsudaçao e crostas melicéricas. Os surtos do eczema podem ser desencadeados por infecçoes respiratórias, alteraçoes climáticas, fatores emocionais e alimentos. Entre os 8 e 10 meses de idade as lesoes acometem as regioes extensoras dos membros, provavelmente pela fricçao ocasionada pelo ato de engatinhar ou mesmo se arrastar no chao. Os pacientes que nesta fase apresentam eczema generalizado podem melhorar; entretanto, o desaparecimento total da doença é pouco provável. Nao é incomum a presença de dermatite seborreica, sobretudo nos primeiros meses de vida, a associaçao de prurido e escamas típicas de dermatite seborreica no couro cabeludo sao sugestivas da combinaçao das duas doenças108,110.
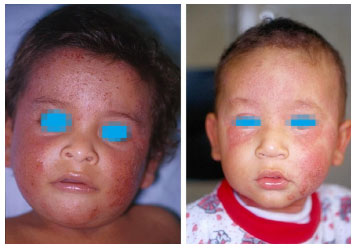
Figura 3 Pacientes com dermatite atópica na fase infantil, lesoes eritematosas com pápulas, vesículas e crostas na face, poupando o maciço central
Fase pré-puberal
Ocorre a partir dos 2 anos e persiste até a puberdade. As lesoes localizam-se principalmente nas regioes flexurais (Figura 4) dos joelhos e dos cotovelos, pescoço, pulsos e tornozelos. As pápulas eritematosas e vesículas sao substituídas gradualmente por liquenificaçao (espessamento, escurecimento e acentuaçao dos sulcos da pele). O prurido está sempre presente e pode ser de difícil controle. É importante salientar que 60% dos pacientes apresentam melhora importante ou desaparecimento total das lesoes nesta fase da doença108,109.

Figura 4 Dermatite atópica com lesoes eczematosas com liquenificaçao em regioes flexurais cubital e poplítea, típicos da fase pré-puberal
Fase adulta
A fase adulta da DA é semelhante à fase pré-puberal, mas as lesoes sao mais liquenificadas (Figura 5), principalmente em regioes flexurais e nas maos. A face (Figura 6) e as maos frequentemente sao as regioes mais acometidas nesta faixa etária. Lesoes localizadas nos mamilos podem ocorrer com frequência nas mulheres e adolescentes jovens. Pacientes com eritrodermia ou lesoes generalizadas nao sao raros nesta fase109.
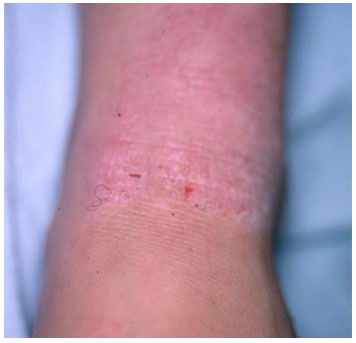
Figura 5 Dermatite atópica na fase adulta no tornozelo com intensificaçao da liquenificaçao
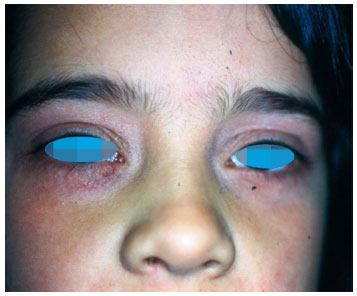
Figura 6 Dermatite atópica na fase adulta. Placa eritematosa liquenificada na regiao periocular
Os pacientes que na infância apresentaram formas graves da doença e alteraçoes psicológicas importantes têm maior chance de persistência da doença na idade adulta. Este aspecto é importante, pois chama à atençao para a necessidade de maior controle do quadro emocional nas crianças atópicas108,109.
Sinais cutâneos associados à dermatite atópica
Além das lesoes clássicas eczematosas há diversos outros sinais frequentes nos pacientes com DA. Os mais importantes sao:
Dupla prega ou prega infra-orbital de Dennie-Morgan – é comum em qualquer pessoa a presença de uma prega nas pálpebras inferiores. No atópico, provavelmente devido à inflamaçao e coçadura constantes, surgem duas ou até três pregas, denominadas de Dennie-Morgan (Figura 7). Acredita-se que apareça em aproximadamente 60% dos pacientes com DA. Atualmente nao sao consideradas patognomônicas de DA, mas fazem parte dos critérios diagnósticos menores111.
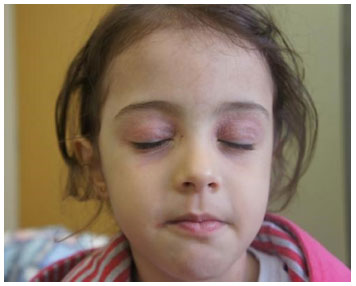
Figura 7 Segunda prega infrapalpebral de Dennie-Morgan. Também é possível observar o afinamento distal das sobrancelhas
Sinal de Hertoghe – também é decorrente da coçadura constante, a porçao distal lateral dos supercílios pode ter diminuiçao de pelos (Figura 7), o que caracteriza este sinal que é observado em menos da metade dos pacientes111.
Asteatose ou Xerose (Pele seca) - praticamente todos os pacientes com DA apresentam a pele ressecada, que é um dos principais sinais observados na doença. A simples presença da xerose desencadeia o prurido. A pele seca é decorrente de defeitos da barreira cutânea e acarreta aumento da TEWL e aumento da permeabilidade cutânea a fatores irritativos e alérgicos.
Pitiríase alba – é comum em crianças e decorre do ressecamento da pele. Nos pacientes atópicos estima-se estar presente em 40 a 60% dos casos, e é caracterizada por manchas hipocrômicas com bordas mal definidas, discretamente ásperas, localizadas principalmente na face, nos membros superiores e inferiores (Figura 8), e menos frequente no tronco. Em casos de dúvida diagnóstica, o exame micológico direto diferencia de pitiríase versicolor. Outro diagnóstico diferencial importante no nosso meio é a hanseníase indeterminada, para a qual devemos realizar a pesquisa de sensibilidade e a prova da histamina102.
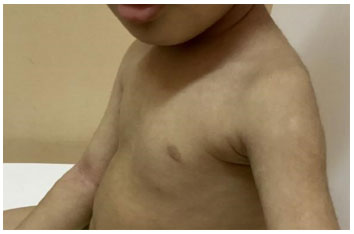
Figura 8 Manchas hipocrômicas da pitiríase alba no braço
Dermatite crônica inespecífica de pés e maos - sao consequentes ao ressecamento e irritaçao destas regioes. Devem ser diferenciados da dermatite alérgica de contato, através do teste de contato, da tinha da mao (micológico direto) e da psoríase (anatomopatológico). Clinicamente há descamaçao e eritema nas palmas e plantas, algumas vezes com fissuras (Figura 9). Quando atingem somente a ponta dos dedos, é denominada de pulpite digital (Figura 10)112.
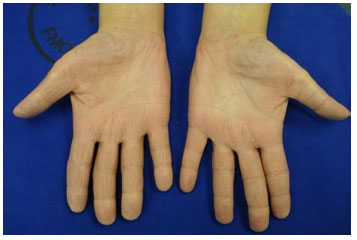
Figura 9 Dermatite crônica de maos: eritema e hiperlinearidade
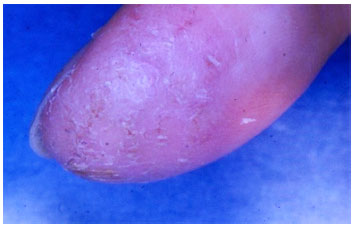
Figura 10 Descamaçao intensa no polegar (fingertips)
Hiperlinearidade palmo-plantar – presença de acentuaçao das linhas palmares e plantares com menos descamaçao111 (Figura 11).
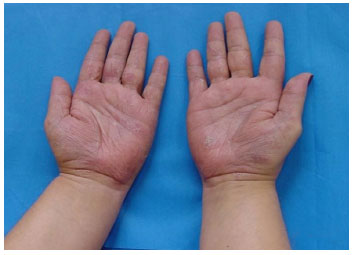
Figura 11 Acentuaçao das linhas das palmas, hiperlinearidade palmar associada a descamaçao
Ceratose pilar (Keratosis pilaris) – cerca de 30% das crianças e adolescentes com DA apresentam lesoes ceratósicas foliculares nos braços, regiao malar e coxas. Estas tendem a desaparecer ou melhorar na idade adulta. Esta manifestaçao clínica também aparece em nao atópicos112.
Eczema palpebral – lesoes eritematosas, descamativas e infiltradas nas pálpebras podem ser devido a dermatite alérgica de contato, mas também sao muito comuns na DA (Figuras 6 e 7)111.
Escurecimento periorbital – decorre do atrito pela coçadura; muitos pacientes apresentam aumento da pigmentaçao periorbital, que é considerado sinal menor da DA111,112.
Eczema de mamilos – mais frequente em meninas, principalmente pelo maior atrito da regiao com roupas que causam irritaçao ou alergia. O diagnóstico diferencial é importante, principalmente quando unilaterais, com doença de Paget, que deve ser afastada pela realizaçao do exame anatomopatológico. Também devemos excluir a possibilidade de dermatite de contato.
Fissuras ou rágades – mais comumente nas regioes infra-auriculares, infranasal e retroauriculares, estas lesoes sao resultado da xerose e coçadura111.
Queilites – mais acentuada no lábio inferior, pelo ato de lamber os mesmos ou mordê-los. A alteraçao inicial é o ressecamento, e o paciente, na tentativa de umedecer, acaba piorando pela açao da saliva111.
Palidez facial – mais da metade dos pacientes apresenta-se com palidez facial no centro da face, decorrente de vasoconstricçao periférica111.
Ictiose vulgar – é genodermatose de amplo espectro, mas cerca de 20 a 30% dos pacientes com DA apresentam escamas aderentes poligonais, sobretudo localizadas nos membros inferiores (Figura 12), mas podem acometer todo o tegumento e poupam as fossas cubitais e poplíteas. É considerada a forma mais simples de ictiose, e é associada às mutaçoes do gene da filagrina113.
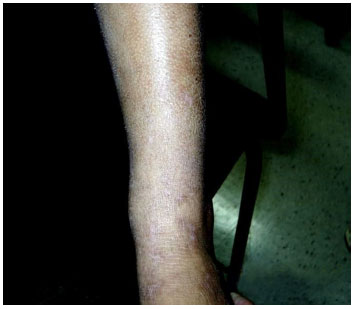
Figura 12 Escamas aderentes poligonais e escurecidas da ictiose vulgar
Dermografismo branco – ao atritar a pele, a resposta fisiológica normal é de vasodilataçao com aparecimento de edema. No atópico ocorre o inverso, quadro conhecido com dermografismo branco (Figura 13)111.
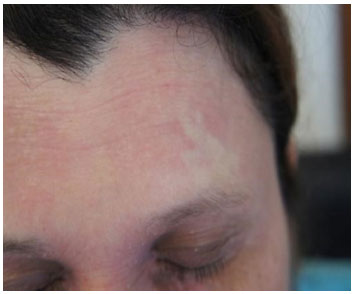
Figura 13 Dermografismo branco
Alguns destes sinais, como a xerose, ictiose, dermatite crônica de maos, e eczema de mamilos sao considerados critérios menores de Hanifin e Rajka114, sendo considerados importantes para o diagnóstico da DA.
DIAGNOSTICO
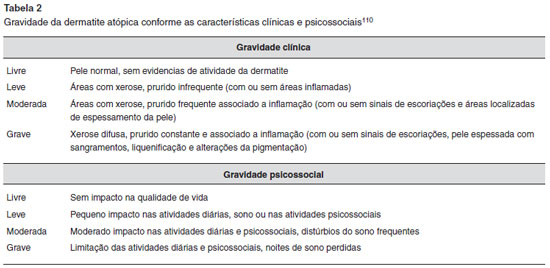
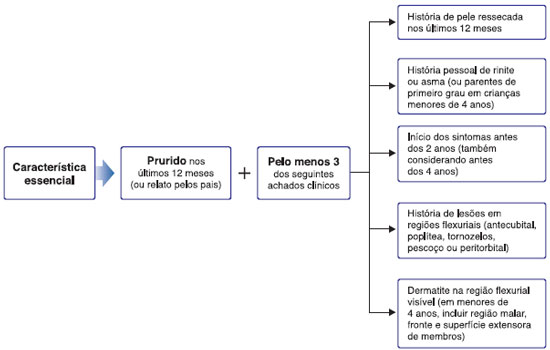
O diagnóstico de DA é essencialmente clínico. O principal sintoma da doença é o prurido que associado às características clínicas descritas na Figura 14, determinam o diagnóstico. A cronicidade, as recidivas, o aspecto de distribuiçao das lesoes conforme a idade e o comprometimento da qualidade de vida do paciente sao importantes tanto para o diagnóstico quanto para a classificaçao da gravidade da doença, que apresenta vários métodos de classificaçao, sendo um dos mais representativos exposto na Tabela 2 e Figura 15108,110.
O prurido causa distúrbios de sono e irritabilidade, e pode ser agravado por vários fatores, como calor, suor, banhos, atividades físicas, mudanças de temperatura ambiente, alteraçoes de humor ou atividades que ocasionem estresse na criança, e uso de roupas de la ou sintéticas108,110.
O diagnóstico de DA é clínico e baseado na história completa e detalhada e nos sinais observados no exame físico. A biópsia cutânea é de pouca utilidade, e realizada eventualmente se houver dúvida diagnóstica. As caraterísticas observadas sao espongiose, formaçao de vesículas, exocitose de linfócitos, paraceratose, e, eventualmente, acantose. A derme apresenta infiltrado linfocitário, e a eosinofilia tissular é variável108.
Diagnóstico diferencial
Várias dermatoses apresentam semelhanças com a DA, sobretudo aquelas caracterizadas por lesoes eritêmato-descamativas e associadas a prurido. Na Tabela 3 sao apresentados os principais diagnósticos diferenciais, e os mais frequentes sao mencionados a seguir108,110.
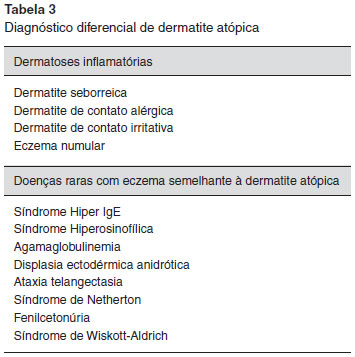
Dermatite seborreica: acomete lactentes e adultos, pela maior produçao sebácea nestas faixas etárias. A distribuiçao das lesoes difere da DA por acometer regiao inguinal, axilas, pescoço e couro cabeludo. A idade de início é mais precoce, nos primeiros meses de vida. É pouco pruriginosa, e nao gera dificuldade para o sono ao lactente como ocorre na DA. A associaçao com DA dificulta a diferenciaçao inicial, mas a evoluçao da dermatite seborreica que melhora depois do primeiro ano de vida permite a distinçao.
Eczema numular: pode estar associado à DA ou mesmo isolado, e se caracteriza por áreas circulares, em formato de moeda, com tamanho de 1 a 5 cm de diâmetro, presentes nos membros, principalmente nas regioes extensoras e nao raras vezes associadas a processos infecciosos ocasionados por S. aureus e xerose próximas as lesoes.
Dermatite de contato alérgica (DCA) ou dermatite de contato irritativa (DCI): as lesoes sao muito semelhantes àquelas da DA, mas a localizaçao, formato e história de contato com o agente causal permitem o diagnóstico. A DCI é ocasionada por irritantes primários, como sabonetes ou detergentes, enquanto a DCA por sensibilizaçao mediada por linfócitos T, sendo o níquel, presente em bijuterias e objetos de metal, o mais frequente. É importante salientar que crianças com DA podem apresentar associaçao com dermatite de contato, sobretudo quando ocorrem lesoes resistentes ao tratamento, localizadas nas maos e pés, regiao periocular e perioral. A anamnese acurada ajudará a descobrir possíveis agentes causais, e nos casos de DCA, a realizaçao do teste de contato (patch test) é útil na identificaçao do alérgeno envolvido.
CRITÉRIOS DE GRAVIDADE
A aferiçao da atividade da DA é realizada de forma mais adequada por meio de escores que avaliem tanto os sintomas subjetivos quanto os objetivos. No entanto, a piora isolada destes escores nao deve definir um surto agudo, que é definido como a piora clínica de sinais e sintomas de DA que necessitem de intervençao terapêutica102.
A apresentaçao clínica da DA varia de formas leves e localizadas até formas graves e disseminadas. As formas graves necessitam de tratamento intensivo e reavaliaçoes seriadas, em períodos curtos de tempo, para evitar ou tratar precocemente os surtos. A fim de determinar o tratamento, predizer a frequência das reavaliaçoes e mesmo quantificar a melhora ou piora clínica a cada avaliaçao, notou-se a necessidade da uniformizaçao de critérios102.
Assim, desenvolveu-se um escore para avaliaçao da gravidade da DA, denominado Scoring Atopic Dermatitis (SCORAD)117, que permite o acompanhamento, de forma padronizada, de pacientes com DA, assim como tem utilidade nos estudos clínicos102.
O índice SCORAD considera a extensao da doença, a gravidade da lesao e a presença de sintomas subjetivos, como prurido e a perda de sono. A extensao das lesoes é indicada pela letra A, está de acordo com a regra dos nove e corresponde a 20% da pontuaçao. A gravidade das lesoes é representada pela letra B, corresponde a 60% da pontuaçao e é composta por seis itens avaliados em uma lesao ativa (eritema, pápulas, escoriaçao, exsudaçao ou formaçao de crostas, liquenificaçao e xerose), cada item pontua de 0 a 3. Os sintomas subjetivos, como prurido durante o dia e despertares noturnos, sao avaliados de 0 a 10 por meio de uma escala analógica visual, indicados pela letra C, e somam 20% da pontuaçao118.
A pontuaçao obtida é entao inserida em uma fórmula (A/5 + 7B/2 + C) que fornece a pontuaçao que pode variar de 0 a 103. A doença é classificada como leve (pontuaçao menor do que 25), moderada (pontuaçao entre 25 e 50) ou grave (pontuaçao maior 50)102.
A Figura 16 ilustra um paciente de 5 anos, com diagnóstico de DA desde os três anos. Na avaliaçao clínica apresentava lesoes nos punhos e fossa poplítea e havia xerodermia discreta. Os pais relatam prurido discreto nos últimos 2 dias (corresponde ao valor 2 na escala visual) e o distúrbio do sono foi pontuado como 2 na escala visual. O valor do cálculo do SCORAD para este paciente foi 12, o que corresponde a DA leve.
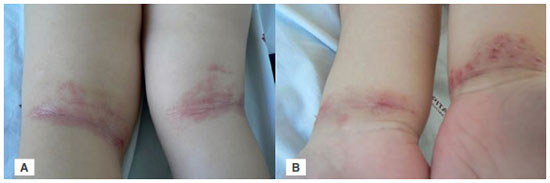
Figura 16 Lesoes eritematosas, com pápulas, escoriaçao leve e crostas hemáticas acometendo regiao poplítea bilateral (A) e punhos (B), classificado como leve pelo SCORAD
O SCORAD pode ser concluído dentro de sete a dez minutos, dependendo da experiência dos investigadores119. Existem aplicativos para celular de fácil utilizaçao para cálculo da gravidade, assim como uma versao que orienta o paciente - patient-oriented SCORAD (PO-SCORAD) desenvolvida para ser realizada pelo próprio paciente ou seus cuidadores, pois fornece orientaçao visual para a pontuaçao. As duas escalas SCORAD e PO SCORAD já demonstraram ter coeficiente de correlaçao com confiabilidade geral boa, intra-avaliador e entre avaliadores120.
Outro escore de gravidade utilizado é o índice EASI (Eczema Score and Severity Index). Este elimina os sintomas subjetivos e permite melhor avaliaçao da gravidade de cada lesao. Em cada regiao do corpo (cabeça e pescoço, membros superiores, membros inferiores e tronco) é definida a extensao, que pode variar de 0 a 100%. Depois, uma lesao em cada área é avaliada em uma escala de 0 a 3 para eritema, edema ou pápulas, escoriaçao e liquenificaçao. A somatória resulta em uma pontuaçao que classifica a doença em: muito leve (0,1 a 1); leve (1,1 a 7); moderada (7,1 a 20); grave (21,1 a 50); ou muito grave (50,1 a 72). Esse escore também se encontra disponível em aplicativo para celular denominado de EASI calculator.
Uma revisao sistemática concluiu que o índice EASI e o SCORAD sao os melhores instrumentos para avaliar os sinais clínicos da DA. Os outros demais 14 instrumentos avaliados no estudo nao foram recomendados por apresentarem propriedades de mediçao pouco claras, ou inadequadas121.
AVALIAÇAO LABORATORIAL
A avaliaçao laboratorial fornece subsídios à identificaçao dos agentes provocadores de DA, essencial na elaboraçao do plano de tratamento e orientaçao do paciente na prevençao ao contato com alérgenos e outros fatores desencadeantes. Entre elas, destacam-se:
Contagem de eosinófilos no sangue periférico e níveis séricos de IgE total
A presença de eosinofilia e de níveis elevados de IgE sérica sao frequentes em pacientes com DA. Entretanto, cerca de 20% deles nao apresentam alteraçoes nos níveis de IgE122, e elevaçao do número de eosinófilos e de IgE sérica podem estar presentes em outras situaçoes clínicas, tais como parasitoses, reaçoes a drogas e doenças infecciosas, caracterizando-se assim, como um dado laboratorial sem especificidade para DA.
A eosinofilia tecidual está associada ao aumento dos níveis de eosinófilos no sangue, e correlacionase com a gravidade da doença. Eosinófilos ativados depositam grânulos de proteínas extracelulares na pele. O papel dos eosinófilos na fisiopatologia da DA permanece incerto123.
Coorte de nascimento alema em que ao menos um dos pais era atópico realizou a contagem de eosinófilos no sangue periférico de 599 lactentes com quatro semanas de vida e de 467 aos sete meses de vida. A presença de eosinofilia (eosinófilos séricos igual ou superior a 5% dos leucócitos) aos 4 meses de idade foi fator de risco para o desenvolvimento de DA até os 3 anos de vida124.
Da mesma forma, a IgE sérica total tem papel controverso na fisiopatologia da DA, e a sua quantificaçao tem valor limitado para o diagnóstico. Embora valores altos sugiram a possibilidade de sensibilizaçao alérgica, valores normais nao afastam alergia125. A maioria dos pacientes com DA têm níveis elevados de IgE sérica total, que, segundo alguns autores, estao relacionados à maior gravidade da doença126, e, segundo outros, nao127. Níveis séricos de IgE total sao mais aumentados em pacientes com mutaçoes do gene da filagrina128. Um subgrupo de crianças, assim como a maioria dos pacientes com idade de início tardio da doença (cerca de 30% de dos pacientes com DA) nunca será sensibilizado, embora tenham lesoes eczematosas típicas129.
Na DA associada a níveis elevados de IgE, existe correlaçao entre os níveis de IgE total e a gravidade, mas a dosagem de IgE sérica nao é útil como biomarcador para a avaliaçao de exacerbaçoes do eczema. Além disso, a depleçao de IgE com anti-IgE nao reduz a expressao clínica da DA130. Níveis elevados de IgE no sangue de cordao umbilical podem servir como um indicador para DA aos 6 meses de idade131,132.
Testes cutâneos de leitura imediata
O teste cutâneo de leitura imediata (TCLI) é método simples, fácil, rápido e barato de identificar anticorpos da classe IgE e pode ser utilizado em todos os pacientes, sem restriçao de idade133.
Os TCLI pela técnica de puntura (prick test) com aeroalérgenos e alérgenos alimentares sao normalmente utilizados como testes de primeira linha na detecçao de IgE específica para determinar o envolvimento destes agentes no desencadeamento do sintoma, devendo por suas características ser avaliado com precauçao.
A positividade a um aeroalérgeno ou a um alérgeno alimentar pode nao apresentar relevância clínica, principalmente se o paciente apresenta níveis elevados de IgE, já que nestes casos podem ocorrer reaçoes de modo nao específico. Independentemente deste fato, a presença de TCLI positivo a um determinado alimento indica apenas sensibilizaçao ao mesmo, e nao necessariamente a sua participaçao na doença em questao, pois apresenta valor preditivo positivo de apenas 50%, devendo, por isso, ser confirmado pelo teste de provocaçao oral134. Em contrapartida, se o TCLI for negativo, ele terá valor preditivo negativo de 90% e afasta a sua participaçao na gênese e/ ou agravamento da DA. Entre os aeroalérgenos mais envolvidos estao os ácaros D. pteronyssinus, D. farinae, Blomia tropicalis e B. kulagini. Entre os alérgenos alimentares merecem destaque o leite de vaca, a clara de ovo, o amendoim e a soja.
Dependendo das condiçoes da pele, uso crônico de anti-histamínicos, baixa potência dos extratos ou técnica inadequada, o TCLI nao pode ser realizado, ou pode apresentar resultados falso-negativos, necessitando assim, da realizaçao de outros testes para avaliaçao da presença de IgE específica no soro, tais como o ImmunoCAP para os alérgenos ou CRD (Component Resolved Diagnosis)133.
Determinaçao dos níveis séricos de IgE específica a alérgenos
A presença de IgE sérica específica a um determinado alérgeno documenta a sensibilizaçao alérgica ao mesmo. Em pacientes com DA, quando associada à alergia respiratória é comum encontrarmos a sensibilizaçao a aeroalérgenos (ácaros da poeira domiciliar, epitélio e descamaçoes de animais [gato, cao e outros animais de estimaçao], baratas, fungos, e mais raramente polens). Entretanto, estima-se que um terço das DA moderadas a graves sejam associadas a alergia alimentar (AA). A sensibilizaçao ao alimento habitualmente ocorre pelo trato gastrintestinal, porém a via cutânea também já foi comprovada135.
Estudos longitudinais documentam que 15% dos lactentes com DA leve a moderada desenvolveram AA136. Metanálise recente confirmou forte associaçao entre DA, sensibilizaçao para alérgenos alimentares e AA137. Quanto mais precoce o surgimento do eczema, maior a chance de desenvolver AA138.
Os alimentos mais apontados na AA, entre indivíduos com DA, têm sido: ovo, leite e amendoim122,136,138, e os dados nacionais sao escassos. O método de uso consagrado para a sua determinaçao, atualmente, é a imunofluorescência enzimática - ImmunoCAP® (Thermo Fisher Scientifics, Uppsala, Suécia). Com o avanço da tecnologia molecular, utilizando-se o mesmo método de imunofluorescência enzimática foi possível investigar a sensibilizaçao direcionada aos componentes constituintes da fonte alergênica, enfoque conhecido como CRD (sigla do inglês para Component Resolved Diagnosis, diagnóstico resolvido por componentes). Neste caso, sao utilizadas proteínas recombinantes ou purificadas. Esse método permite a identificaçao mais precisa do alérgeno envolvido, assim como a possibilidade de reatividade cruzada entre fontes alergênicas que compartilham moléculas estruturalmente semelhantes, os panalérgenos, com quantidades mínimas de soro do paciente139,140.
No Brasil, o CRD disponível comercialmente é o ImmunoCAP-ISAC® (microarray, Thermo Fisher Scientifics, Uppsala, Suécia). É um painel fixo com mais de 100 proteínas naturais, purificadas e recombinantes, de cerca de 50 fontes alergênicas, que estao acopladas em triplicata a uma superfície laminar de vidro revestida por nitrocelulose ou gel específico (plataforma ImmunoCAP ISAC®). Estudos comparando os dois métodos ImmunoCAP® e ImmunoCAP-ISAC® demonstraram boa correlaçao entre ambos141,142. O custo elevado limita o emprego do CRD de modo indiscriminado, ficando limitado aos pacientes com DA grave.
Teste de contato para atopia
O teste de contato para atopia (APT - atopy patch test) é procedimento novo para a identificaçao de alérgenos provocadores de lesoes eczematosas nos pacientes com DA. Em contraste com o TCLI, o APT permite detectar sensibilizaçao relevante na ausência de IgE específica143. A resposta positiva ao APT representa a expressao de reaçao imunológica mediada por linfócitos T ou uma reaçao de fase tardia mediada por IgE144. Podem ser utilizados alérgenos de ácaros, de animais, de fungos, de polens, e de alimentos145.
O APT consiste na aplicaçao epicutânea de alérgenos de proteína intactas, com o uso de dispositivos próprios. É necessária a padronizaçao quanto à técnica de realizaçao e tempo de oclusao. Para pesquisa de sensibilizaçao à ácaros, o material para o APT é composto de uma mistura em partes iguais de D. pteronyssinus e de D. farinae (corpo total), 20% a 30% em vaselina. Com o uso de Finn chambers, os alérgenos potenciais sao aplicados na regiao dorsal (pele sadia), permanecendo no local por 48 horas. A leitura é realizada com 48, 72 e até 96 horas após a oclusao. O controle com vaselina é também removido e lido concomitantemente146.
O APT com aeroalérgenos está melhor padronizado, ao contrário deste teste para alimentos, e existem várias dúvidas quanto ao tipo de alérgeno utilizado e quantidade do mesmo147.
Em relaçao aos alérgenos alimentares, na literatura sao empregados desde proteínas isoladas de alérgenos alimentares até alimento in natura em quantidades variáveis, o que torna difícil um consenso sobre a melhor padronizaçao para a utilizaçao deste teste com alimentos148.
O APT é recurso utilizado no diagnóstico das alergias alimentares em crianças com DA. Giusti et al. demonstraram que APT sao suficientemente reprodutíveis para serem empregados como procedimentos de investigaçao de alérgenos envolvidos na DA149.
Roehr et al. mostraram que a combinaçao de APT positivo com níveis de IgE específica para leite de vaca superiores a 0,35 kU/L ou de clara de ovo iguais ou superiores a 17,5 kU/L dispensam a provocaçao oral com os referidos alimentos150.
Visitsunthorn et al. demonstraram que a sensibilidade, especificidade, valor preditivo positivo e negativo com alérgenos liofilizados em crianças com DA leve a grave foi 40%, 90,2%, 65,2% e 76,6%, respectivamente, enquanto que para puntura foi 40%, 93,9%, 75% e 77,3%, respectivamente. Os extratos liofilizados para alimentos foram seguros e tiveram alta especificidade e valor preditivo positivo, mas baixa sensibilidade151. O APT é um exame promissor para detecçao de alérgenos que desencadeiam crises de DA, e pode ser útil nos casos de DA grave e de difícil controle, mas para indicaçao em larga escala ainda falta definiçao de padrao de antígenos e técnica a ser empregada.
Provocaçao oral com alimentos (duplo-cego, placebo controlado)
A provocaçao alimentar (duplo-cego, placebo controlado) representa o padrao ouro no diagnóstico de alergia alimentar em crianças com DA152. Depois de dieta com exclusao de alérgenos, os alimentos suspeitos ou placebo sao administrados em doses crescentes. O período de observaçao de reaçoes depende da história clínica, apontando para reaçoes IgE mediadas ou nao IgE mediadas, variando desde horas, até vários dias nos mecanismos que envolvem imunidade celular153.
Há necessidade da padronizaçao dos procedimentos utilizados nas provocaçoes orais com alimentos, para que seja possível a comparaçao dos resultados entre diferentes centros e entre diferentes populaçoes, em protocolos científicos.
A Academia Europeia de Alergia e Imunologia Clínica padronizou recentemente as provocaçoes orais com alimentos, em pacientes que apresentam reaçoes a alimentos do tipo imediatas154. As provocaçoes com alérgenos alimentares têm dois objetivos principais: identificar os alérgenos causadores para que sejam evitados; provar que os alimentos nao sao responsáveis pelos sintomas apresentados pelas crianças e que, portanto nao é necessária sua restriçao dietética.
Esforços para a padronizaçao de provocaçoes orais com alimentos sao justificáveis para prevenir dietas nao específicas que podem levar a prejuízos intensos no crescimento e no desenvolvimento das crianças.
A principal indicaçao de uma provocaçao oral é a suspeita dos pais ou do médico de que os sintomas sejam relacionados à ingestao de determinado grupo de alimentos, o que pode ser comprovado pelo teste duplo cego controlado por placebo155.
Pacientes com história de reaçoes imediatas graves e sistêmicas à ingestao de alimentos, nao devem ser desencadeados por via oral155. Quando os níveis de IgE específica forem iguais ou superiores aos previamente definidos para determinados grupos de alimentos (valores preditivos positivos superiores a 95%), o diagnóstico pode ser inferido sem a necessidade do desencadeamento, preservando o paciente de reaçoes indesejáveis155,156.
Outros exames
Outros marcadores sorológicos vêm sendo estudados no sentido de permitirem a confirmaçao do diagnóstico de alergia alimentar em pacientes com DA ou do seu acompanhamento, entretanto, poucos estao disponíveis na prática clínica. Entre eles, destacamos: a quantificaçao de histamina liberada por basófilos, a determinaçao dos níveis de anticorpos séricos IgG e IgG4 específicos, a pesquisa e a quantificaçao de complexos antígeno-anticorpo, a determinaçao da expressao de CD63 em basófilos, a determinaçao dos níveis de anticorpos IgA anti-gliadina, antitransglutaminase e anti-endomísio152,157-159.
REFERENCIAS
1. Addor FA, Aoki V. Skin barrier in atopic dermatitis. An Bras Dermatol. 2010;85(2):184-94.
2. Katayama I, Aihara M, Ohya Y, Saeki H, Shimojo N, Shoji S, Taniguchi M, YamadaH; Japanese Society of Allergology. Japanese guidelines for atopic dermatitis 2017. Allergol Int. 2017;66(2):230-47.
3. Gonzalez ME, Schaffer JV, Orlow SJ, Gao Z, Li H, Alekseyenko AV, et al. Cutaneous microbiome effects of fluticasone propionate cream and adjunctive bleach baths in childhood atopic dermatitis. J Am Acad Dermatol. 2016;75(3):481-93.
4. Williams HC. Clinical practice. Atopic dermatitis. N Engl J Med. 2005;352(22):2314-24.
5. Furue M, Chiba T, Tsuji G, Ulzii D, Kido-Nakahara M, Nakahara T, et al. Atopic dermatitis: immune deviation, barrier dysfunction, IgE autoreactivity and new therapies. Allergol Int. 2017;S1323- 8930(16)30171-X.
6. Johansson SG, Bieber T, Dahl R, Friedmann PS, Lanier BQ, Lockey RF, et al. Revised nomenclature for allergy for global use: Report of the Nomenclature Review Committee of the World Allergy Organization, October 2003. J Allergy Clin Immunol. 2004;113(5):832-6.
7. Osawa R, Akiyama M, Shimizu H. Filaggrin gene defects and the risk of developing allergic disorders. Allergol Int. 2011;60(1):1-9.
8. Deckers IA, McLean S, Linssen S, Mommers M, van Schayck CP, Sheikh A. Investigating international time trends in the incidence and prevalence of atopic eczema 1990-2010: a systematic review of epidemiological studies. PLoS One 2012;7:e39803.
9. Williams H, Stewart A, von Mutius E, Cookson W, Anderson HR, and the International Study of Asthma and Allergies in Childhood (ISAAC) Phase One and Three Study Groups. Is eczema really on the increase worldwide? J Allergy Clin Immunol. 2008;121:947-54.
10. Ballardini N, Kull I, Soderhall C, Lilja G, Wickman M, Wahlgren CF. Eczema severity in preadolescent children and its relation to sex, filaggrin mutations, asthma, rhinitis, aggravating factors and topical treatment: a report from the BAMSE birth cohort. Br J Dermatol. 2013;168:588-94.
11. Illi S, von Mutius E, Lau S, Nickel R, Grüber C, Niggemann B, et al. The natural course of atopic dermatitis from birth to age 7 years and the association with asthma. J Allergy Clin Immunol. 2004;113:925-31.
12. Peters AS, Kellberger J, Vogelberg C, Dressel H, Windstetter D, Weinmayr G, et al. Prediction of the incidence, recurrence, and persistence of atopic dermatitis in adolescence: a prospective cohort study. J Allergy Clin Immunol. 2010;126:590-95.
13. Draaisma E, Garcia-Marcos L, Mallol J, Solé D, Pérez-Fernández V, Brand PL, et al. A multinational study to compare prevalence of atopic dermatitis in the first year of life. Pediatr Allergy Immunol. 2015;26(4):359-66.
14. Solé D, Rosário Filho NA, Sarinho ES, Camelo-Nunes IC, Paes Barreto BA, Medeiros ML, et al. Prevalence of asthma and allergic diseases in adolescents: nine-year follow-up study (2003-2012). J Pediatr (Rio J). 2015;91(1):30-35.
15. Silverberg JI, Hanifin JM. Adult eczema prevalence and associations with asthma and other health and demographic factors: a US population-based study. J Allergy Clin Immunol. 2013;132:1132-38.
16. Margolis JS, Abuabara K, Bilker W, Hoffstad O, Margolis DJ. Persistence of mild to moderate atopic dermatitis. JAMA Dermatol. 2014;150:593-600.
17. Weidinger S, Gupta AK. Atopic dermatitis. Lancet. 2016;387(10023):1109-22.
18. Wandalsen GF, Camelo-Nunes ICC, Naspitz CK, Solé D. Fatores de risco para eczema atópico em escolares. Rev Inst Matern Infant Pernamb. 2005;5:19-25.
19. Kantor R, Silverberg JI. Environmental risk factors and their role in the management of atopic dermatitis. Exp Rev Clin Immunol. 2017:13(1):15-20.
20. Andersson NW, Hansen M V, Larsen AD, Hougaard KS, Kolstad HA, Schlünssen V. Prenatal maternal stress and atopic diseases in the child: a systematic review of observational human studies. Allergy. 2016:71:15-26.
21. Kantor R, Kim A, Thyssen J, Silverberg JI. Association of atopic dermatitis with smoking: A systematic review and meta-analysis. J Am Acad Dermatol. 2016:75(6):1119-25.
22. Shaheen SO, Rutterford C, Zuccolo L, Ring SM, Davey Smith G, Holloway JW, et al. Prenatal alcohol exposure and childhood atopic disease: a Mendelian randomization approach. J Allergy Clin Immunol. 2014:133:225-32.
23. Cork MJ, Danby SG, Vasilopoulos Y, Hadgraft J, Lane ME, Moustafa M, et al. Epidermal barrier dysfunction in atopic dermatitis. J Invest Dermatol. 2009:129:1892-908.
24. Sole D, Camelo-Nunes IC, Wandalsen GF, Mallozi MC, Naspitz CK; Brazilian ISAAC Group. Prevalence of atopic eczema and related symptoms in Brazilian schoolchildren: results from the International Study of Asthma and Allergies in Childhood (ISAAC) phase 3. J Investig Allergol Clin Immunol. 2006:16:367-76.
25. Silverberg JI, Hanifin J, Simpson EL. Climatic factors are associated with childhood eczema prevalence in the United States. J Invest Dermatol. 2013;33:1752-9.
26. Ahn K. The role of air pollutants in atopic dermatitis. J Allergy Clin Immunol. 2014;134:993-9.
27. Morgenstern V, Zutavern A, Cyrys J, Brockow I, Koletzko S, Krämer U, et al. Atopic diseases, allergic sensitization, and exposure to traffic-related air pollution in children. Am J Respir Crit Care Med. 2008;177:1331-7.
28. Song S, Lee K, Lee YM, Lee JH, Lee SI, Yu SD, et al. Acute health effects of urban fine and ultrafine particles on children with atopic dermatitis. Environ Res. 2011;111:394-9.
29. Bornehag CG, Sundell J, Hagerhed-Engman L, Sigsggard T, Janson S, Aberg N, et al. Association between ventilation rates in 390 Swedish homes and allergic symptoms in children. Indoor Air. 2005;15:275-80.
30. Engebretsen KA, Bager P, Wohlfahrt J, Skov L, Zachariae C, Andersen CAN, et al. Prevalence of atopic dermatitis in infants by domestic water hardness and 1 season of birth. J Allergy Clin Immunol. 2016 Dec 23. pii: S0091-6749(16)32464-2.
31. Thomas KS, Dean T, O'Leary C, Sach TH, Koller K, Frost A, et al. A randomised controlled trial of ion-exchange water softeners for the treatment of eczema in children. PLoS Med. 2011;8: e1000395.
32. Kramer M S, Kakuma R. Maternal dietary antigen avoidance during pregnancy or lactation, or both, for preventing or treating atopic disease in the child. Evid Based Child Health. 2014:9:447-83.
33. Alm B, Aberg N, Erdes L, Möllborg P, Pettersson R, Norvenius SG, et al. Early introduction of fish decreases the risk of eczema in infants. Arch Dis Child. 2009;94:11-15.
34. Ellwood P, Asher M I, Garcia-Marcos L, Williams H, Keil U, Robertson C, et al. Do fast foods cause asthma, rhinoconjunctivitis and eczema? Global findings from the International Study of Asthma and Allergies in Childhood (ISAAC) phase three. Thorax. 2013;68:351-60.
35. Saarinen UM, Kajosaari M. Breastfeeding as prophylaxis against atopic disease: prospective follow-up study until 17 years old. Lancet. 1995;346:1065-9.
36. Yang YW, Tsai CL, Lu CY. Exclusive breastfeeding and incident atopic dermatitis in childhood: a systematic review and meta-analysis of prospective cohort studies. Br J Dermatol. 2009;161:373-83.
37. Pelucchi C, Chatenoud L, Turati F, Pelucchi C, Chatenoud L, Turati F, et al. Probiotics supplementation during pregnancy or infancy for the prevention of atopic dermatitis: a meta-analysis. Epidemiology. 2012;23:402-14.
38. Boyle RJ, Bath-Hextall FJ, Leonardi-Bee J, Murrell DF, Tang ML. Probiotics for the treatment of eczema: a systematic review. Clin Exp Allergy. 2009;39:1117-27.
39. Spergell JM, Paller AS. Atopic dermatitis and the atopic march. J. Allergy Clin Immunol. 2003;112:118-27.
40. Thomsen SF. Epidemiology and natural history of atopic diseases. Eur Clin Respir J. 2015 Mar 24;2. doi: 10.3402/ecrj.v2.24642.
41. Singh AM, Moore PE, Gern JE, Lemanske RF Jr, Hartert TV. Bronchiolitis to asthma: a review and call for studies of genevirus interactions in asthma causation. Am J Respir Crit Care Med. 2007;175:10819.
42. Ben-Gashir MA. Predictors of atopic dermatitis severity over time J Am Acad Dermatol. 2004;50:349-56.
43. Alduraywish AS, Standl M, Lodge CJ, Abramson MJ, Allen KJ, Erbas B, et al. Is there a march from early food sensitization to later childhood allergic airway disease? Results from two prospective birth cohort studies. Pediatr Allergy Immunol. 2017;28(1):30-7.
44. van Beijsterveldt CE, Boomsma DI. Genetics of parentally reported asthma, eczema and rhinitis in 5-year-old twins. Euro Respir J. 2007;29(3):516-21.
45. Strachan DP, Wong HJ, Spector TD. Concordance and interrelationship of atopic diseases and markers of allergic sensitization among adult female twins. J Allergy Clin Immunol. 2001;108(6):901-7.
46. Barnes KC. An update on the genetics of atopic dermatitis: scratching the surface in 2009. J Allergy Clin Immunol. 2010;125(1):16-29.
47. Hoffjan S, Epplen JT. The genetics of atopic dermatitis: recent findings and future options. J Mol Med. 2005; 83:682-92.
48. Bin L, Leung DY. Genetic and epigenetic studies of atopic dermatitis. Allergy Asthma Clin Immunol. 2016 Oct 19;12:52. eCollection 2016 Oct 19.
49. Gao PS, Rafaels NM, Mu D, Hand T, Murray T, Boguniewicz M, et al. Genetic Variants in TSLP are Associated with Atopic Dermatitis and Eczema Herpeticum. J Allergy Clin Immunol. 2010;125(6):1403-7.
50. Sokolowska-Wojdylo M, Glen J, Zablotna M, Rebala K, Trzeciak M, Sikorska M, et al. The frequencies of haplotypes defined by three polymorphisms of the IL-31 gene: -1066, -2057, and IVS2 + 12 in Polish patients with atopic dermatitis. Int J Dermatol. 2015;54(1):62-7.
51. Stemmler S, Parwez Q, Petrasch-Parwez E, Epplen JT, Hoffjan S. Association of variation in the LAMA3 gene, encoding the alphachain of laminin 5, with atopic dermatitis in a German case-control cohort. BMC Dermatol. 2014;14:17.
52. Margolis DJ, Gupta J, Apter AJ, Ganguly T, Hoffstad O, Papadopoulos M, et al. Filaggrin-2 variation is associated with more persistent atopic dermatitis in African American subjects. J Allergy Clin Immunol. 2014;133(3):784-9.
53. Trzeciak M, Wesserling M, Bandurski T, Glen J, Nowicki R, Pawelczyk T. Association of a Single Nucleotide Polymorphism in a Late Cornified Envelope-like Proline-rich 1 Gene (LELP1) with Atopic Dermatitis. Acta Derm Venereol. 2016;96(4):459-63.
54. Heine G, Hoefer N, Franke A, Nöthling U, Schumann RR, Hamann L, et al. Association of vitamin D receptor gene polymorphisms with severe atopic dermatitis in adults. Br J Dermatol. 2013;168(4):855-8.
55. Kilic S, Silan F, Hiz MM, Isik S, Ögretmen Z, Özdemir Ö. Vitamin D receptor gene BSMI, FOKI, APAI, and TAQI polymorphisms and the risk of atopic dermatitis. J Investig Allergol Clin Immunol. 2016;26(2):106-10.
56. Cork MJ, Robinson DA, Vasilopoulos Y, Ferguson A, Moustafa M, MacGowan A, et al. New perspectives on epidermal barrier dysfunction in atopic dermatitis: gene-environment interactions. J Allergy Clin Immunol. 2006;118(1):3-21.
57. Hon KL, Leung AK, Barankin B. Barrier repair therapy in atopic dermatitis: an overview. Am J Clin Dermatol. 2013;14(5):389-99.
58. van Smeden J, Bouwstra JA. Stratum corneum lipids: their role for the skin barrier function in healthy subjects and atopic dermatitis patients. Curr Probl Dermatol. 2016;49:8-26.
59. Castro APM, Solé D, Filho NAR, Jacob CMA, Rizzo MCFV, Fernandes MFM, et al. Guia Prático para o Manejo da Dermatite Atópica - opiniao conjunta de especialistas em alergologia da Associaçao Brasileira de Alergia e Imunopatologia e da Sociedade Brasileira de Pediatria. Rev Bras Alerg Imunolpatol. 2006;29(6):268-82.
60. Draelos ZD. Modern moisturizer myths, misconceptions, and truths. Cutis. 2013;91(6):308-14.
61. Ong PY, Leung DY. Bacterial and Viral Infections in Atopic Dermatitis: aComprehensive Review. Clin Rev Allergy Immunol. 2016;51(3):329-37.
62. Hepburn L, Hijnen DJ, Sellman BR, Mustelin T, Sleeman MA, May RD, et al. The complex biology and contribution of Staphylococcus aureus in atopic dermatitis, current and future therapies. Br J Dermatol. 2016; Oct 25. doi: 10.1111/bjd.15139. [Epub ahead of print].
63. Dybboe R, Bandier J, Skov L, Engstrand L, Johansen JD. The Role of the Skin Microbiome in Atopic Dermatitis: A Systematic Review. Br J Dermatol. 2017, Feb 16. doi:10.1111/bjd.15390. [Epub ahead of print].
64. Park JM, Jo JH, Jin H, Ko HC, Kim MB, Kim JM, et al. Change in Antimicrobial Susceptibility of Skin-Colonizing Staphylococcus aureus in Korean Patients with Atopic Dermatitis during Ten-Year Period. Ann Dermatol. 2016;28(4):470-8.
65. Leung DY. New Insights into Atopic Dermatitis: Role of Skin Barrier and Immune Dysregulation. Allergol Int. 2013;62:151-61.
66. Boguniewicz M, Leung D. Recent insights into atopic dermatitis and implications for management of infectious complications. J Allergy Clinical Immunol. 2010;125(1):4-13.
67. Wang AX, Landén N X. New insights into T cells and their signature cytokines in atopic dermatitis. Int Um Bioc Mol Bio. 2015;67:601-10.
68. Mrabet-Dahbi S, Maurer M. Does allergy impair innate immunity? Leads and lessons from atopic dermatites. Allergy. 2010;65:1351-6.
69. Han NR, Oh HA, Nam SY, Moon PD, Kim DW, Kim HM, et al. TSLP induces mast cell development and aggravates allergic reactions through the activation of MDM2 and STAT6. J Invest Dermatol. 2014;134:2521-30.
70. Gutowska-Owsiak D, Schaupp AL, Salimi M, Selvakumar TA, McPherson T, Taylor S, et al. IL-17 downregulates filaggrin and affects keratinocyte expression of genes associated with cellular adhesion. Exp Dermatol. 2012;21:104-10.
71. Raap U, Weissmantel S, Gehring M, Eisenberg AM, Kapp A, Fölster-Holst R. IL-31 significantly correlates with disease activity and Th2 cytokine levels in children with atopic dermatitis. Pediatr Allergy Immunol. 2012;23:285-8.
72. Sabat R, Ouyang W, Wolk K. Therapeutic opportunities of the IL- 22-IL-22R1 system. Nat Rev Drug Discov. 2014;13:21-38.
73. Nakayamada S, Kanno Y, Takahashi H, Jankovic D, Lu KT, Johnson TA, et al. Early Th1 cell differentiation is marked by a Tfh cell-like transition. Immunity. 2011:35:919-31.
74. Sawada E, Yoshida N, Sugiura A, Imokawa G. Th1 cytokines accentuate but Th2 cytokines attenuate ceramide production in the stratum corneum of human epidermal equivalents: an implication for the disrupted barrier mechanism in atopic dermatitis. J Dermatol Sci. 2012;68:25-35.
75. Johnson-Huang LM, Suarez-Farinas M, Pierson KC, Fuentes- Duculan J, Cueto I, Lentini T, et al. A single intradermal injection of IFN-gamma induces an inflammatory state in both non-lesional psoriatic and healthy skin. J Invest Dermatol. 2012;132:1177-87.
76. Totte JE, van der Feltz WT, Hennekam M, van Belkum A, van Zuuren EJ, Pasmans SG. Prevalence and odds of Staphylococcus aureus carriage in atopic dermatitis: a systematic review and meta-analysis. Br J Dermatol. 2016;175(4):687-95.
77. Lubbe J. Secondary infections in patients with atopic dermatitis. Am J Clin Dermatol. 2003;4(9):641-54.
78. Park KD, Pak SC, Park KK. The pathogenic effect of natural and bacterial toxins on atopic dermatitis. Toxins (Basel). 2017;9(1):3.
79. Travers JB. Toxic interaction between Th2 cytokines and Staphylococcus aureus in atopic dermatitis. J Investig Dermatol. 2014;134(8):2069-71.
80. Bunikowski R, Mielke M, Skarabis H, Herz U, Bergmann RL, Wahn U, et al. Prevalence and role of serum IgE antibodies to the Staphylococcus aureus-derived superantigens SEA and SEB in children with atopic dermatitis. J Allergy Clin Immunol. 1999;103(1 Pt 1):119-24.
81. Nomura I, Tanaka K, Tomita H, Katsunuma T, Ohya Y, Ikeda N, et al. Evaluation of the staphylococcal exotoxins and their specific IgE in childhood atopic dermatitis. J Allergy Clin Immunol. 1999;104(2 Pt 1):441-6.
82. Zhang X, Shang W, Yuan J, Hu Z, Peng H, Zhu J, et al. Positive feedback cycle of TNF alpha promotes Staphylococcal enterotoxin B-Induced THP-1 cell apoptosis. Frontiers in cellular and infection microbiology. 2016;6:109.
83. Novak N, Bieber T, Leung DY. Immune mechanisms leading to atopic dermatitis. J Allergy Clin Immunol. 2003;112(6 Suppl):S128-39.
84. Gupta AK, Batra R, Bluhm R, Boekhout T, Dawson TL, Jr. Skin diseases associated with Malassezia species. J Am Acad Dermatol. 2004;51(5):785-98.
85. Bolognia JL, Jorizzo JL, Rapini RP. Dermatology. Elsevier Health Sciences; 2003.
86. Glatz M, Bosshard PP, Hoetzenecker W, Schmid-Grendelmeier P. The Role of Malassezia spp. in Atopic Dermatitis. J Clin Med. 2015;4(6):1217-28.
87. Aspres N, Anderson C. Malassezia yeasts in the pathogenesis of atopic dermatitis. Austr J Dermatol. 2004;45(4):199-205.
88. Thayikkannu AB, Kindo AJ, Veeraraghavan M. Malassezia-Can it be Ignored? Ind J Dermatol. 2015;60(4):332-9.
89. Mittermann I, Wikberg G, Johansson C, Lupinek C, Lundeberg L, Crameri R, et al. IgE sensitization profiles differ between adult patients with severe and moderate atopic dermatitis. PloS one. 2016;11(5):e0156077.
90. Sampson HA. The evaluation and management of food allergy in atopic dermatitis. Clin Dermatol. 2003;21:183-928.
91. Chiu CY, Huang YL, Tsai MH, Tu YL, Hua MC, Yao TC, et al. Sensitization to food and inhalant allergens in relation to atopic diseases in early childhood: a birth cohort study. PLoS One. 2014 Jul 17;9(7):e102809.
92. Heratizader A, Wichmann K, Werfel T. Food allergy and atopic dermatitis: how are they connected? Cur Allergy Asthma Rep. 2011:11(4):284-91.
93. Boyce JA, Assa'a A, Burks AW, Jones SM, Sampson HA, Wood RA, et AL. Guidelines for the diagnosis and management of food allergy in the United States: report of the NIAID sponsored expert panel. Nutr Res. 2011;31(1):61-75.
94. Cocco RR. Alergias alimentares. Rev Bras Med. 2012;69:1-5.
95. Werfel T, Heratizadeh A, Niebuhr M, Kapp A, Roesner LM, Karch A, et al. Exacerbation of atopic dermatitis on grass pollen exposure in an environmental challenge chamber. J Allergy Clin Immunol. 2015;136:96-103,e109.
96. Darsow U, Vieluf D, Ring J. Evaluating the relevance of aeroallergen sensitization in atopic eczema using the tool 'atopy patch test': a randomized, double-blind multicenter study. Atopy patch test study group. J Am Acad Dermatol. 1999;40:187-93.
97. Herbarth O, Fritz GJ, Rehwagen M, Richter M, Röder S, Schlink U. Association between indoor renovation activities and eczema in early childhood. Int J Hyg Environ Health. 2006;209:241-7.
98. Scalabrin DM, Bavbek S, Perzanowski MS, Wilson BB, Platts-Mills TA, Wheatley LM. Use of specific IgE in assessing the relevance of fungal and dust mite allergens to atopic dermatitis: a comparison with asthmatic and nonasthmatic control subjects. J Allergy Clin Immunol. 1999;104:1273-9.
99. Guillet G, Guillet MH. Natural history of sensitizations in atopic dermatitis. A 3-year follow-up in 250 children: food allergy and high risk of respiratory symptoms. Arch Dermatol. 1992;128:187-92.
100. Kutlua A, Karabacak E, Aydinc E, Ozturka S, Taskapan O, Aydinoz S, et al. Relationship between skin prick and atopic patch test reactivity to aeroallergens and disease severity in children with atopic dermatites. Allergol Immunopathol (Madr). 2013;41(6):369-73.
101. Wisniewski J, Agrawal R, Minnicozzi S, Xin W, Patrie J, Heymann PW, et al. Sensitization to Food and Inhalant Allergens in Relation to Age and Wheeze Among Children with Atopic Dermatitis. Clin Exp Allergy. 2013;43(10):1160-70.
102. Wollenberg A, Oranje A, Deleuran M, Simon D, Szalai Z, Kunz B, et al. ETFAD/EADV Eczema task force 2015 position paper on diagnosis and treatment of atopic dermatitis in adult and paediatric patients. J Eur Acad Dermatol Venereol. 2016;30:729-47.
103. Cipriani F, Ricci G, Leoni MC, Capra L, Baviera G, Longo G, et al. Autoimmunity in atopic dermatitis: Biomarker or simply epiphenomenon? J Dermatol. 2014;41:1-8.
104. Valenta R, Natter S, Seiberler S, Wichlas S, Maurer D, Hess M, et al. Molecular characterization of an autoallergen, hom s 1, identified by serum IgE from atopic dermatitis patients. J Invest Dermatol. 1998;111:1178-83.
105. Valenta R, Mittermann I, Werfel T, Garn H, Renz H. Linking allergy to autoimmune disease. Trends Immunol. 2009;30(3):109-16.
106. Honeyman JF. Psychoneuroimmunology and the Skin. Acta Derm Venereol. 2016;96(217):38-46.
107. Gaspar NK, Aide MK. Atopic dermat i t is: al lergic dermatitis or neuroimmune dermatitis? An Bras Dermatol. 2016;91(4):479-88.
108. Paller AS, Mancini AJ. Hurwitz Clinical Pediatric Dermatology: A textbook of skin disorders of childhood and adolescence.Elsevier Health Sciences; 2015.
109. Eichenfield LF, Tom WL, Chamlin SL, Feldman SR, Hanifin JM, Simpson EL, et al. Guidelines of care for the management of atopic dermatitis: section 1. Diagnosis and assessment of atopic dermatitis. Journal of the American Academy of Dermatology. 2014;70(2):338-51.
110. Griffiths C, Barker J, Bleiker T, Chalmers R, Creamer D. Rook's Textbook of Dermatology, 4 Volume. Set: Wiley; 2016.
111. Pires MC, Cestari S. In: Dermatite atópica. Rio de Janeiro: Ed. Diagraphic; 2005. p. 111-8.
112. Pires MC, Santos RNR. Dermatites e eczemas. In: Sittart JAS & Pires MC. Dermatologia na prática médica. Sao Paulo: Ed. Roca; 2007. p. 31-62.
113. Ezzedine K, Droitcourt C, Ged C, Diallo A, Hubiche T, de Verneuil H, et al. Usefulness of a global clinical icthyosis vulgaris scoring system for predicting common FLG null mutations in an adult caucasian populations. Br J Dermatol. 2012;167:1165-9.
114. Hanifin JM, Rajka G. Diagnosis features of atopic dermatitis. Acta Derm Venereol (Stockh). 1980; Suppl. 92:44-7.
115. Brenninkmeijer EE, Schram ME, Leeflang MM, Bos JD, Spuls PI. Diagnostic criteria for atopic dermatitis: a systematic review. The British journal of dermatology. 2008;158(4):754-65.
116. Williams HC, Burney PG, Pembroke AC, Hay RJ. The U.K. Working Party's Diagnostic Criteria for Atopic Dermatitis. III. Independent hospital validation. Br J Dermatol. 1994;131(3):406-16.
117. Kunz B, Oranje AP, Labrèze L, Stalder JF, Ring J, Taïeb A. Clinical validation and guidelines for the SCORAD index: consensus report of the European Task Force on Atopic Dermatitis. Dermatol. 1997;195(1):10-9.
118. Oranje AP, Glazenburg EJ, Wolkerstorfer A, de Waard-van der Spek FB. Practical issues on interpretation of scoring atopic dermatitis: the SCORAD index, objective SCORAD and the three-item severity score. Br J Dermatol. 2007;157(4):645-8.
119. Van Oosterhout M, Janmohamed SR, Spierings M, Hiddinga J, de Waard-van der Spek FB, Oranje AP. Correlation between Objective SCORAD and Three-Item Severity Score used by physicians and Objective PO-SCORAD used by parents/patients in children with atopic dermatitis. Dermatology. 2015;230(2):105-12.
120. Hanifin JM, Thurston M, Omoto M, Cherill R, Tofte SJ, Graeber M. The eczema area and severity index (EASI): assessment of reliability in atopic dermatitis. EASI Evaluator Group. Exp Dermatol. 2001;10(1):11-8.
121. Schmitt J, Langan S, Deckert S, Svensson A, von Kobyletzki L, Thomas K, Spuls P. Harmonising Outcome Measures for Atopic Dermatitis (HOME) Initiative. Assessment of clinical signs of atopic dermatitis: a systematic review and recommendation. J Allergy Clin Immunol. 2013;132(6):1337-47.
122. Flohr C, Johansson SGO, Wahlgren CF, Williams H. How atopic is atopic dermatitis? J Allergy Clin Immunol. 2004;114:150-8.
123. Werfel T, Allam JP, Biedermann T, Eyerich K, Gilles S, Guttman- Yassky E, et al. Cellular and molecular immunologic mechanisms in patients with atopic dermatitis. J Allergy Clin Immunol. 2016;138:336-49.
124. Rossberg S, Gerhold K, Geske T, Zimmermann K, Menke G, Zaino M, et al. Elevated blood eosinophils in early infancy are predictive of atopic dermatitis in children with risk for atopy. Pediatr Allergy Immunol. 2016;27:702-8.
125. Kerkhof M, Dubois AE, Postma DS, Schouten JP, de Monchy JG. Role and interpretation of total serum IgE measurements in the diagnosis of allergic airway disease in adults. Allergy. 2003;58(9):905-11.
126. Laske N, Niggemann B. Does the severity of atopic dermatitis correlate with serum IgE levels? Pediatr Allergy Immunol. 2004;15(1):86-8.
127. Thijs J, Krastev T, Weidinger S, Buckens CF, de Bruin-Weller M, Bruijnzeel-Koomen C, et al. Biomarkers for atopic dermatitis: a systematic review and meta-analysis. Curr Opin Allergy Clin Immunol. 2015;15:453-60.
128. Kabashima-Kubo R, Nakamura M, Sakabe J, Sugita K, Hino R, Mori T, et al. A group of atopic dermatitis without IgE elevation or barrier impairment shows a high Th1 frequency: possible immunological state of the intrinsic type. J Dermatol Sci. 2012;67:37-43.
129. Lowe AJ, Carlin JB, Bennett CM, Hosking CS, Abramson MJ, Hill DJ, et al. Do boys do the atopic march while girls dawdle? J Allergy Clin Immunol. 2008;121:1190-5.
130. Heil PM, Maurer D, Klein B, Hultsch T, Stingl G. Omalizumab therapy in atopic dermatitis: depletion of IgE does not improve the clinical course - a randomized, placebo-controlled and double blind pilot study. J German Soc Dermatol. 2010; 8:990-98.
131. Kawamoto N, Fukao T, Kaneko H, Hirayama K, Sakurai S, Arai T, et al. Risk factors for infantile atopic dermatitis and recurrent wheezing. J Investig Allergol Clin Immunol. 2012;22:116-25.
132. Wen HJ, Wang YJ, Lin YC, Chang CC, Shieh CC, Lung FW, et al. Prediction of atopic dermatitis in 2-yr-old children by cord blood IgE, genetic polymorphisms in cytokine genes, and maternal mentality during pregnancy. Pediatr Allergy Immunol. 2011;22:695-703.
133. Chong Neto HJ, Rosário NA. Studying specific IgE: in vivo or in vitro. Allergol Immunopathol (Madr.). 2009;37:31-5.
134. Sampson HA, Albergo R. Comparison of results of skin tests, RAST and double-blind, placebo-controlled food challenges with atopic dermatitis. J Allergy Clin Immunol. 1984;74:26-33.
135. Lack G, Fox D, Northstone K, Golding J; Avon Longitudinal Study of Parents and Children Study Team. Factors associated with the development of peanut allergy in childhood. N Engl J Med. 2003;348(11):977-85.
136. Spergel JM, Boguniewicz M, Schneider L, Hanifin JM, Paller AS, Eichenfield LF. Food allergy in infants with atopic dermatitis: limitations of food-specific ige measurements. Pediatrics. 2015;136(6):e1530-8.
137. Tsakok T, Marrs T, Mohsin M, Baron S, du Toit G, Till S, et al. Does atopic dermatitis cause food allergy? A systematic review. J Allergy Clin Immunol. 2016;137(4):1071-8.
138. Hill DJ, Hosking CS, de Benedictis FM, Oranje AP, Diepgen TL, Bauchau V, et al. Confirmation of the association between high levels of immunoglobulin E food sensitization and eczema in infancy: an international study. Clin Exp Allergy. 2008;38(1):161-8.
139. Canonica GW, Ansotegui IJ, Pawankar R, Schmid-Grendelmeier P, van Hage M, Baena-Cagnani CE, et al. A WAO - ARIA - GA2LEN consensus document on molecular-based allergy diagnostics. World Allergy Organ J. 2013;6(1):17.
140. Matricardi PM, Kleine-Tebbe J, Hoffmann HJ, Valenta R, Hilger C, Hofmaier S, et al. EAACI Molecular Allergology User's Guide. Pediatr Allergy Immunol. 2016;27 Suppl 23:1-250.
141. Ott H, Fölster-Holst R, Merk HF, Baron JM. Allergen microarrays: a novel tool for high-resolution IgE profiling in adults with atopic dermatitis. Eur J Dermatol. 2010;20(1):54-61.
142. Gadisseur R, Chapelle JP, Cavalier E. A new tool in the field of in-vitro diagnosis of allergy: preliminary results in the comparison of ImmunoCAPc 250 with the ImmunoCAPc ISAC. Clin Chem Lab Med. 2011;49(2):277-80.
143. Kerschenlohr K, Darsow U, Burgdorf WH, Ring J, Wollenberg A. Lessons from atopy patch testing in atopic dermatitis. Cur Allergy Asthma Rep. 2004; 4:285-9.
144. Leung DY. Pathogenesis of atopic dermatitis. J Allergy Clin Immunol. 1999;104:S99-S108.
145. Leung DYM. Atopic dermatitis: new insights and opportunities for therapeutic intervention. J Allergy Clin Immunol. 2000;105:860-76.
146. Beltani VS. The role of house dust mites and other aeroallergens in atopic dermatitis. Clin Dermatol. 2003;21:177-82.
147. Seidenari S, Giusti F, Pellacani G, Bertoni L. Frequency and intensity of responses to mite patch tests are lower in nonatopic subjects with respect to patients with atopic dermatitis. Allergy. 2003;58:426-9.
148. Resende ERMA, Segundo GRS. Testes cutâneos de leitura tardia para alimentos: revisao da literatura. Rev Bras Alerg Imunopatol. 2010; 33:184-9.
149. Giusti F. Reproducibility of atopy patch tests with Dermatophagoides: a study on 85 patients with atopic dermatitis. Contact Dermatitis. 2004;50:18-21.
150. Roehr CC, Reibel S, Ziegert M, Sommerfeld C, Wahn U, Niggemann B. Atopy patch tests, together with determination of specific IgE levels, reduce the need for oral food challenges in children with atopic dermatitis. J Allergy Clin Immunol. 2001;107:548-53.
151. Visitsunthorn N, Chatpornvorarux S, Pacharn P, Jirapongsananuruk O. Atopy patch test in children with atopic dermatitis. Ann Allergy Asthma Immunol. 2016;117:668-73.
152. Solé D, Silva LR, Rosário NA, Sarni ROS, Pastorino AC, Jacob CMA, et al. Consenso Brasileiro sobre Alergia Alimentar: 2007. Documento conjunto elaborado pela Sociedade Brasileira de Pediatria e Associaçao Brasileira de Alergia e Imunopatologia. Rev Bras Alerg Imunopatol. 2008;31(2):66-89.
153. Niggemann B. Role of oral food challenges in the diagnostic work-up of food allergy in atopic eczema dermatitis syndrome. Allergy. 2004;59:S32-4.
154. Werfel T, Ballmer-Weber B, Eigenmann PA, Niggemann B, Rancé F, Turjanmaa K, et al. Eczematous reactions to food in atopic eczema: position paper of the EAACI and GA2LEN. Allergy. 2007;62(7):723-8.
155. Bird JA, Lack G, Perry TT. Clinical management of food allergy. J Allergy Clin Immunol Pract. 2015;3(1):1-11.
156. Brand PL, Landzaat-Berghuizen MA. Differences between observers in interpreting double-blind placebo-controlled food challenges: a randomized trial. Pediatr Allergy Immunol. 2014;25(8):755-9.
157. Szabo I, Eigenmann PA. Allergenicity of major cow's milk and peanut proteins determined by IgE and IgG immunoblotting. Allergy. 2000; 55:42-9.
158. Teuber SS, Porch-Curren C. Unproved diagnostic and therapeutic approaches to food allergy and intolerance. Curr Opin Allergy Clin Immunol. 2003; 3:217-21.
159. Erdmann SM, Heussen N, Moll-Siodowy S, Merk HF, Sachs B. CD63 expression on basophils as a tool for the diagnoses of pollen-associated food allergy: sensitivity and specificity. Clin Exp Allergy. 2003; 33:607-14.