Número Atual: Setembro-Outubro 2015 - Volume 3 - Número 5
Editorial
Novos biológicos para asma: terapia anti-interleucina-5
New biologicals for asthma: anti interleukin-5 therapy
Lucas Brom, MD; Thais Nociti Mendonça, MD; Fabiola Reis Oliveira, MD, PhD; Willy Sarti, MD, PhD; Janaina Michelle Lima Melo, MD, PhD; Luisa Karla de Paula Arruda, MD, PhD
DOI: 10.5935/2318-5015.20150024
Faculdade de Medicina de Ribeirao Preto, Universidade de Sao Paulo, Ribeirao Preto, SP
Endereço para correspondência:
L. Karla Arruda
karla@fmrp.usp.br
Estima-se que a asma afete 300 milhoes de indivíduos no mundo, de todas as idades. De acordo com as diretrizes da Global Initiative for Asthma GINA, o paciente com asma é avaliado de acordo com seus sintomas, funçao pulmonar, comorbidades e medicaçoes necessárias para seu controle. A gravidade da asma pode também ser avaliada pelo nível de tratamento necessário para controle dos sintomas e exacerbaçoes nos pacientes1. A maioria dos pacientes alcança bom controle com corticosteroide inalatório (CI) associado ou nao a broncodilatador de longa açao (Long Acting Beta-2 Agonists, LABA), entretanto cerca de 5-10% dos casos permanecem sintomáticos e nao controlados apesar do tratamento otimizado, gerando altos custos de internaçao, medicaçao, idas ao pronto-socorro, faltas no trabalho, além do prejuízo da qualidade de vida do paciente e familiares2,3.
O tratamento da asma nem sempre é fácil, visto ser uma doença respiratória crônica, heterogênea, com diferentes fenótipos, e sinergismo entre fatores ambientais e genéticos4. Portanto, esforços têm sido feitos para delinear, com maior propriedade, os diferentes fenótipos da asma e, com isso, estabelecer um melhor direcionamento no tratamento, dentro do conceito de Medicina de Precisao. Um exemplo é a asma eosinofílica, definida pela presença de eosinofilia pulmonar, na qual o estímulo aos eosinófilos depende inequivocamente da atividade da Interleucina 5 (IL-5), logo, um antagonista da atividade desta interleucina tornou-se óbvio alvo terapêutico5. Recentemente, o anticorpo anti-IL5 mepolizumabe foi adicionado na etapa 5 de tratamento da asma na GINA, para pacientes acima de 12 anos de idade com asma grave eosinofílica nao controlada na etapa 41.
A IL-5 é a principal citocina eosinofilopoiética, com papel importante na inflamaçao alérgica por estimular a produçao, maturaçao, recrutamento, diferenciaçao, sobrevivência e ativaçao de eosinófilos5. É uma proteína de 115 aminoácidos, que consiste de 4 alfa-hélices. A formaçao de dímeros da molécula é importante, pois, quando o dímero IL-5 é reduzido, a forma monomérica pura perde sua atividade biológica. IL-5 é produzida principalmente por linfócitos Th2, Tc2 (células T citotóxicas tipo 2), eosinófilos, mastócitos e células T-ϒδ. Mais recentemente, células linfoides inatas têm se mostrado uma importante fonte de IL-56.
O receptor de IL-5 é um receptor de citocina tipo 1, com estrutura de receptor transmembrana que reconhece e responde a citocinas que tenham 4 cadeias helicoidais alfa. Consiste de uma subunidade alfa ligante específica, e de subunidade β que está associada à transduçao de sinal. Essa subunidade β é expressa numa variedade de leucócitos e também compoe o receptor de IL-3 e do fator estimulador de colônia de macrófago e granulócito (GM-CSF). Com a ligaçao ao receptor de IL-5, um complexo tirosina quinase com ativaçao de JAK2 e Lyn é formado a partir da subunidade β comum, resultando em sinalizaçao intracelular. O receptor de IL-5 está presente em eosinófilos e basófilos.
Os eosinófilos representam 1 a 6% da série branca sanguínea e atuam na defesa contra infecçoes parasitárias. Essas células sao mediadores importantes nas reaçoes alérgicas e participantes na patogênese e gravidade de desordens inflamatórias crônicas das vias aéreas, incluindo a asma. Eosinófilos auxiliam na resposta imune inata desencadeada em vias aéreas por alérgenos ambientais, infecçoes virais e outros estímulos externos, e a ativaçao dessas células pode levar a dano tecidual e remodelamento. Potentes mediadores pro-inflamatórios sao liberados por eosinófilos teciduais, incluindo proteína básica principal derivada de grânulos, mediadores lipídicos, citocinas e quimiocinas, que podem causar inflamaçao das vias aéreas, hiper-responsividade brônquica e remodelamento caracterizado por fibrose, angiogênese e espessamento das vias aéreas5.
A classificaçao da asma e de outras doenças alérgicas em fenótipos pode melhorar o entendimento e o tratamento destas doenças. A identificaçao e utilizaçao de biomarcadores, particularmente aqueles ligados à inflamaçao do tipo 2, podem ser úteis para agrupar os pacientes nesses fenótipos, predizer aqueles que se beneficiarao com uma terapia específica e avaliar a resposta ao tratamento. Biomarcadores podem ser quantificados no escarro, ar exalado e sangue de pacientes com doenças alérgicas. Eles incluem eosinófilos e neutrófilos no escarro, fraçao exalada do óxido nítrico (FeNO), eosinofilia sanguínea, IgE e periostina sérica. Embora o papel dos biomarcadores nao esteja muito bem estabelecido, alguns parâmetros têm sido utilizados de forma consistente como marcadores de resposta do tipo 2:
- Eosinofilia sanguínea > 300/mm3 ou µL (associada com exacerbaçoes graves) ou > 400/mm3 ou µL;
- Eosinofilia no escarro > 2%;
- Periostina sérica (estimulada por IL-13) > 50 ng/mL;
- FeNO > 30 partes por bilhao ppb;
- Dipeptidil peptidase IV (DPP4) (estimulada por IL-13) - níveis de cut-off ainda nao estabelecidos.
Estudos iniciais com anticorpos monoclonais que tinham como alvo a IL-5 nao tiveram sucesso em demonstrar a eficácia desta terapia no controle dos sintomas5. Estes estudos inicias nao consideraram fenótipos de asma existentes para indicaçao da terapia anti-iL-5. Terapia anti-iL-5 pode agir de duas formas, direcionada à própria IL-5, ou ao receptor desta interleucina. Mepolizumabe e reslizumabe agem da primeira forma, ou seja, bloqueiam a IL-5, enquanto que benralizumabe promove o bloqueio do receptor da IL-5.
Mepolizumabe é um anticorpo monoclonal humanizado IgG1/k de alta afinidade, que inibe a ligaçao da IL-5 com seu receptor expresso em eosinófilos. Promove uma significante reduçao dos eosinófilos circulantes, e estudos mais recentes demonstram também diminuiçao de exacerbaçoes de asma e uso de corticosteroide oral4 (Figura 1).
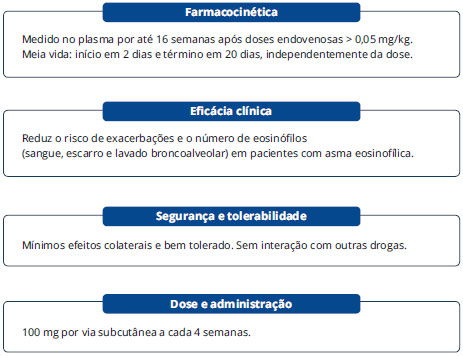
Figura 1 - Aspectos farmacocinéticos e clínicos do mepolizumabe4
Estudos iniciais que avaliaram pacientes com asma leve constataram queda dos eosinófilos séricos e no escarro, porém sem melhora dos sintomas, scores de qualidade de vida ou alteraçao da funçao pulmonar após provocaçao com alérgenos6,7. Entretanto, quando a medicaçao foi administrada a pacientes com asma persistente moderada-grave nao controlada associada a eosinofilia, as respostas foram mais promissoras. O efeito biológico do mepolizumabe na eosinofilia do sangue periférico foi confirmado (reduçao de 67-100%) e foi associado a uma queda de aproximadamente 24% no número de eosinófilos em biópsia de mucosa de vias aéreas, e a uma diminuiçao de 52% de eosinófilos na medula óssea, porém este estudo também nao mostrou efeitos clínicos relevantes na hiper-responsividade brônquica8,9.
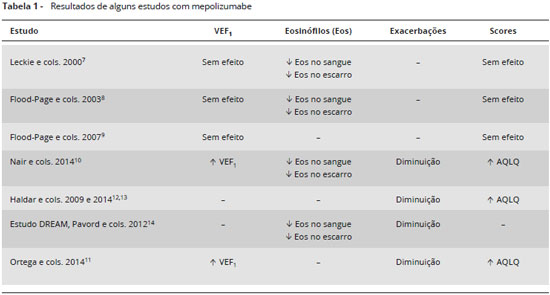
Nair e cols. avaliaram o mepolizumabe em pacientes selecionados pela eosinofilia no escarro (> 3%) e persistência de sintomas de asma, apesar de tratamento com CI em dose alta e prednisona. O objetivo principal foi avaliar especificamente a diminuiçao do uso de CI com a utilizaçao do mepolizumabe. Os indivíduos que receberam mepolizumabe foram capazes de reduzir significantemente o uso de corticosteroide oral (p=0,04). Foi observado também, semelhante aos estudos prévios, reduçao significante de eosinófilos na circulaçao e no escarro, porém, diferentemente dos estudos prévios, nesses indivíduos com grande quantidade de eosinófilos no escarro, melhoras no controle da asma foram evidenciadas através de aumento no escore do Asthma Control Questionnaire ACQ e do VEF1, que permaneceram por 8 semanas. Ao longo do tempo, os indivíduos que receberam mepolizumabe tiveram média de exacerbaçoes de uma a cada 20 semanas, e os do grupo placebo uma a cada 12 semanas, sendo esta diferença significante (p=0,003). Estes achados foram opostos aos estudos prévios, que tiveram resultados negativos em indivíduos nao selecionados pela presença de eosinofilia a despeito de tratamento otimizado da asma, chamando a atençao para a necessidade de identificar biomarcadores que possam predizer melhor resposta a estas medicaçoes5,10.
Outro estudo com mepolizumabe comparado a placebo nao mostrou diferenças em relaçao à via de administraçao. Tanto a via de administraçao endovenosa (EV) quanto a via subcutânea (SC) resultaram em melhora na qualidade de vida, diminuiçao das exacerbaçoes, melhora da funçao pulmonar e diminuiçao das crises e do uso de corticosteroide oral. Portanto, a terapia anti-iL-5 com mepolizumabe foi eficaz para pacientes com asma grave que mantinham elevada contagem eosinofílica no escarro e sangue periférico, a despeito de tratamento otimizado para asma11.
A Tabela 1 mostra resultados de alguns estudos com mepolizumabe.
Haldar e cols. conduziram estudo randomizado, duplo-cego, placebo-controlado, grupo-paralelo com 61 indivíduos com asma eosinofílica refratária e história de exacerbaçoes graves e recorrentes. Vinte e nove pacientes receberam mepolizumabe e 32 receberam placebo, a intervalos mensais, por 1 ano. O objetivo principal foi avaliar o número de exacerbaçoes por indivíduo durante 50 semanas de tratamento. Os autores concluíram que a terapia com mepolizumabe reduziu o número de exacerbaçoes e mostrou melhora no score AQLQ em pacientes com asma eosinofílica refratária12,13,15.
O estudo DREAM14, multicêntrico, duplo-cego, placebo-controlado analisou indivíduos com asma grave com eosinófilos no escarro ≥ 3%, fraçao exalada de óxido nítrico (FeNO) ≥ 50 ppb, asma associada a número de eosinófilos no sangue periférico ≥ 300 cels/µL ou rápida piora da asma após reduçao de 25% ou menos da dose de manutençao de corticosteroide inalado ou oral. Os autores evidenciaram queda dos eosinófilos no escarro e sangue periférico durante o período de tratamento no grupo mepolizumabe. Nesse estudo, a dose de mepolizumabe de 75 mg via intravenosa a cada 4 semanas diminuiu as exacerbaçoes de asma em 48% durante o curso do tratamento. As doses de 250 e 750 mg também resultaram em melhora das crises de asma, mas sem ganho superior àquele observado com a dose de 75 mg4,5.
Ortega e cols. conduziram um estudo duplo-cego, randomizado, com 576 pacientes, que tinham asma com exacerbaçoes recorrentes e evidência de inflamaçao eosinofílica apesar de doses altas de CI. As doses de mepolizumabe administradas foram 75 mg via intravenosa ou 100 mg via subcutânea, comparadas a placebo a cada 4 semanas, por 32 semanas. O mepolizumabe administrado tanto por via intravenosa quanto subcutânea reduziu de maneira significante a taxa de exacerbaçoes e teve associaçao com melhora dos marcadores de controle de asma11.
Por fim, Bel e cols. estudaram o mepolizumabe com o objetivo principal de avaliar a eficácia em diminuir a dose de corticosteroide. Nesse estudo, 135 participantes foram randomizados para receber 100 mg de mepolizumabe por via subcutânea ou placebo. Aqueles que utilizaram mepolizumabe conseguiram reduzir em até 50% a dose de corticosteroides, enquanto os que receberam placebo nao conseguiram nenhuma reduçao. O grupo mepolizumabe também obteve diminuiçao no número de crises, mostrando a importância dos eosinófilos na exacerbaçao da asma5.
Reslizumabe é um anticorpo monoclonal humanizado IgG4/k, desenvolvido para neutralizar a IL-5 circulante e prevenir sua ligaçao aos eosinófilos. É administrado por via endovenosa a cada 4 semanas, com meia-vida de aproximadamente 25 dias16. Analisado para o tratamento da asma moderada/grave com eosinofilia, foi associado à reduçao das exacerbaçoes, maior intervalo entre as crises, melhora dos parâmetros e scores, além de diminuiçao da eosinofilia nas vias aéreas5,17. A Tabela 2 resume alguns estudos realizados com reslizumabe.
Os estudos que avaliaram pacientes com asma eosinofílica moderada-grave evidenciaram benefícios significantes com o uso de reslizumabe na dose de 3 mg/kg por via endovenosa, a cada 4 semanas. Sao estudos randomizados, duplo-cegos, placebo-controlados que mostraram melhora dos scores de avaliaçao da doença através de questionários de controle da asma, melhora clínica, aumento de VEF1 e reduçao das exacerbaçoes5,6,16,18,19.
A chave para o sucesso terapêutico está em selecionar o paciente adequado. A mera presença de eosinófilos no sangue ou escarro talvez nao seja o suficiente. Os pacientes com maior chance de resposta sao aqueles com doença altamente dependente de eosinófilos15. Com a seleçao do fenótipo de asma eosinofílica, a terapia anti-iL-5 leva a uma reduçao importante das exacerbaçoes e da dose de manutençao de corticosteroide4. Comparado aos possíveis efeitos adversos de tratamentos prolongados usando corticosteroides, a segurança e boa tolerância dos anti-iL-5 torna-os opçao terapêutica adicional bem-vinda no arsenal de tratamento para asma grave eosinofílica4,19.
Benralizumabe é um anticorpo humanizado, antirreceptor de IL-5, que induz depleçao quase completa de eosinófilos de forma direta e rápida. Estudo recente avaliou a eficácia do benralizumabe em pacientes com asma grave, nao controlada com tratamento com doses médias a altas de CI mais LABA, e história de duas ou mais exacerbaçoes no ano anterior20. Trata-se de estudo randomizado, duplo-cego, placebo controlado, de grupos paralelos, de fase 3 (estudo CALIMA), realizado em 303 centros em 11 países, em que foram incluídos pacientes com idades entre 12 e 75 anos. Dois grupos de pacientes do grupo benralizumabe receberam 30 mg por via subcutânea a cada 4 semanas (425 pacientes incluídos) ou a cada 8 semanas (441 pacientes incluídos), respectivamente, e foram comparados ao grupo placebo (440 pacientes incluídos). Pacientes foram também estratificados pela contagem de eosinófilos sanguíneos, de 300 eos/µL ou mais, e menos de 300 eos/µL. O uso de benralizumabe resultou em diminuiçao significante das taxas de exacerbaçoes anuais tanto no regime de administraçao a cada 4 semanas quanto a cada 8 semanas, quando comparadas a placebo. Benralizumabe também aumentou de forma significante os valores de VEF1 pré-broncodilator a cada 4 ou 8 semanas, e do score total de asma, apenas a cada 8 semanas, nesses pacientes. Em conclusao, em estudo clínico de fase 3, benralizumabe diminuiu as taxas de exacerbaçoes de asma em pacientes com asma grave, nao controlada, com eosinófilos sanguíneos de 300 eos/µL ou superiores, e foi em geral bem tolerado. Estes resultados reforçam a identificaçao mais refinada de pacientes que terao chance de ter os maiores benefícios com o tratamento com benralizumabe20.
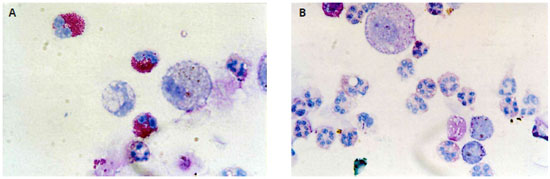
Figura 2 - Aspectos da celularidade do escarro em pacientes com asma grave. A) Escarro de paciente asmático grave mostrando presença de eosinófilos. B) Escarro de paciente asmático grave mostrando presença marcante de neutrófilos. Visualizaçao com aumento de 100x
Em nosso meio, Oliveira realizou estudo em 2005 para avaliar se a pulsoterapia mensal com metilprednisolona na dose de um grama (1 g), administrada durante seis meses, seria capaz de promover controle clínico e funcional de pacientes asmáticos graves, corticodependentes21. Todos os 63 pacientes selecionados, adultos maiores de 18 anos, estavam em uso de corticosteroide na dose diária mínima de 20 mg de prednisona (ou equivalente) há pelo menos três meses, ou faziam uso rotineiro de corticosteroide de depósito intramuscular (betametasona), ou ainda apresentavam efeitos colaterais graves relacionados ao seu uso. Após seleçao inicial, os pacientes passaram por um período de adaptaçao de 90 dias, que incluiu o fornecimento sistemático de medicaçao (CI + LABA e em alguns casos terceira droga controladora) e orientaçao detalhada sobre técnica de uso de medicamentos inalatórios e sobre a importância da adesao ao tratamento. Aqueles que apresentavam comorbidades foram tratados, a exemplo da prescriçao de bloqueador de bomba de prótons nos portadores de doença de refluxo gastresofágico, de corticosteroide tópico nasal nos portadores de rinite alérgica, de antibióticos e antifúngicos naqueles com infecçoes associadas, como sinusites e onicomicoses e de antiparasitários, nos que tinham protoparasitológico positivo. Pacientes em uso de medicamentos anti-hipertensivos do tipo inibidores da enzima conversora de angiotensina e β-bloqueadores adrenérgicos, assim como usuários de AAS e de anti-inflamatórios nao hormonais, foram orientados a modificar os esquemas terapêuticos por outras classes de hipotensores e analgésicos. Em paralelo, foi realizado trabalho educativo para controle ambiental de exposiçao a alérgenos; uso domiciliar de medidor de peak flow; preenchimento de diário de sintomas; e fornecido plano de açao individual para exacerbaçoes. De forma interessante, ao final de 90 dias do período de adaptaçao, apenas 18/63 pacientes (28,5%) selecionados como asmáticos graves corticodependentes continuaram atendendo aos critérios de inclusao do estudo, principalmente no que se refere ao uso continuado de corticosteroides sistêmicos, e 17 deles completaram o estudo randomizado, duplo-cego, controlado com placebo, que avaliou a eficácia de pulsos de metilprednisolona por seis meses. A caracterizaçao fenotípica desses pacientes com asma grave, com idades entre 20 e 73 anos (média 47 anos) que permaneceram sintomáticos e corticodependentes mesmo após abordagem sistemática e tratamento otimizado da asma (n = 17) revelou que apresentavam elevada percentagem de eosinófilos no escarro, variando de 3% a 62% (média de 21%), quando comparados a indivíduos controle (n = 6, eosinófilos entre 0% e 2%). Portanto, todos os pacientes apresentavam níveis > 3% de eosinófilos, considerados elevados. Dez dos dezessete pacientes tinham eosinofilia sanguínea, com > 300 eos/mm3 21. Alguns pacientes também apresentaram elevaçao de neutrófilos no escarro, com valores entre 10% e 90% (média 39,5%), em comparaçao a indivíduos controle (n = 6, neutrófilos entre 1% e 47%, média 17%). Três dos 17 pacientes apresentaram neutrófilos no escarro acima de 65%, considerados elevados (Figura 1). A caracterizaçao do fenótipo desses pacientes asmáticos adultos ainda revelou que 13/17 pacientes (76,4%) apresentaram testes cutâneos de hipersensibilidade imediata positivos para pelo menos um alérgeno inalante, e que 10/16 (62,5%) tinham IgE total elevada, com níveis acima de 100 UI/mL. Este estudo de Oliveira21 ilustra claramente que em nosso meio temos pacientes que apresentam fenótipo semelhante aos descritos para pacientes que participaram de clinical trials para avaliaçao de terapia anti-IL-5, e que portanto poderiam se beneficiar com esta forma de tratamento. Além disso, destaca que a avaliaçao detalhada e o manejo apropriado, incluindo adesao, técnica e cuidados com as comorbidades, sao imprescindíveis para a caracterizaçao do fenótipo correto da asma em pacientes que sao encaminhados por apresentarem asma grave ao médico especialista em asma, alergista/imunologista ou pneumologista.
Recentemente, os biológicos anti-iL-5 mepolizumabe (Nucala®) e reslizumabe (Cinqair®) foram aprovados pelo Food and Drug Administration FDA nos Estados Unidos. O mepolizumabe (Nucala®) foi aprovado como terapia de manutençao adicional para pacientes com asma grave com idades de 12 anos ou maiores, e com fenótipo eosinofílico. É administrado na dose de 100 mg via subcutânea a cada 4 semanas, e apresentado em ampolas de 100 mg de pó liofilizado para reconstituiçao. O reslizumabe (Cinqair®) é indicado como terapia de manutençao adicional para pacientes com asma grave, com idades de 18 anos e maiores, e com fenótipo eosinofílico. Cinqair® é para uso endovenoso, na dose de 3 mg/kg, uma vez a cada 4 semanas, em infusao endovenosa por 20 a 50 minutos, sendo as ampolas com soluçao de 100 mg/10 mL (10 mg/mL) em frascos para uso único. O benralizumabe ainda nao foi licenciado pelo FDA.
Atualmente apenas o omalizumabe (Xolair®) é licenciado para pacientes com asma alérgica grave pela ANVISA em nosso meio, entretanto ainda nao foi incorporado pela Comissao Nacional de Incorporaçao de Tecnologias no SUS, a CONITEC. O omalizumabe tem alta eficácia, comprovada por estudos controlados envolvendo número elevado de pacientes e por metanálises, com nível de evidência A, e segurança demonstrada em adultos e crianças. É licenciado para uso por via subcutânea em crianças de 6 anos de idade ou maiores e adultos, como terapêutica de manutençao adicional naqueles pacientes com asma alérgica grave que permanecem nao controlados após as terapias recomendadas na step 4 da GINA1. Em Julho de 2016 foi publicado parecer da CONITEC contrário à incorporaçao do omalizumabe para o tratamento de pacientes com asma grave nao controlada. O Relatório de Recomendaçao da CONITEC N° 219 de Julho de 2016, disponível em http://conitec.gov.br/images/Relatorios/2016/Relatorio_Omalizumabe_Asma_Grave_final.pdf descreve de forma detalhada e apropriada uma revisao extensa da literatura realizada, os resultados da Consulta Pública e da Apresentaçao de Especialistas no plenário da CONITEC. Este documento cita a recomendaçao do omalizumabe para asma grave nao controlada em outros países, pelo National Institute for Health and Clinical Excellence NICE nos Estados Unidos, e pelos governos australiano e escocês. Entretanto, dentre as razoes para a nao incorporaçao, destaca que as recomendaçoes e uso do omalizumabe por experts no Brasil e exterior sao diferentes das recomendaçoes em bula, sendo utilizado em nosso meio para pacientes com maior gravidade do que o indicado na bula do produto na prática clínica, quando comparados aos pacientes dos clinical trials que demonstraram a eficácia do omalizumabe. Como especialistas em asma, reconhecemos que o uso do omalizumabe deve ser recomendado mediante protocolo detalhado, com indicaçao precisa, preferencialmente com aprovaçao por Centro de Referência para pacientes com asma grave, alinhado com as recomendaçoes da GINA 2016, uma vez que vivemos em um país com recursos financeiros limitados. Pacientes com asma grave em uso de corticosteroide inalatório em altas doses, associado à LABA, e à terceira droga controladora quando possível (tiotrópio, antileucotrienos, teofilina de longa duraçao), com adesao adequada e técnica correta de uso das medicaçoes inalatórias, excluídas e/ou tratadas comorbidades, que ainda permanecem sem o controle da doença, têm indicaçao de se associar o omalizumabe, ou outros imunobiológicos (por exemplo, anti-iL-5 para asma grave eosinofílica) quando estes estiverem disponíveis no Brasil.
Neste número do BJAI, Costa et al. descrevem de forma detalhada a definiçao, diagnóstico, diagnóstico diferencial, comorbidades e estratégias de tratamento e monitorizaçao clínica para pacientes com asma grave, incluindo as indicaçoes do uso de biológicos na asma. Trata-se de um trabalho de revisao de literatura e incorporaçao de experiências do Grupo de Assessoria em Asma da ASBAI, com o objetivo de prover informaçoes atuais em forma de guia prático para o manejo de pacientes com asma grave22. Neste documento, os autores enfatizam que, para a correta abordagem de pacientes com asma grave, sao imprescindíveis a avaliaçao adequada da gravidade da asma e do nao controle da doença com a terapia padrao nas etapas 4 e 5 da GINA, além da avaliaçao correta do nível de aderência ao tratamento e ao controle do ambiente, e identificaçao dos principais fenótipos e comorbidades que impactam o seu controle. Além disso, destacam que a terapia com imunobiológicos para o grupo de pacientes com asma grave, focada em alvos específicos de acordo com o fenótipo e/ou endótipo da doença, já está em prática com o omalizumabe para asma alérgica grave, e foi aprovada recentemente com mepolizumabe para asma eosinofílica pelo FDA nos Estados Unidos, representando uma nova e grande janela de oportunidade para a abordagem dos casos mais desafiadores da doença22.
O grande desafio atual é o acesso dos nossos pacientes aos biológicos para asma, que em geral têm custo elevado. Na prática clínica e em Centros de Referência para pacientes com asma grave, este acesso tem sido possibilitado por processo de judicializaçao na grande maioria dos casos, que resulta em aquisiçao a custos elevados e tempo longo para o acesso efetivo do paciente a essas medicaçoes. Em futuro próximo, novos biológicos além do omalizumabe, aprovados para o tratamento de pacientes com asma grave em outros lugares do mundo, serao também aprovados pela Agência Nacional de Vigilância Sanitária ANVISA no Brasil, e atençao especial deverá ser dirigida às indicaçoes específicas de cada um deles, particularmente considerando o fenótipo da asma em cada paciente.
REFERENCIAS
1. GINA. The global initiative for asthma. 2016 GINA report, global strategy for asthma management and prevention. Available from: www.ginasthma.org.
2. Sheehan WJ, Phipatanakul W. Difficult-to-control asthma: epidemiology and its link with environmental factors. Curr Opin Allergy Clin Immunol. 2015;15(5):397-401.
3. O'Neill S, Sweeney J, Patterson CC, Menzies-Gow A, Niven R, Mansur AH, et al. The cost of treating severe refractory asthma in the UK: an economic analysis from the British Thoracic Society Difficult Asthma Registry. Thorax. 2015;70(4):376-8.
4. Fainardi V, Pisi G, Chetta A. Mepolizumab in the treatment of severe eosinophilic asthma. Immunotherapy. 2016;8(1):27-34.
5. Patterson MF, Borish L, Kennedy JL. The past, present, and future of monoclonal antibodies to IL-5 and eosinophilic asthma: a review. J Asthma Allergy. 2015;8:125-34.
6. Hilvering B, Xue L, Pavord ID. Evidence for the efficacy and safety of anti-interleukin-5 treatment in the management of refractory eosinophilic asthma. Ther Adv Respir Dis. 2015;9(4):135-45.
7. Leckie MJ, ten Brinke A, Khan J, Diamant Z, O'Connor BJ, Walls CM, et al. Effects of an interleukin-5 blocking monoclonal antibody on eosinophils, airway hyper-responsiveness, and the late asthmatic response. Lancet. 2000;356(9248):2144-8.
8. Flood-Page PT, Menzies-Gow AN, Kay AB, Robinson DS. Eosinophil's role remains uncertain as anti-interleukin-5 only partially depletes numbers in asthmatic airway. Am J Respir Crit Care Med. 2003;167(2):199-204.
9. Flood-Page P, Swenson C, Faiferman I, Matthews J, Williams M, Brannick L, et al. A study to evaluate safety and efficacy of mepolizumab in patients with moderate persistent asthma. Am J Respir Crit Care Med. 2007;176(11):1062-71.
10. Nair P. Anti-interleukin-5 monoclonal antibody to treat severe eosinophilic asthma. N Engl J Med. 2014;371(13):1249-51.
11. Ortega HG, Liu MC, Pavord ID, Brusselle GG, FitzGerald JM, Chetta A, et al. Mepolizumab treatment in patients with severe eosinophilic asthma. N Engl J Med. 2014;371(13):1198-207.
12. Haldar P, Brightling CE, Singapuri A, Hargadon B, Gupta S, Monteiro W, et al. Outcomes after cessation of mepolizumab therapy in severe eosinophilic asthma: a 12-month follow-up analysis. J Allergy Clin Immunol. 2014;133(3):921-3.
13. Haldar P, Brightling CE, Hargadon B, Gupta S, Monteiro W, Sousa A, et al. Mepolizumab and exacerbations of refractory eosinophilic asthma. N Engl J Med. 2009;360(10):973-84.
14. Pavord ID, Korn S, Howarth P, Bleecker ER, Buhl R, Keene ON, et al. Mepolizumab for severe eosinophilic asthma (DREAM): a multicentre, double-blind, placebo-controlled trial. Lancet. 2012;380(9842):651-9.
15. Mukherjee M, Sehmi R, Nair P. Anti-IL5 therapy for asthma and beyond. World Allergy Organ J. 2014;7(1):32.
16. Kips JC, O'Connor BJ, Langley SJ, Woodcock A, Kerstjens HA, Postma DS, et al. Effect of SCH55700, a humanized anti-human interleukin-5 antibody, in severe persistent asthma: a pilot study. Am J Respir Crit Care Med. 2003;167(12):1655-9.
17. Castro M, Zangrilli J, Wechsler ME, Bateman ED, Brusselle GG, Bardin P, et al. Reslizumab for inadequately controlled asthma with elevated blood eosinophil counts: results from two multicentre, parallel, double-blind, randomised, placebo-controlled, phase 3 trials. Lancet Respir Med. 2015;3(5):355-66.
18. Bjermer L, Lemiere C, Maspero J, Weiss S, Zangrilli J, Germinaro M. Reslizumab for Inadequately Controlled Asthma with Elevated Blood Eosinophil Levels: a Randomized Phase 3 Study. Chest. 16;150(4):789-98.
19. Cardet JC, Israel E. Update on reslizumab for eosinophilic asthma. Expert Opin Biol Ther. 2015;15(10):1531-9.
20. FitzGerald JM, Bleecker ER, Nair P, Korn S, Ohta K, Lommatzsch M, et al. Benralizumab, an anti-interleukin-5 receptor α monoclonal antibody, as add-on treatment for patients with severe, uncontrolled, eosinophilic asthma (CALIMA): a randomised, double-blind, placebo-controlled phase 3 trial. Lancet. 2016 Sep 5. pii: S0140-6736(16)31322-8. doi: 10.1016/S0140-6736(16)31322-8.
21. Oliveira FR. Efeito da pulsoterapia mensal com metilprednisolona em pacientes asmáticos graves e corticodependentes. Estudo prospectivo, duplo-cego, controlado por placebo. Tese de Doutorado apresentada à Faculdade de Medicina de Ribeirao Preto da Universidade de Sao Paulo; 2005.
22. Costa E, Melo JML, Aun MV, Giavina-Bianchi PF, Boechat JL, Wandalsen GF, et al. Guia para o manejo da asma grave. Braz J Allergy Immunol. 2015;3(5):205-25.