Número Atual: Novembro-Dezembro 2014 - Volume 2 - Número 6
- Imprimir
- Indicar
- Estatísticas
- (0)
Comentários - Como Citar
- Download da Citação
- Artigos Relacionados
- Outros do Autor
RELATO DE CASO
Doença celíaca: um diagnóstico diferencial a ser lembrado
Celiac disease: a differential diagnosis to be considered
Adliz da Rocha Siqueira, Claudia Salvini Barbosa Martins da Fonseca, Isabela Maria Barbosa de Paula, Marina Magalhaes Novais
MD. Faculdade Medicina de Petrópolis, Petrópolis, RJ
Endereço para correspondência:
Claudia S. B. Martins da Fonseca
E-mail: claudiasalvini@hotmail.com
Submetido em: 22/01/2015.
Aceito em: 01/08/2015.
Nao foram declarados conflitos de interesse associados à publicaçao deste artigo.
RESUMO
A doença celíaca (DC) é uma enteropatia imuno-mediada, com uma prevalência de 1:100 a 1:300 indivíduos entre os diversos países. Resulta da interaçao de fatores ambientais (exposiçao ao glúten), predisposiçao genética (presença de HLA DQ 2 e DQ 8) e uma resposta imunológica. Há grupos de risco, aonde a incidência é mais elevada que a da populaçao geral: parentes de primeiro grau de pacientes com DC, diabetes mellitus tipo 1, certas síndromes como síndrome de Down, Turner e Williams, doenças autoimunes de tireoide e fígado, e pacientes com deficiência de IgA. Apresenta-se com uma grande variedade de sinais e sintomas. Os sintomas típicos sao diarreia crônica, esteatorreia e distensao abdominal. As demais manifestaçoes sao bem variadas, incluindo baixa estatura, atraso na puberdade, deficiência de ferro refratária ao tratamento, traumas devido à osteoporose, anormalidades dentárias, urticária, estomatite aftosa, elevaçao de aminotransferases, artralgias e constipaçao crônica. Desta forma, a suspeita clínica de DC deve ser cada vez mais encorajada e questionada, sendo necessário que os profissionais da saúde possam realizar triagem adequada com a dosagem de IgA total e IgA antitransglutaminase e, em casos positivos, realizar biopsia duodenal para constataçao de alteraçao da mucosa intestinal. O tratamento consiste na retirada do glúten da dieta, com melhora total dos sintomas e prevençao de possíveis complicaçoes. Neste relato de caso, quisemos enfatizar a DC como diagnóstico diferencial de alergia alimentar à proteína de leite de vaca nao IgE mediada, e destacar a importância de rastrear DC em pacientes com deficiência de IgA, e de pensar neste diagnóstico em pacientes com urticária crônica sem etiologia conhecida.
Descritores: Doença celíaca, deficiência de IgA, autoimunidade, urticária, hipersensibilidade alimentar.
INTRODUÇAO
Doença celíaca (DC) é uma enteropatia imunomediada, precipitada pela ingestao de alimentos contendo glúten em indivíduos geneticamente predispostos1-4. A prevalência de DC afeta de 1:100 a 1:300 indivíduos entre os diversos países1,5,6. No Brasil foram realizados estudos em doadores de sangue, demonstrando elevada prevalência dessa doença em nosso meio. Observou-se uma incidência de 1:681 em Brasília,1:273 em Ribeirao Preto, 1:417 em Curitiba, e 1:214 em Sao Paulo6-8.
A doença resulta da interaçao de fatores ambientais (exposiçao ao glúten), predisposiçao genética (presença de HLA DQ2/DQ8) e uma resposta imunológica. Os alimentos que contêm glúten sao trigo, cevada e centeio, e suas respectivas prolaminas sao gliadina, hordeina e cecalina7,9. É necessária a expressao do HLA DQ2 e/ou HLA DQ8 na superfície das células apresentadoras de antígenos, mas isso nao é suficiente para causar a doença, pois 30 a 40% da populaçao em geral pode ter expressao destas moléculas, mas somente 1% irá apresentar a doença2.
Na DC há produçao de autoanticorpos contra o endomísio, elemento do tecido conjuntivo que reveste a musculatura lisa, e mais especificamente para a transglutaminase tecidual, que é uma enzima intracelular detectada em todas as camadas do intestino delgado, com predomínio na submucosa1. A transglutaminase é liberada em situaçoes de estresse, injúria, infecçao e apoptose, apresentando papel importante na diferenciaçao do epitélio intestinal e na cicatrizaçao de lesoes da mucosa7.
A transglutaminase é responsável pela deaminaçao da gliadina1. Quando atinge a lâmina própria do intestino delgado, a gliadina sofre deaminaçao pela transglutaminase, tornando-se um peptídeo que se liga com maior avidez às moléculas do HLA DQ2/DQ8 das células apresentadoras de antígenos, levando a intensa resposta proliferativa de clones de linfócitos T CD4+, desencadeando resposta Th1 e Th23,6. A resposta Th1 é responsável pela atrofia vilositária e hiperplasia das células das criptas da mucosa intestinal. Já a resposta Th2 leva à produçao de anticorpos contra o endomísio e transglutaminase6,7.
A DC sempre deve ser investigada em crianças com sintomas gastrointestinais como náuseas, vômitos, diarreia crônica, constipaçao crônica, cólicas, dor abdominal; e com sintomas extraintestinais incluindo baixa estatura, perda de peso, atraso puberal, amenorreia, anemia ferropriva crônica, fadiga crônica, estomatite de repetiçao, dermatite herpetiforme, traumas devido à osteopenia/osteoporose, provas hepáticas alteradas, irritabilidade, artrite/artralgia, neuropatia e alteraçao do esmalte dentário2,4.
Grupos de risco nos quais há uma elevada incidência de DC incluem parentes de primeiro grau de pacientes portadores de DC, pacientes com doenças autoimunes da tireoide e fígado, diabetes mellitus tipo I, deficiência seletiva de IgA, portadores de síndromes de Down, Turner e Williams2,10. Pacientes portadores de quadro clínico sugestivo ou que se encontram em grupo de risco devem ser rastreados para DC (Tabela 1).

A DC pode ser classificada em:
Clássica/típica: as manifestaçoes gastrointestinais têm início entre 6 e 24 meses, após a introduçao do glúten na dieta4,5,7. O quadro clínico cursa com: diarreia crônica, esteatorreia, distensao abdominal, perda de peso, diminuiçao do tecido celular subcutâneo, hipotrofia muscular, alteraçao do humor (irritabilidade ou apatia). Vômitos e anemia podem estar presentes quando a doença se manifesta precocemente1,4,5,7.
Nao clássica/atípica: apresenta-se mais tardiamente na criança, com predomínio dos sintomas extraintestinais, como: baixa estatura, anemia por deficiência de ferro refratária ao tratamento oral, anemia por deficiência de folato e vitamina B12, osteoporose, hipoplasia do esmalte dentário, artralgias ou artrites, constipaçao intestinal refrataria ao tratamento, atraso puberal, irregularidade do ciclo menstrual, esterilidade, abortos de repetiçao, úlcera aftosa recorrente, elevaçao das enzimas hepáticas sem causa aparente, dermatite herpetiforme, epilepsia (isolada ou associada a calcificaçao cerebral), distúrbios psiquiátricos, edema de apariçao abrupta após infecçao ou cirurgia2,4,5,7,8,11.
Silenciosa/assintomática: definida pela presença de anticorpos específicos positivos, HLA e biópsia compatíveis com DC, mas sem sintomas e sinais suficientes para justificar uma suspeita clínica1,2. Esta forma de apresentaçao está sendo cada vez mais reconhecida, pela triagem sorológica em grupos de risco, principalmente em parentes assintomáticos de primeiro grau de pacientes com doença celíaca5,7. A biópsia intestinal realizada nesse grupo pode revelar grave lesao da mucosa e evidência histológica de atrofia das vilosidades consistentes com DC, porém nao há sintomas aparentes7.
DC latente: indivíduos com diagnóstico prévio de DC, com lesao histológica comprovada, e que consumem glúten posteriormente, permanecendo assintomáticos e sem alteraçao na mucosa. Acreditase que alguns pacientes passam a tolerar o glúten ou que a doença demore alguns anos para induzir nova manifestaçao2,5,7.
DC potencial: é definida pela presença de anticorpos específicos para DC e HLA compatíveis, identificados por estudos de triagem positivos, mas sem anomalias histológicas em biópsias duodenais. O indivíduo pode ou nao ter sinais e sintomas, e pode ou nao desenvolver uma enteropatia glúten-dependente posteriormente2,5,7.
Os testes sorológicos para DC sao importantes para selecionar os pacientes que devem ser submetidos a biópsia, e para confirmar o diagnóstico em caso em que foi detectada uma enteropatia. Eles podem ser divididos em dois grupos: os autoanticorpos como o antiendomísio (EMA) e antitransglutaminase tecidual (tTG); e os anticorpos dirigidos contra o agente agressor (gliadina), anticorpo antigliadina convencional (AGA) e anticorpo contra os peptídeos de gliadina deamidados sintéticos (DGPs)1. Esses anticorpos sao da classe IgA ou IgG1. Existe uma alta probabilidade de o paciente com DC ter deficiência de IgA, portanto a IgA total deve ser solicitada2,3,6,10. Os testes baseados na IgG sao úteis para a detecçao de DC em pacientes com deficiência de IgA1,2,10.
A escolha da dosagem de anticorpos IgA antitransglutaminase como triagem se deve ao fato de sua alta sensibilidade (95%), especificidade (95%) e baixo custo2,3,6,10. Para investigaçao de anticorpos IgA antiendomísio, o anticorpo antiendomísio liga-se ao endomisio produzindo um padrao de coloraçao característico visualizado por imunofluorescência indireta, portanto o resultado é informado como positivo ou negativo1. É um teste sensível (80%) e muito específico (100%) para DC, porém é caro e dependente do observador1,2. Os testes para IgA e IgG antigliadina têm sensibilidade e especificidade moderadas, e atualmente nao sao recomendados de rotina para o diagnóstico da doença celíaca. Os anticorpos IgA e IgG para peptídeos sintéticos de gliadina deaminada (DPG) apresentam um alto nível de sensibilidade, mas baixa especificidade. Estudos demonstraram que a detecçao da classe IgG é altamente sensível e específica para a suspeita de DC em geral.
A investigaçao inicia-se pela dosagem de IgA anti-TG2 ou IgA antiendomísio, em associaçao com IgA total. Dá-se preferência à IgA anti-TG2 em relaçao à IgA antiendomísio, devido a esta última ser de alto custo e avaliador-dependente. A dosagem DGP IgG é muito útil nos pacientes com deficiência de IgA, e a combinaçao deste com IgA anti-TG2 melhora a detecçao de casos.
Em um paciente com quadro clínico fortemente sugestivo de DC, mas que apresenta a IgA anti-TG2 negativo com IgA normal, devemos considerar a possibilidade de um resultado falso negativo. Esta situaçao pode ocorrer nos seguintes casos: dieta com pouca ingesta de glúten, enteropatia perdedora de proteína, uso de medicaçao imunossupressora e crianças abaixo de 2 anos de idade2. Nas crianças abaixo de 2 anos deve-se associar a dosagem de IgA e IgG anti-DPG para minimizar este viés1,2,10.
Por outro lado, a IgA anti-TG2 pode estar levemente aumentada em outras patologias como doenças autoimunes, infecçoes, tumores, lesao miocárdica, desordens hepáticas e psoríase2.
Se a dosagem de IgA anti-TG2 for positiva, devese encaminhar a criança ao gastroenterologista para avaliar a realizaçao de biópsia. Alto nível de IgA anti-TG2 é preditivo de atrofia vilositária. No último consenso da European Society for Paediatric Gastroenterology, Hepatology and Nutrition ESPGHAN, foi recomendado que crianças com níveis de IgA anti-TG2 maior que dez vezes o limite normal para a idade sejam submetidas a uma nova coleta sanguínea com dosagem de IgA anti-EMA e HLA DQ-2/DQ8. No caso de ambos serem positivos, a biópsia intestinal poderá ser dispensada, após consenso entre médicos e familiares2 (Figuras 1 e 2).
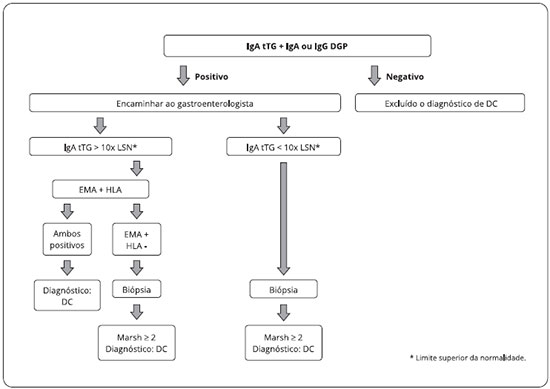
Figura1 - Algoritmo para diagnóstico de doença celíaca (DC) em crianças ou adolescentes com sintomas ou sinais sugestivos de doença celíaca, incluindo sintomas atípicos
Modificado de Husby S et al.2.
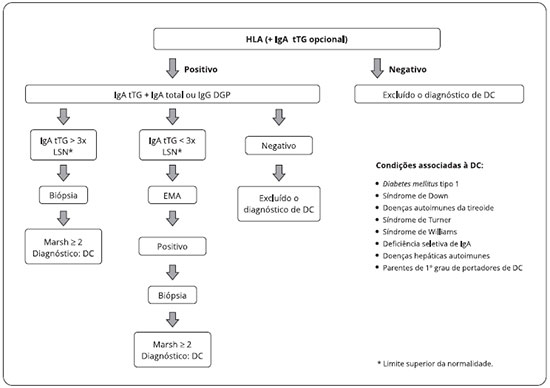
Figura 2 - Algoritmo para investigaçao de doença celíaca (DC) em crianças ou adolescentes com condiçoes associadas à doença celíaca
Modificado de Husby S et al.2.
A biópsia é considerada o padrao ouro, e deve ser feita através de endoscopia com o objetivo de obter mais de quatro fragmentos, pois a doença pode ocorrer em mosaico. Um fragmento ou mais devem ser retirados do bulbo duodenal, e os demais da segunda e terceira porçao do duodeno. Na biópsia, os achados incluem: infiltrados, padroes de hiperplasia e de atrofia. É utilizada a classificaçao de Marsh para a caracterizaçao histológica, sendo Marsh II-III compatíveis com DC2.
A classificaçao de Marsh é determinada pelos seguintes critérios: Marsh I, aumento de linfócitos intraepiteliais (mais de 30 linfócitos por 100 enterócitos); Marsh II, hiperplasia das criptas da altura das vilosidades (aumento da profundidade das criptas sem reduçao) e aumento de linfócitos intraepiteliais; Marsh III, atrofia das vilosidades (A, parcial; B, subtotal; e C, total). O infiltrado linfocitário nao é patognômico de DC, e pode ocorrer em outras patologias como alergia ao leite de vaca, infestaçao maciça por Giardia lamblia, imunodeficiência, sprue tropical, e superpopulaçao de bactérias2.
A dosagem de HLA DQ2 e HLA DQ8 nao deve ser realizada de rotina, mas é de grande valia para excluir a doença em situaçoes específicas10. A sensibilidade do HLA DQ2 é alta, em torno de 91% e, se associada ao HLA DQ8, fica em torno de 96,2%, tornando-se muito difícil um paciente negativo para HLA DQ2/HLA DQ8 ter DC2. Mas devemos estar cientes que 2% dos pacientes portadores de DC nao irao apresentar HLA DQ2 e ou HLA DQ 83.
O tratamento da doença celíaca é composto por uma dieta isenta de glúten (trigo, cevada e centeio) durante toda a vida. Um melhor conhecimento da doença promove melhor adesao ao tratamento, evitando desta forma as transgressoes da dieta, que podem ser voluntárias ou nao (em caso de alimentos contaminados). O Codex Alimentarius define como dieta sem glúten aquela que tem uma concentraçao menor que 20 ppm4. O glúten pode ser substituído pelas farinhas de milho (farinha de milho, amido de milho, fubá), arroz (farinha de arroz), batata (fécula de batata), mandioca (farinha de mandioca, polvilho doce, polvilho azedo e tapioca), farinha de soja e araruta6,12. A aveia, se nao estiver contaminada com o glúten, pode ser aceita na grande maioria dos pacientes com DC, mas deve ser introduzida com muito cuidado e observaçao, pois alguns pacientes irao desenvolver resposta imunológica à avenina4.
A FENACELBRA (Federaçao Nacional das Associaçoes dos Celíacos do Brasil) congrega 15 associaçoes que oferecem suporte aos celíacos e divulgaçao da doença no nosso meio6. Crianças e adolescentes celíacos devem participar de todas as atividades escolares. A família deve comunicar à escola, através de laudo médico, sobre o cuidado no ambiente escolar, que inclui: dieta sem glúten; servir guloseimas como mariola, paçoca, cajuzinho, brigadeiro (com receita original), gelatina, picolé de frutas, pipoca, em festas da escola. É importante a socializaçao da criança durante a alimentaçao12.
O seguimento deve ser multidisciplinar, com médicos e nutricionistas. No primeiro ano de tratamento, as consultas devem ser trimensais e, posteriormente anuais. Devem-se observar os sinais clínicos, um bom manejo da dieta e acompanhamento sorológico, pois a queda dos marcadores é sugestiva de adesao à dieta1.
Em resumo, a DC é doença comum no nosso meio, mas ainda pouco diagnosticada. Os sintomas de alergia ao leite de vaca nao-IgE mediada podem ser muito semelhantes aos sintomas clássicos da DC, e a introduçao do leite e do trigo é realizada no primeiro ano de vida do lactente. Por esta razao, achamos relevante descrever este caso, para enfatizar a importância da DC como um diagnóstico diferencial.
RELATO DE CASO
Paciente do sexo feminino, branca, com 6 anos de idade, natural de Petrópolis, RJ, foi atendida no ambulatório Escola da Faculdade de Medicina de Petrópolis.
Há 3 anos apresentava hiporexia, dor abdominal, burburinho, diarreia, por vezes esteatorreia, urgência fecal e dificuldade de ganho ponderal. Sintomas de rinite persistente leve, com obstruçao nasal, espirros, tosse, febre e mal-estar, necessitando o uso de antibióticos, uma vez por mês. Tinha diagnóstico prévio de alergia a proteína do leite de vaca, nao realizando dieta de exclusao no momento da consulta.
A história alimentar revelava aleitamento materno exclusivo por 1 mês. A partir de entao foi introduzida formula láctea, apresentou 2 episódios de hiperemia cutânea disseminada, sendo realizado diagnóstico clínico de alergia à proteína do leite de vaca, sem confirmaçao sorológica, com substituiçao por fórmula contendo soja até completar 1 ano de vida. Com 1 ano de idade, foi reintroduzido leite de vaca, com boa aceitaçao. Aos 3 anos passou a apresentar vômitos e diarreia. Nao ganhou peso entre os 4 e 6 anos de idade, permanecendo com 17 kg. Aos 5 anos procurou gastropediatra, que orientou dieta de exclusao do leite de vaca, que nao foi realizada. Procurou o nosso serviço para investigaçao de alergia às proteínas do leite de vaca. Ao exame físico, apresentava-se emagrecida, com palidez cutânea e cabelos ressecados.
A investigaçao laboratorial revelou:
Hemograma completo, provas de funçao hepáticas e renal, lipidograma, glicemia, e avaliaçao da tireoide sem alteraçoes. Níveis de imunoglobulinas foram: IgA 112 mg/dL; IgM 59,5 mg/dL; IgG 811 mg/dL; IgE total122 UI/mL. Anticorpos IgE para trigo, alfa lactoalbumina, betalactoglobulina, caseína e leite vaca foram indetectáveis (classe 0).
A avaliaçao para DC mostrou:
- IgA antitransglutaminase 112 U/mL (positivo > 10,0 U/mL).
- IgG antitransglutaminase < 2 (positivo > 10,0 U/mL).
- IgA antiendomisio reagente. IgG antiendomisio nao reagente.
- IgA antigliadina 7,8 U/mL (positivo > 10,0 U/mL).
- IgG antigliadina 14 U/mL (positivo > 10,0 U/mL).
Após a confirmaçao dos marcadores sorológicos, a criança foi encaminhada ao serviço de gastropediatria. Com a dieta rica em glúten, foi realizada biópsia que demonstrou atrofia de mucosa jejunal e jejunite crônica com atrofia moderada, achados compatíveis com DC. Iniciada a dieta de exclusao de glúten, houve melhora do humor, do apetite, da dor abdominal, da esteatorreia, e aumento de peso.
DISCUSSAO
A epidemiologia da DC é semelhante a um iceberg, há mais casos nao identificados do que identificados, portanto temos que pensar nesta patologia para fazermos mais diagnóstico.
Neste relato de caso, os sintomas assemelhavam-se mais aos de alergia ao leite de vaca nao-IgE mediada ou mista, com dor abdominal, diarreia e dificuldade de ganhar peso; porém no momento da consulta a mae nao referia melhora com a dieta de exclusao do leite. Isso nos levou a considerar outros agentes possíveis de desencadear estes sintomas. A IgA antitransglutaminase alta e a IgA antiendomísio reagente nos direcionaram para a necessidade de encaminhar ao gastroenterologista, que através do resultado da biópsia intestinal confirmou o diagnóstico de DC.
Tanto a sorologia quanto a biópsia devem ser realizados mediante uma dieta rica em glúten, para nao mascarar o diagnóstico2,10.
Uma vez feito o diagnóstico, devemos instituir a dieta sem glúten, pois melhora os sintomas e promove a cura da alteraçoes no epitélio intestinal, diminuindo o risco de adenocarcinoma de intestino delgado, câncer de esôfago, linfomas nao Hodgkin de células B e T4, infertilidade nao explicada, osteoporose e fraturas ósseas1.
No período de 2001 a 2009, foi realizado na Holanda um estudo retrospectivo multicêntrico em que foram acompanhadas 129 crianças com menos 19 anos, com biópsia compatível com DC e sorologia antes e após instituiçao da dieta. Foram realizadas dosagem sorológicas, anti-TG2 e EMA, aos 3, 6, 9, 12, 18 e 24 meses após instituiçao da dieta. Observou-se que a concentraçao de anti-TG2 caiu em torno de 74% nos 3 meses de início da dieta sem glúten, e que com 2 anos de dieta, 80% das crianças tornaram-se negativas para anti-EMA e anti-tTG13. O acompanhamento sorológico é muito importante, pois seu declínio indica boa adesao à dieta.
No âmbito da alergia, nos deparamos com outras duas situaçoes em que a DC torna-se um diagnóstico diferencial importante: pacientes com deficiência de IgA e pacientes com urticária crônica. Pacientes com deficiência de IgA têm uma incidência mais elevada de DC, sendo grupo de risco para DC1,2,4,6,14, portanto sempre deve ser feita triagem sorológica de rotina nestes pacientes. Na urticária crônica há estudos que mostraram associaçao com DC15,16. Em Israel foi realizado um estudo objetivando correlacionar urticária crônica e doenças autoimunes, em que foram acompanhados 12.778 pacientes com urticária crônica e 10.714 pacientes saudáveis durante 17 anos. Foi encontrada forte associaçao entre urticária crônica e doenças autoimunes, em ordem decrescente de prevalência: hipotireoidismo, hipertiroidismo, artrite reumatoide, diabetes mellitus tipo 1, síndrome de Sjogren, doença celíaca e LES16.
Desta forma, levando em consideraçao o amplo aspecto clínico da DC, concluímos que DC deve ser um diagnóstico a ser considerado também por alergistas, principalmente nas alergias alimentares nao mediadas por IgE, nos pacientes com deficiência seletiva de IgA e naqueles com urticária crônica.
AGRADECIMENTO
A Dra. Silvia Anderson Cruz, professora e gastroenterologista pediátrica da Faculdade de Medicina de Petrópolis.
REFERENCIAS
1. Bai JC, Fried M, Corazza GR, Schuppan D, Farthing M, Catassi C, et al. World Gastroenterology Organisation global guidelines on celiac disease. J Clin Gastroenterol. 2013;47(2):121-6.
2. Husby S, Koletzko S, Korponay-Szabó IR, Mearin ML, Phillips A, Shamir R, et al. European Society for Pediatric Gastroenterology, Hepatology, and Nutrition guidelines for the diagnosis of coeliac disease. J Pediatr Gastroenterol Nutr. 2012;54(1):136-60.
3. Branski D, Troncone R. Disorders of malabsorption: Gluten-sensitive enteropathy (celiac disease). In: Kliegman RM, Stanton BMD, Geme JS, Schor NF, Behrman RE, editors. Nelson textbook of pediatrics. 19th ed. Philadelphia: Elsevier Saunders; 2011. p. 4715-23.
4. Hill ID, Dirks MH, Liptak GS, Colletti RB, Fasano A, Guandalini S, et al. Guideline for the diagnosis and treatment of celiac disease in children: recommendations of the North American Society for Pediatric Gastroenterology, Hepatology and Nutrition. J Pediatr Gastroenterol Nutr. 2005;40(1):1-19.
5. Baptista ML. Doença celíaca: uma visao contemporânea. Pediatria (Sao Paulo). 2006;28(4):262-71.
6. Sdepanian VL, Galvao LC. Gastroenterologia: Doença celíaca. In: Campos Júnior D, Burns DAR, org. Tratado de Pediatria da Sociedade Brasileira de Pediatria. 3ªed. Barueri: Manole; 2009. p.1075-82.
7. Carvalho S, Pereira J, Cal_ado A, Gracia J, Junqueira J, Guerra S, et al. Doença celíaca: características clínicas e métodos diagnósticos. Revista de Pediatria SOPERJ. 2008;9(2).
8. Pratesi R, Gandolfi L. Celiac disease: a disease with many faces. J Pediatr (Rio J). 2005;81(5):357-8.
9. Misak Z, Hojsak I, Jadresin O, Kekez AJ, Abdović S, Kolaček S. Diagnosis of coeliac disease in children younger than 2 years. J Pediatr Gastroenterol Nutr. 2013;56(2):201-5.
10. Rubio-Tapia A, Hill ID, Kelly CP, Calderwood AH, Murray JA, Gastroenterology ACo. ACG clinical guidelines: diagnosis and management of celiac disease. Am J Gastroenterol. 2013;108(5):656-76.
11. Kalayci AG, Kansu A, Girgin N, Kucuk O, Aras G. Bone mineral density and importance of a gluten-free diet in patients with celiac disease in childhood. Pediatrics. 2001;108(5):E89.
12. Federaçao Nacional das Associaçoes de Celíacos do Brasil [homepage na internet]. Alimentos proibidos e permitidos. Diponível em: www.fenacelbra.com.br/fenacelbra/alimentos-proibidos-e-permitidos/. Acessado em 12 outubro de 2014.
13. Esch CEH, Wolters VM, Gerretsen SAM, Putter H, Blomberg MV, Hoogstraten IMWV, et al. Specific Celiac Disease antibodies in children on a gluten-free diet. Pediatrics. 2011;128(3);547-52.
14. Yel L. Selective IgA Deficiency. J Clin Immunol. 2010;30:10-16.
15. Levine A, Dalal I, Bujanover Y. Celiac Disease associated with familial chronic urticaria and thyroid autoimmunity in a child. Pediatrics. 1999;104;e25.
16. Confino-Cohen R, Chodick G, Shalev V, Leshno M, Kimhi O, Goldberg A. Chronic urticaria and autoimmunity: associations found in a large population study. J Allergy Clin Immunology. 2012;129:1307-13.
17. Lopez FA e Campos Jr. D, org. Tratado de Pediatria da Sociedade Brasileira de Pediatria. 2ª ed. Barueri: Manole; 2009.



