Número Atual: Abril-Junho 2024 - Volume 8 - Número 2
- Imprimir
- Indicar
- Estatísticas
- (0)
Comentários - Como Citar
- Download da Citação
- Artigos Relacionados
-
Outros dos
Autores- Fernanda Casares Marcelino
- Beni Morgenstern
- Laila Sabino Garro
- Tânia Maria Gonçalves Gomes
- Mara Morelo Rocha Felix
- Marcelo Vivolo Aun
- Adriana Teixeira Rodrigues
- Diogo Costa Lacerda
- Gladys Queiroz
- Inês Cristina Camelo-Nunes
- Luiz Alexandre Ribeiro da-Rocha
- Maria Fernanda Malaman
- Ullissis Pádua Menezes
- Maria Inês Perelló Lopes Ferreira
ARTIGO ESPECIAL
Reações aos meios de contraste iodados - aspectos práticos
Reactions to iodinated contrast media - practical aspects
Fernanda Casares Marcelino1; Beni Morgenstern2; Laila Sabino Garro3; Tânia Maria Gonçalves Gomes4; Mara Morelo Rocha Felix5,6,7; Marcelo Vivolo Aun8,9; Adriana Teixeira Rodrigues7,10; Diogo Costa Lacerda9; Gladys Queiroz11; Inês Cristina Camelo-Nunes12; Luiz Alexandre Ribeiro da-Rocha11; Maria Fernanda Malaman13; Ullissis Pádua Menezes14; Maria Inês Perelló Lopes Ferreira15
1. Hospital Regional da Asa Norte (HRAN), Serviço de Alergia e Imunologia- Brasília, DF, Brasil
2. Hospital de Clínicas da Faculdade de Medicina Universidade de São Paulo (HCFMUSP), Unidade de Alergia e Imunologia do Instituto da Criança e do Adolescente - São Paulo, SP, Brasil
3. Universidade Federal de Roraima, Centro de Ciências da Saúde - Boa Vista, RR, Brasil
4. Hospital Central do Exército (HCE), Ambulatório de Alergia e Imunologia - Rio de Janeiro, RJ, Brasil
5. Hospital Federal dos Servidores do Estado (HFSE), Setor de Alergia e Imunologia Pediátrica - Rio de Janeiro, RJ, Brasil
6. Universidade Federal do Estado do Rio de Janeiro (UNIRIO), Departamento de Medicina Geral - Rio de Janeiro - RJ - Brasil
7. Faculdade Souza Marques, Departamento de Pediatria - Rio de Janeiro, RJ, Brasil
8. Faculdade Israelita de Ciências da Saúde Albert Einstein, Hospital Israelita Albert Einstein - São Paulo, SP, Brasil
9. Universidade de São Paulo (FMUSP), Disciplina de Imunologia Clínica e Alergia - São Paulo, SP, Brasil
10. Hospital do Servidor Público do Estado de São Paulo (IAMSPE), Serviço de Alergia e Imunologia - São Paulo, SP, Brasil
11. Universidade Federal de Pernambuco (UFPE), Centro de Pesquisa em Alergia e Imunologia do Hospital das Clínicas - Recife, PE, Brasil
12. Universidade Federal de São Paulo (UNIFESP-EPM), Disciplina de Alergia, Imunologia Clínica e Reumatologia - Departamento de Pediatria - São Paulo, SP, Brasil
13. Universidade Tiradentes, Faculdade de Medicina - Aracaju, SE, Brasil
14. Faculdade de Medicina de Ribeirão Preto (FMUSP- Ribeirão Preto), Serviço de Alergia e Imunologia Clínica e Pediátrica - Ribeirão Preto, SP, Brasil
15. Universidade do Estado do Rio de Janeiro (UERJ) - Rio de Janeiro, RJ, Brasil
Endereço para correspondência:
Fernanda Casares Marcelino
E-mail: fcmalergia@hotmail.com
Submetido em: 22/04/2024
Aceito em: 10/06/2024.
Não foram declarados conflitos de interesse associados à publicação deste artigo.
RESUMO
Desde a sua introdução na década de 1950, os meios de contraste iodados (MCI) têm estado entre os fármacos mais frequentemente prescritos na radiologia e vêm sendo amplamente utilizados após as novas formulações, com melhor resolução e menor toxicidade. As reações adversas a esses agentes não são incomuns, mas são subnotificadas e nem sempre há registro das reações graves. As diretrizes para manejo de pacientes com reação aos contrastes variam entre as diferentes sociedades internacionais, trazendo à discussão diversas controvérsias. Nesse artigo discutiremos sobre os principais aspectos relacionados às reações adversas aos MCI, sobre a investigação através dos testes in vivo em busca de alternativas seguras em caso de procedimentos futuros e também abordaremos as indicações da pré-medicação.
Descritores: Meios de contraste iodados, reações de hipersensibilidade, testes cutâneos, pré-medicação.
Introdução
Os meios de contraste são soluções utilizadas para aumentar a definição da imagem em radiologia, melhorando a acurácia do diagnóstico e monitoramento de diversas doenças.
Os principais meios de contraste utilizados são os meios de contraste iodados (MCI) para exames de raios X e tomografia, meios de contraste a base de gadolínio para exames de ressonância magnética e corantes como o azul patente, o azul de isoflurano, o azul de metileno e fluoresceína.
Mais de 70 milhões de doses de MCI são administradas anualmente em todo o mundo, fazendo com que as reações adversas a esses agentes sejam cada vez mais relevantes1,2.
As reações adversas aos meios de contraste podem ser reações tóxicas (prurido generalizado, sensação de calor, rubor, náuseas, gosto metálico) ou reações de hipersensibilidade (RH). As RH, por sua vez, podem ser alérgicas ou não alérgicas e, de acordo com a cronologia e quadro clínico, se dividem em reações imediatas, se ocorrem até 1 hora (a 6 horas) da administração do contraste, ou tardias, quando se desenvolvem após 1 hora até alguns dias após a exposição3,4.
A elaboração da investigação por testes cutâneos é altamente recomendada para identificar reações de hipersensibilidade alérgica, selecionar alternativas, podendo o teste de provocação ser utilizado para confirmar tolerância3.
Como são classificados os meios de contraste iodados?
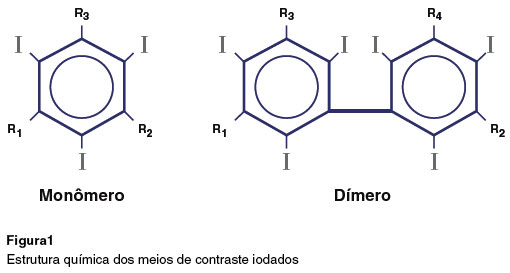
A estrutura química dos MCI consiste em um anel benzênico ligado a pelo menos 3 átomos de iodo responsáveis pela radiopacidade. Cadeias laterais são modificadas com grupos hidroxila e outras moléculas e definem as propriedades de cada meio de contraste (Figura 1)5.
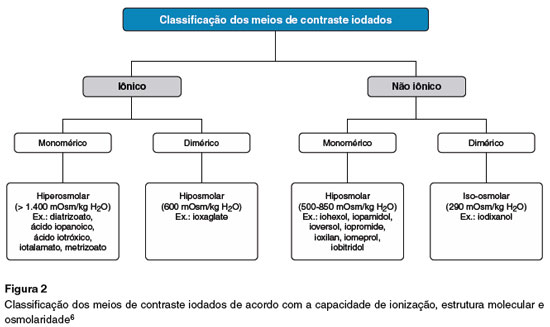
Os diferentes MCI podem ser classificados com base em três propriedades: a carga da molécula de iodo (iônico ou não iônico), a estrutura molecular (monomérica ou dimérica) e a osmolaridade da solução do contraste (hiperosmolar, hiposmolar ou iso-osmolar) (Figura 2)6.
A capacidade de ionização do MCI está diretamente relacionada com a frequência e a gravidade das reações adversas6. Os MCI não iônicos e de mais baixa osmolaridade estão associados a uma menor incidência de reações.
As reações aos meios de contraste iodados são comuns?
No passado, os MCI de alta osmolaridade eram associados a uma maior incidência de reações imediatas por liberação direta de histamina, sem mecanismo imune envolvido. Após a introdução no mercado dos MCI de baixa osmolaridade, houve um decréscimo nessa incidência, mas as evidências de reações induzidas por mecanismo imune vêm aumentando, especialmente nas reações tardias6.
Atualmente reações imediatas ou tardias aos MCI ocorrem em uma frequência de 0,5 a 3% das infusões, sendo normalmente leves a moderadas. A mortalidade é baixa, variando de 1 a 2 por 100.000 administrações3,4,7.
Quais os principais fatores de risco?
Reações prévias ocorridas em exames com contraste são o principal fator de risco para novas reações, aumentando em aproximadamente 5 vezes o risco na reexposição ao mesmo meio de contraste2,4,7,8. Uma reação de hipersensibilidade imediata não constitui um fator de risco para uma reação tardia e vice-versa. As reações de hipersensibilidade imediatas aos meios de contraste são substancialmente menos frequentes nas administrações intra-arteriais e extravasculares (por exemplo, gastrointestinal, genitourinário)3. Outros fatores de risco menos significativos para reações imediatas e tardias estão descritos na Tabela 16.

Deve-se salientar que a história de alergia a crustáceos, moluscos e peixes bem como a dermatite de contato por produtos contendo iodo, não são fatores de risco para reações a MCI6.
Na mastocitose sistêmica não há evidências de maior risco de reações de hipersensibilidade imediata aos MCI quando comparados à população geral3,4, mas uma vez que na mastocitose a anafilaxia ocorre com vários desencadeantes, recomenda-se dosar a triptase sérica basal dos pacientes que apresentaram anafilaxia ao MCI como screening4.
Como classificar as reações?
As reações adversas aos meios de contraste podem ser divididas em reações tóxicas ou RH. As primeiras estão associadas às propriedades químicas dos contrastes, são dependentes da dose e velocidade de infusão e incluem reação vasovagal, convulsões, arritmias e toxicidade em alguns órgãos, especialmente renal4,6,7.
As RH independem da dose e velocidade de infusão, podem ocorrer em resposta a pequenas quantidades do contraste e são classificadas a partir da cronologia, mecanismo envolvido ou fenótipo. De acordo com o tempo de aparecimento após a infusão do contraste se dividem em reações de hipersensibilidade imediatas (RHI) ou tardias (RHT), sendo importante também considerar o tipo de lesão apresentada4,6,7.
As RHI podem ter mecanismo imunológico (IgE mediado), entretanto o mecanismo não imunológico (liberação direta de histamina ou ativação não imunomediada do complemento) é mais comum, especialmente entre os MCI de alta osmolaridade. As manifestações clínicas das RHI são urticária e/ou angioedema isolados ou associados a broncoespasmo, vômitos e/ou hipotensão, caracterizando anafilaxia. Setenta por cento das RHI ocorrem nos primeiros 5 minutos após a infusão, e quanto maior o número de órgãos acometidos e/ou gravidade da reação, maior a possibilidade de reação IgE mediada2,4.
As RHT imunomediadas (célula T) são direcionadas para a estrutura do MCI, e seu espectro de gravidade varia de exantema maculopapular (EMP), erupção fixa à droga (EFD), exantema intertriginoso e flexural simétrico relacionado a drogas (SDRIFE), urticária de início tardio até reações cutâneas graves como reação a droga com eosinofilia e sintomas sistêmicos (DRESS), pustulose exantemática generalizada aguda (PEGA), síndrome de Stevens-Johnson (SSJ) e necrólise epidérmica tóxica (NET). O EMP não complicado é a reação adversa mais frequente com os MCI não iônicos diméricos, que estão implicados em mais de 50% dos casos4,9.
Quem precisa ser investigado?
Reações prévias ocorridas em exames com contraste são o principal fator de risco para novas reações imediatas ou tardias. Portanto, é importante a investigação dos pacientes com suspeita de RH.
Reações inespecíficas como prurido generalizado, sensação de calor, eritema transitório, rubor, reação cutânea no local da injeção, atopia, asma, alergia a outros medicamentos, alergia alimentar, pacientes rotulados como alérgicos a iodo (alérgicos a crustáceos, povidona e moluscos) não têm indicação para investigação de alergia a contrastes na ausência de história prévia de reação ao uso dos mesmos4,6.
Quando, como e onde investigar?
O tempo ideal para investigação de RHI ou RHT deve ser 2 a 6 meses após a reação, e pelo menos seis meses em DRESS após o período de reativação sequencial do herpes vírus. Estudos demonstram que após 6 meses da reação há diminuição da sensibilidade dos testes de 50% para 18%3.
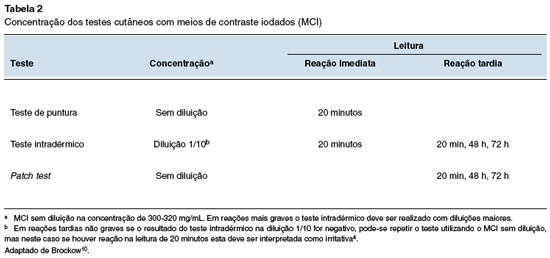
Para RHI, recomenda-se teste de puntura com o MCI não diluído 300-320 mg/mL e leitura imediata em 20 minutos. Se negativo, prosseguir com o teste intradérmico (ID) em diluição 1/10. Utilizar sempre que possível o MCI envolvido3,4.
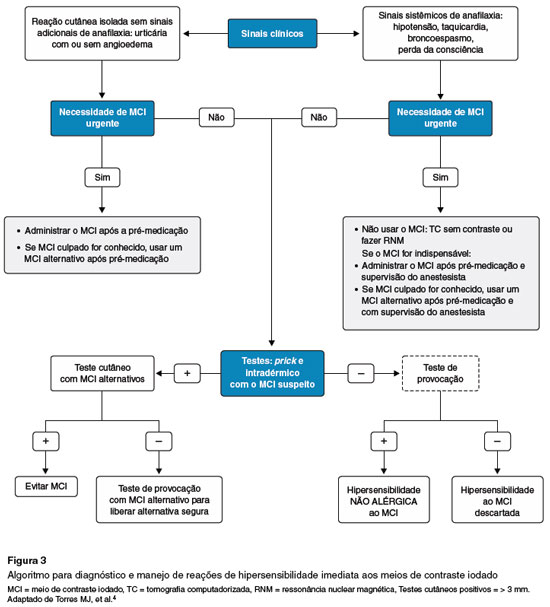
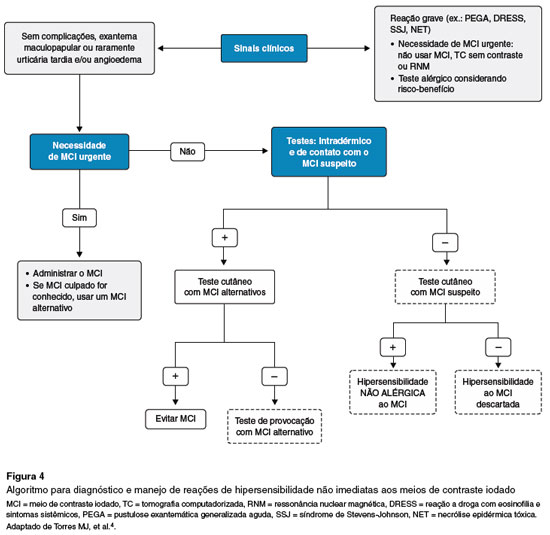
Em RHT testes ID (1/10) com leitura tardia (48/72 h) e testes de contato (MCI não diluído) são a abordagem inicial (Tabela 2). Não fazer teste ID em DRESS, EFD e reações bolhosas pelo risco de reativação. Testes com MCI alternativos são mandatórios se testes positivos ou se o MCI incriminado for desconhecido (Figuras 3 e 4)3,4.
Testes in vitro (Teste de ativação de basófilos - BAT e Teste de linfoproliferação - LTT) não são padronizados e ainda indisponíveis fora da pesquisa clínica.
Testes de provocação são discutíveis pelo risco, mas podem ser realizados para descartar reações tardias leves ou oferecer alternativas, avaliados os riscos e benefícios e excluídas contraindicações4.
Importante salientar que os testes devem ser sempre realizados em ambiente preparado (hospital ou consultório nível 3) e com equipe treinada para eventuais reações.
Existe reatividade cruzada entre os meios de contraste iodados?
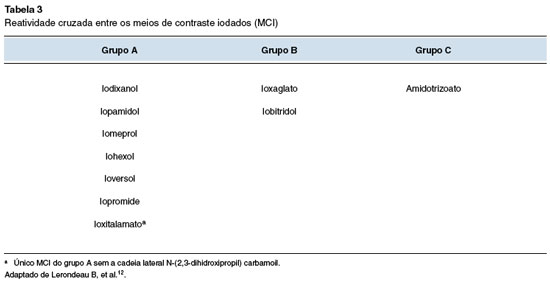
As reações cruzadas entre os MCI têm frequência variável em diferentes estudos (20 e 75%) e não apresentam relação com o iodo, excipiente ou carga iônica. São mais comuns nas reações tardias com MCI que possuem a cadeia lateral N-(2,3-dihidroxipropil) carbamoil 3,6,11,12.
A escolha de alternativas seguras para reexposição deve ser feita com cautela pela possibilidade de reatividade cruzada entre os diferentes produtos13.
O papel das reações cruzadas entre diferentes MCI foi salientado em um artigo de Lerondeau et al. e confirmado por Schrijvers e cols., onde os MCI foram classificados em três grupos, A, B e C, com base na frequência de reatividade cruzada entre os contrastes do mesmo grupo e na baixa reatividade cruzada entre os três grupos (Tabela 3)12,14. Portanto, os pacientes sensibilizados devem ser testados com MCI alternativo de um subgrupo diferente daquele do MCI agressor12.
Quando devemos usar pré-medicação?
A pré-medicação de rotina para pacientes com reações tipo alérgicas ou indeterminadas a MCI é prática comum e referendada por algumas associações americanas, entretanto diretrizes europeias desaconselham essa prática, ressaltando a importância da investigação, considerando tanto o risco de breakthrough reactions, em pacientes com antecedente de reações graves, assim como a falsa sensação de segurança que seu uso pode gerar. A troca do MCI dentro do mesmo grupo hiposmolar ou o uso da pré-medicação para reações imediatas leves a moderadas são recomendadas. Entretanto, não há qualquer evidência de eficácia da pré-medicação em reações IgE mediadas moderadas e graves. Nestes casos, fazer o teste cutâneo e utilizar o MCI alternativo com teste negativo é mais seguro. A pré-medicação não está indicada para reações tardias.
O protocolo mais utilizado e referenciado na literatura para pré-medicação indica o uso da difenidramina como anti-histamínico (Tabela 4)4,6,8,15. No entanto, como tal medicação não está disponível no Brasil na apresentação oral, sugerimos como opção um anti-H1 de 2ª geração.
Protocolos com duração menor que 4-5 horas (oral ou IV) não têm evidência de eficácia, mas podem ser considerados nas situações emergenciais quando não existem alternativas. Nesses casos, utiliza-se a metilprednisolona 40 mg ou hidrocortisona 200 mg IV imediatamente e a cada 4 horas até a administração do MCI e a difenidramina 50 mg IV 1 hora antes do uso do MCI8.
Conclusão
A abordagem do paciente com reação a contraste é um desafio. A história clínica e os testes in vivo são pilares para o diagnóstico, enquanto testes in vitro ainda não são amplamente disponíveis. Reação prévia ao MCI é o principal fator de risco para reações futuras. A frequente ausência de descrição do MCI envolvido e o tempo decorrido desde a reação até o momento da investigação prejudicam todo esse processo. Deve-se incluir testes cutâneos com alternativas em caso de testes positivos, uma vez que reações cruzadas podem ocorrer. Testes de provocação podem ser indicados após avaliação de risco e benefício. A pré-medicação pode ser indicada em reações leves a moderadas, mas não está indicada em reações imediatas graves e tardias.
Referências
1. Schönmann C, Brockow K. Adverse reactions during procedures: Hypersensitivity to contrast agents and dyes. Ann Allergy Asthma Immunol. 2020 Feb;124(2):156-64.
2. Tasker F, Fleming H, McNeill G, Creamer D, Walsh S. Contrast media and cutaneous reactions. Part 1. Immediate hypersensitivity reactions to contrast media and gadolinium deposition. Clin Exp Dermatol. 2019;44(8):839-43.
3. Brockow, K. Diagnosing and Managing Patients with Reactions to Radiocontrast Media. Curr Treat Options Allergy. 2021;8:21021.
4. Torres MJ, Trautmann A, Böhm I, Scherer K, Barbaud A, Bavbek S, et al. Practice parameters for diagnosing and managing iodinated contrast media hypersensitivity. Allergy. 2021 May;76(5):1325-39.
5. Dutra BG, Bauab Jr T (eds.). Meios de contraste: conceitos e diretrizes. Manual da Sociedade Paulista de Radiologia e Diagnóstico por Imagem. 1ª ed. São Caetano do Sul, Difusão Editora; 2020. p. 1-226.
6. Rosado Ingelmo A, Doña Diaz I, Cabañas Moreno R, Moya Quesada MC, García-Avilés C, García Nuñez I, et al. Clinical Practice Guidelines for Diagnosis and Management of Hypersensitivity Reactions to Contrast Media. J Investig Allergol Clin Immunol. 2016;26(3):144-55.
7. Brockow K, Sánchez-Borges M. Hypersensitivity to contrast media and dyes. Immunol Allergy Clin North Am. 2014 Aug;34(3):54764.
8. American College Radiology, ACR Committee on Drugs and Contrast Media. Wang C, Ash D (eds.). Manual on Contrast Media. ACR; 2023. p.1-140.
9. Tasker F, Fleming H, McNeill G, Creamer D, Walsh S. Contrast media and cutaneous reactions. Part 2: Delayed hypersensitivity reactions to iodinated contrast media. Clin Exp Dermatol. 2019 Dec;44(8):844-60.
10. Brockow K. Medical algorithm: Diagnosis and treatment of radiocontrast media hypersensitivity. Allergy. 2020 May;75(5):127880.
11. Gamboa P, Sánchez de Vicente J, Galán C, Jáuregui I, Segurola A, García-Lirio E, et al. Non-immediate hypersensitivity reactions to iomeprol: Diagnostic value of skin tests and cross-reactivity with other iodinated contrast media. Allergy. 2022 Dec;77(12):3641-7.
12. Lerondeau B, Trechot P, Waton J, Poreaux C, Luc A, Schmutz JL, et al. Analysis of cross-reactivity among radiocontrast media in 97 hypersensitivity reactions. J Allergy Clin Immunol. 2016 Feb;137(2):633-635.e4.
13. Brockow K, Romano A, Aberer W, Bircher AJ, Barbaud A, Bonadonna P, et al.; European Network of Drug Allergy and the EAACI interest group on drug hypersensitivity. Skin testing in patients with hypersensitivity reactions to iodinated contrast media - a European multicenter study. Allergy. 2009 Feb;64(2):234-41.
14. Schrijvers R, Breynaert C, Ahmedali Y, Bourrain JL, Demoly P, Chiriac AM. Skin Testing for Suspected Iodinated Contrast Media Hypersensitivity. J Allergy Clin Immunol Pract. 2018;6(4):124654.
15. Schopp JG, Iyer RS, Wang CL, Petscavage JM, Paladin AM, Bush WH, et al. Allergic reactions to iodinated contrast media: premedication considerations for patients at risk. Emerg Radiol. 2013 Aug;20(4):299-306.