Número Atual: Outubro-Dezembro 2022 - Volume 6 - Número 4
- Imprimir
- Indicar
- Estatísticas
- (0)
Comentários - Como Citar
- Download da Citação
- Artigos Relacionados
-
Outros dos
Autores- Evandro Prado
- Antonio C. Pastorino
- Danielle K. Harari
- Marice C. Mello
- Herberto Chong-Neto
- Vânia Oliveira Carvalho
- Dayane M. V. Bruscky
- Jandrei Markus
- Adriana A. Antunes
- Fábio Kuschnir
- Ana Paula M. Castro
- Marcia C. Mallozi
- Gustavo F. Wandalsen
- Clóvis F. Constantino
- Emanuel Sávio Cavalcanti Sarinho
- Dirceu Solé
- Norma P. M. Rubini
ARTIGO ESPECIAL
Dermatite atópica grave: guia prático de tratamento da Associação Brasileira de Alergia e Imunologia e Sociedade Brasileira de Pediatria
Severe atopic dermatitis: a practical treatment guide from the Brazilian Association of Allergy and Immunology and the Brazilian Society of Pediatrics
Evandro Prado1; Antonio C. Pastorino2; Danielle K. Harari1; Marice C. Mello2; Herberto Chong-Neto2; Vânia Oliveira Carvalho2; Dayane M. V. Bruscky1; Jandrei Markus2; Adriana A. Antunes2; Fábio Kuschnir1; Ana Paula M. Castro1; Marcia C. Mallozi1; Gustavo F. Wandalsen2; Clóvis F. Constantino2; Emanuel Sávio Cavalcanti Sarinho1; Dirceu Solé2; Norma P. M. Rubini1
DOI: 10.5935/2526-5393.20220053
1. Associação Brasileira de Alergia e Imunologia (ASBAI)
2. Sociedade Brasileira de Pediatria (SBP)
Endereço para correspondência:
Evandro Prado
E-mail: eprado@domain.com.br
Submetido em: 03/10/2022
Aceito em: 09/10/2022
RESUMO
A dermatite atópica (DA) é uma doença cutânea inflamatória, crônica, comum, complexa e de etiologia multifatorial, que se manifesta clinicamente com prurido muitas vezes incapacitante, lesões recorrentes do tipo eczema, xerose e que pode evoluir para liquenificação. Embora o conhecimento sobre a sua fisiopatologia venham crescendo nos últimos anos, ainda as formas graves são frequentes e representam um desafio para o clínico. Para o presente guia realizou-se revisão não sistemática da literatura relacionada à DA grave refratária aos tratamentos habituais com o objetivo de elaborar um documento prático e que auxilie na compreensão dos mecanismos envolvidos na DA, assim como dos possíveis fatores de risco associados à sua apresentação. A integridade da barreira cutânea é um dos pontos fundamentais para a manutenção da homeostase da pele. Além dos cuidados gerais: evitação dos agentes desencadeantes e/ou irritantes, o uso de hidratantes, suporte emocional, entre outros, o uso de agentes anti-inflamatórios/imunossupressores de uso tópico e/ou sistêmico também foi revisado. A aquisição de novos agentes, os imunobiológicos e as pequenas moléculas, melhorou a terapêutica para os pacientes com formas graves de DA, sobretudo as refratárias aos tratamentos convencionais.
Descritores: Dermatite atópica, hidratação da pele, corticosteroides tópicos, inibidores da calcineurina, ciclosporina, imunobiológicos, dupilumabe, inibidores de JAK.
INTRODUÇÃO
A dermatite atópica (DA) é uma doença cutânea inflamatória, crônica, comum, complexa e de etiologia multifatorial, que se manifesta clinicamente com prurido muitas vezes incapacitante, lesões recorrentes do tipo eczema e xerose e que pode evoluir para liquenificação. A distribuição e morfologia das lesões na pele são variáveis, com início em geral antes dos dois anos, e os pacientes apresentam antecedentes familiares e pessoais de atopia1.
Na ausência de um teste laboratorial diagnóstico de certeza e a grande variabilidade de sinais e sintomas presentes nas diferentes regiões geográficas e com a idade, o diagnóstico da DA é baseado na presença e no padrão de distribuição das lesões associados aos achados clínicos e à história pessoal e familiar de atopia. Há tempos os critérios de Hanifin e Rajka têm sido os mais utilizados para o seu diagnóstico (Tabela 1)2. Essa definição diagnóstica inclui 4 critérios maiores e 22 menores. A presença de pelo menos três dos critérios maiores e três dos menores identifica o paciente com DA2.
Outros critérios diagnósticos foram sendo introduzidos: critério de Williams3 (Tabela 2) e mais recentemente o da Academia Americana de Dermatologia, que acrescentou alguns critérios que devem ser excluídos para realizar-se o diagnóstico de DA com maior precisão (Tabela 3)4.

Os estudos de prevalência de DA realizados mundialmente têm se concentrando, sobretudo, na população pediátrica, e mais raramente em adultos. A heterogeneidade dos grupos estudados, faixa etária e critérios empregados têm contribuído para a divergência dos valores encontrados5,6.
O estudo sobre prevalência de DA que abrangeu o maior número de países e centros de pesquisa foi o International Study of Asthma and Allergies in Childhood (ISAAC), conduzido em 154 centros de 56 países e incluiu mais de 750.000 crianças em duas faixas etárias (6-7 anos e 13-14 anos) que utilizou instrumento padronizado em momentos diferentes.
Nesse estudo a prevalência de DA nos últimos 12 meses, na faixa etária de 6-7 anos, variou de 0,9 na Índia a 22,5% no Equador, e entre 13-14 anos variou de 0,2% na China até 24,6% na Colômbia. No Brasil, o estudo ISAAC documentou na Fase III ser a prevalência média de eczema 8,2% entre os 6-7 anos, e 5,0% entre os de 13-14 anos7. A prevalência de formas graves foi ao redor de 1,5% para ambas as faixas etárias7.
Entre lactentes (12 a 15 meses) o Estudo Internacional de Sibilância da Infância (EISL) documentou valores mais elevados em crianças da Europa e América Latina,14,2% e 18,2%, respectivamente8,9. Pesquisa recente de revisão sistemática avaliou 378 estudos com qualidade para análise, sendo 352 sobre prevalência e apenas 26 sobre incidência de DA, a maioria em crianças. A variação geral da prevalência entre crianças foi de 1,7% a 32,8%, sendo que a prevalência no último ano com diagnóstico médico foi de 0,96% a 22,6%. Em adultos a prevalência geral variou de 1,2% a 9,7%, e a prevalência no último ano, com diagnóstico médico, variou de 1,2% a 17,1%10.
A DA, especialmente nas formas moderadas a graves, tem grande impacto da qualidade de vida do paciente e de seus familiares. Está associada a várias comorbidades atópicas (rinite alérgica, asma, alergia alimentar e esofagite eosinofílica) e também a comorbidades não atópicas, com destaque para a saúde mental, com frequente associação à depressão e ansiedade. Nos últimos anos, foram disponibilizadas terapias sistêmicas inovadoras, incluindo imunobiológicos e pequenas moléculas, que atuam de forma seletiva na inibição de citocinas que participam do processo inflamatório da DA. Essas novas classes de fármacos apresentam eficácia e segurança superiores aos imunossupressores sistêmicos e representam uma nova era no tratamento da DA grave. O objetivo deste guia é atualizar o tratamento da DA grave, com foco principal no racional para a utilização de biológicos e pequenas moléculas.
ASPECTOS CLÍNICOS: HISTÓRIA NATURAL E FENÓTIPOS
Em todos os pacientes com DA a lesão característica é o eczema, e a presença do prurido é achado obrigatório11. Entretanto, as manifestações clínicas de pacientes com DA grave são expressões ampliadas do quadro clínico de DA, e os sinais e sintomas se agravam imensamente. Ao longo da vida a apresentação clínica da DA é variável, e pode ser dividida em quatro seguimentos, conforme descrito a seguir.
Dermatite do lactente (0-2 anos)
As lesões se iniciam cerca de dois meses após nascimento e acometem face (bochechas), couro cabeludo, tronco e superfície extensora dos membros. Nas lesões agudas há vesículas, exsudação, crostas e eritema. A xerose é frequente e é observada em cerca de 42% dos pacientes12,13.
Dermatite da criança (fase pré-puberal 2 a 12 anos)
A superfície flexora passa a ser mais acometida, com destaque às fossas poplítea e cubital. Mãos e pulsos podem estar acometidos. Há um número maior de lesões subagudas, ressecadas e espessadas. Lesões crônicas com algum grau de liquenificação também podem ser observadas12,13.
Dermatite do adulto (12-60 anos)
As lesões se distribuem de maneira mais ampla. Além das flexuras pode haver lesões na cabeça, pescoço e mãos. Xerose é a complicação de pele mais comum em pacientes com DA, e a persistência da pele seca pode prejudicar a função de barreira da pele e alterar a sua microbiota. As lesões são crônicas e liquenificadas, e pacientes podem apresentar surtos de reagudização, além de maior risco de infecções virais12,13.
Dermatite do adulto idoso (acima de 60 anos)
Esta forma é caracterizada principalmente por lesões eczematosas extensas, e alguns pacientes podem apresentar eritrodermia com forte componente pruriginoso. Ocasionalmente as lesões poupam as áreas de flexão. Este grupo específico certamente precisa de uma análise mais profunda para definir critérios clínicos claros para seu diagnóstico. Vale destacar que nesta faixa etária, assim como na DA do lactente, especialmente nos casos graves, diagnósticos diferenciais precisam ser considerados.
A história natural da DA vem mudando nos últimos anos, de lesão restrita à faixa etária pediátrica, a doença se estendeu pela vida adulta e atualmente há relatos de dermatites que se iniciam na sexta década de vida.
Considerando a idade de início da lesão, a história natural da DA pode evoluir das maneiras descritas abaixo.
1. Início muito precoce (entre 3 meses e 2 anos) - não há estudos epidemiológicos nacionais, mas dependendo dos estudos epidemiológicos, pacientes com DA de início precoce podem corresponder entre 60% e 80% de todas as formas de início da doença. Uma parcela substancial dos pacientes pode entrar em remissão completa antes dos 2 anos de idade, mas cerca de 40%, continuam a ter a doença por um longo período de tempo e podem representar a população com maior risco para a marcha alérgica14-16.
2. Início precoce (entre 2 e 6 anos) - esses pacientes também apresentam alto risco de ter outras doenças alérgicas14-16.
3. Início na infância (entre 6 e 14 anos) - grupo pequeno de pacientes, com poucos estudos para entendimento dos riscos ou benefícios de iniciar a DA nesta idade14,15.
4. Início na adolescência (entre 14 e 18 anos) - grupo pequeno de pacientes com dados restritos na literatura, poucas informações sobre a sua evolução.
5. Início adulto (entre 20 e 60 anos) - terceiro maior grupo de indivíduos, é caracterizado principalmente por pacientes do sexo feminino, com um fenótipo clínico bastante leve e espectro de sensibilização, geralmente acompanhado por níveis séricos normais de IgE14,15.
6. Início muito tardio (> 60 anos) - grupo recentemente identificado, que já se divide em dois subgrupos: aqueles que tiveram DA no passado associada a um período longo de remissão, e os que iniciam a doença muito tarde na vida. Estudos observacionais relatam pacientes deste grupo que apresentam uma forma bastante grave da doença e níveis altos de IgE sérica total14,15.
Observa-se ainda, com relação ao curso clínico e gravidade da doença, diferentes padrões evolutivos, que podem ser subdividios em cinco padrões principais: (1) início na infância evoluindo com remissão; (2) doença remitente e recorrente; (3) doença crônica persitente; (4) longos períodos de remissão seguidos de recorrência; e (5) início na adolescência ou vida adulta. Nos padrões 3 e 5 são preponderantes as formas moderadas a graves da doença17.
Fenótipos
Como já descrito, o comportamento da DA pode variar de acordo com a idade de início dos sintomas, mas outros fatores podem influenciar no curso da doença e definir fenótipos diversos. A classificação da DA segundo sua gravidade é uma outra possibilidade de delinear fenótipos, mas traz consigo desafios. É importante que a gravidade seja determinada por escores definidos de gravidade, validados e usados amplamente (vide avaliação da gravidade).Tentativas têm sido feitas para que os dois escores mais utilizados - SCORAD (Scoring Atopic Dermatitis) e EASI (Eczema Area and Severity Index) - possam ter equivalência de seus resultados, para facilitar a uniformização e comparabilidade da população sob avaliação.
A presença de IgE sérica elevada também define um fenótipo de DA: a dermatite extrínseca, presente em 80% dos casos e definida por níveis séricos elevados de IgE total com mutação do gene das filagrinas em 30% aproximadamente, presença de outras atopias, inclusive alergia alimentar, e possível associação com hiperlinearidade palmar. Por outro lado, a DA intrínseca é mais comum em adultos, principalmente em mulheres, e há possibilidade de associação com dermatite de contato, em especial ao níquel15,16,18.
A definição de fenótipos clínicos de DA também traz aspectos importantes para a discussão. É necessário ressaltar que além da apresentação clínica clássica de DA, outras apresentações menos usuais podem fazer parte do estigma atópico. Entre elas destacam-se16,18:
- eczema numular: lesões em moeda que podem ser apresentações atípicas de DA, mas é importante lembrar que nem todos os pacientes que desenvolveram eczema numular apresentam de fato a mesma base fisiopatológica da DA;
- prurido nodular: pápulas hiperqueratóticas e extremamente pruriginosas, que pode estar ou não relacionado à DA;
- eczemas localizados em pálpebra, em mãos e pés, nos mamilos ou a queilite angular. São apresentações clínicas que, se associadas a outras doenças atópicas, podem ser entendidas como manifestações atípicas da DA. Neste contexto é fundamental a realização de diagnósticos diferenciais.
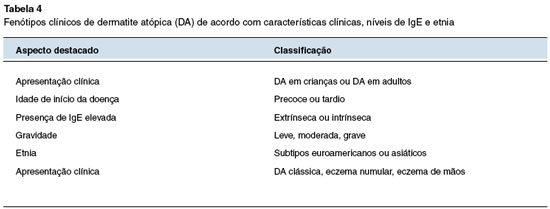
Na Tabela 4 estão apresentados os possíveis fenótipos de DA definidos com base na faixa etária, idade de início, presença de IgE elevada ou não, gravidade da doença, etnia e apresentação clínica clássica ou não.
IMUNOPATOGENIA
São muitos os conhecimentos atuais que envolvem a fisiopatogenia da DA, mas os mais relevantes parecem ser aqueles envolvendo as desordens genéticas, barreira cutânea alterada, desregulação imunológica e alterações do microbioma cutâneo.
Há alguns anos se admitia que a DA era uma doença "inside-out", isto é, o processo inflamatório iniciava na derme acarretando como consequência uma lesão de barreira. Com o conhecimento atual de que a inflamação é decorrente ou se inicia a partir das alterações na barreira cutânea, passou então a ser reconhecida como uma doença predominantemente "outside-in"20.
Barreira cutânea
A barreira cutânea se altera devido a muitos fatores. Um dos fatores inicialmente conhecidos era a destruição de corneócitos por ação excessiva de proteases em corneodesmossomos (banhos com sabonetes alcalinos, aumento de pH da pele, infecção estafilocócica com produção e liberação de enteroxinas) ou por falta da inibição dessas proteases quando exercem essas ações excessivas. O resultado é a perda da integridade e coesão celulares ou o desarranjo entre as células. Os corneócitos são que ratinócitos do estrato córneo que produzem e liberam peptídeos antimicrobianos, um dos representantes da resposta de imunidade inata. São importantes na defesa contra a agressão microbiana e também produtores de ceramidas e colesterol, componentes do fator de hidratação natural da pele. Podemos dizer então que a destruição acelerada de corneócitos aumenta a permeabilidade de barreira, diminui a defesa e também os teores de lipídeos da pele21.
A diminuição dos níveis de filagrina (por mutações ou de forma adquirida) e outras proteínas estruturais da pele, como loricrina e involucrina também alteram a barreira cutânea. As filagrinas são proteínas derivadas das pró-filagrinas presentes nas camadas mais profundas da pele e que por ação de grânulos de querato-hialina migram em direção ao estrato córneo. Submetidas a ações enzimáticas se transformam em ácidos graxos e passam a compor de modo importante a camada lamelar lipídica. Alguns trabalhos consideram a filagrina como uma substância que se comporta como um cimento intercelular que mantém maior adesão entre as células22.
As proteínas de junção são representantes da barreira física. Estão localizadas imediatamente abaixo do estrato córneo. As claudinas, principalmente a claudina-1, têm importante papel nessa defesa. Mutações do gene da claudina diminuem a sua expressão e aumentam a permeabilidade de barreira23.
Todos esses mecanismos, como desorganização celular, diminuição de proteínas como a filagrina e a claudina são importantes para explicar como a pele se defende das agressões ou como essas alterações no nível da barreira cutânea comprometem a integridade da pele com possibilidade da penetração de alérgenos e patógenos.
O microbioma cutâneo mal constituído com baixa diversidade microbiana (disbiose) e a deficiência de peptídeos antimicrobianos contribuem muito para as infecções cutâneas, principalmente estafilocócicas24.
Desregulação imunológica
A barreira cutânea lesada proporciona a liberação de citocinas como a TSLP (linfopoietina do estroma tímico), interleucina (IL)-33 e IL-25, consideradas alarminas e que provocam desregulação imunológica no nível da derme.
A TSLP ativa grande variedade de células como as células linfoides inatas do tipo 2 (ILC2)e Th2, caracterizando o que conhecemos como inflamação T2.
As células Th1, Th2, Th17 e Th22 são as mais importantes na fisiopatologia da DA por produzirem e liberarem substâncias capazes de ativar outras células ou que apresentam atividades pró-inflamatórias como ações principais. Células Th1 são mais participantes na evolução da doença para a cronicidade e liberam interferon-gama.
As células Th2, Th17, Th22 e ILC2 são as principais responsáveis pelo início do processo inflamatório. Muitas citocinas são liberadas por essas células e têm diferentes ações e papel relevante na patogênese da doença25.
Estudos que investigaram a participação das diferentes subpopulações de linfócitos T no processo inflamatório da DA identificaram quatro endotipos principais - americano/europeu, asiático, afroamericano e pediátrico, que estão apresentados na Tabela 5. É importante destacar que embora existam variabilidades com relação à participação das subpopulações Th22, Th17 e Th1, a participação da subpopulação Th2 está presente em todos os fenótipos, definindo a inflamação tipo 2 como fundamental na patogênese da DA26.
As IL-4 e IL-13 induzem a formação de IgE. Quanto maiores os níveis dessas citocinas, menor será a expressão de filagrina, portanto contribuem também para a diminuição dos lipídeos no estrato córneo e indiretamente para o dano tissular. A IL-5 ativa, diferencia e dá sobrevida aos eosinófilos. A IL-17 tem particular importância no agravamento da lesão de barreira. É uma citocina que degrada a claudina-1, proteína de junção que tem função de barreira entre o estrato córneo e o estrato granuloso.
A IL-22, citocina que participa do fenômeno de remodelamento cutâneo, ativa fibroblastos e tem participação na hiperceratose e na hiperpigmentação da pele. A IL-25 estimula células ILC2, Th2, eosinófilos e provoca maior liberação de IL-31. A IL-26, produzida a partir de células Th17, induz a produção e liberação de citocinas Th2, potencializando o processo inflamatório.
A IL-31 é uma citocina muito importante no processo de prurido cutâneo, pois ativa terminais nervosos com liberação de neurotransmissores como os neuropeptídeos (substância P e CGRP)27. A IL-33 estimula mastócitos a liberar histamina, ativa eosinófilos e células ILC2, aumentando os níveis de IL-4 e IL-13 com maior produção de IgE e diminuição dos níveis de filagrina25. O processo inflamatório que se estabelece por ação dessas células e citocinas diminui a expressão de IL-10 liberada de linfócitos B.
Outro fator que potencializa o processo inflamatório é a infecção bacteriana. Enteroxinas estafilocócicas, como a do tipo B (SEB), atuam como superantígenos e aumentam a ação de linfócitos com maior liberação de citocinas pró-inflamatórias27,28.
FATORES DESENCADEANTES E AGRAVANTES
Vários estudos são concordantes em afirmar que a interação entre predisposição genética, disfunção imunológica e fatores desencadeantes ambientais contribui para a fisiopatologia da DA29.
Além da adesão ao tratamento, a exposição a fatores ambientais, incluindo alérgenos e estímulos no local de trabalho e no domicílio, fatores decorrentes do estilo de vida e temperatura, além da desregulação da fisiologia da pele, estão associados à manutenção e exacerbação da DA. Uma sensação de calor, sudorese, fibras de lã, estresse psicológico, comida, ingestão de álcool e o resfriado comum são considerados particularmente importantes como fatores de indução e exacerbação do prurido na DA. Os detalhes relativos aos fatores de início e exacerbação e suas especificidades medidas serão discutidas a seguir30.
Clima e temperatura
Estudos associaram maior prevalência de DA a localidades com baixa umidade, baixa exposição aos raios UV e baixa temperatura ou ao uso de aquecimento interno31.
Poluentes intradomiciliares
Ainda é questionável o envolvimento de substâncias eliminadas no interior dos domicílios, como fumaça de tabaco, produtos de combustão (biomassa, fogões, lareiras), materiais de construção, fontes biológicas e produtos de limpeza31 e os ácaros, na recorrência da DA11.
Poluentes atmosféricos
Estudos de coorte associaram a exposição à poluição do ar e maior prevalência de DA. Possivelmente decorrente do estresse oxidativo e danos à barreira cutânea causada por esses fatores externos. Portanto, mudanças nos fatores climáticos, como temperatura, umidade, radiação e poluição do ar, podem influenciar a resposta e os sintomas da DA31.
A exposição a poluentes liberados pela queima de combustíveis fósseis foi associada a risco aumentado de pré-escolares desenvolverem DA31. Além disso, material particulado em contato com a pele pode favorecer a coçadura da pele, arranhões e a alocinese, estado sensorial anormal em que estímulos que normalmente não evocam coceira causam coceira, e, assim, pioram a DA.
Dieta/Antígenos alimentares
DA e Alergia Alimentar (AA) são condições comuns que aparecem na infância e que podem estar intimamente ligadas. Aproximadamente 30% das crianças com DA moderada a grave sofrem de AA. Há evidências de que dietas de eliminação não justificadas não devem ser administradas a pacientes com DA. A sensibilização a um alimento (teste cutâneo positivo e/ou dosagem de IgE sérica específica) não significa alergia, e a eliminação injustificada desse alimento específico pode ser prejudicial e levar à perda de tolerância, com a possibilidade de anafilaxia quando o mesmo for reintroduzido. Há fortes evidências para a ligação entre o início precoce da DA e o desenvolvimento de outras doenças alérgicas durante avida, a chamada marcha atópica, e várias intervenções preventivas foram sugeridas, como o uso de emolientes, a introdução precoce de amendoim e de ovo em lactentes de alto risco, que em um primeiro momento mostraram resultados promissores para a prevenção da DA, bem como da alergia ao amendoim e ao ovo32. Revisão sistemática recente demonstrou que a aplicação profilática de emolientes, iniciada na primeira infância, pode prevenir a DA, principalmente se usados de modo contínuo em populações de alto risco, mas não preveniram AA. Ainda é discutível se a introdução precoce de alimentos em crianças de risco previne a AA33.
Revisão sistemática seguida de metanálise avaliou os pontos de vista díspares de muitos pacientes com DA e seus cuidadores. A eliminação de determinados alimentos da dieta pode levar à melhora discreta e potencialmente sem importância para a intensidade do eczema, prurido, insônia e alteração na qualidade do sono nesses pacientes. Tal conduta deve ser avaliada em compasso com os riscos potenciais das dietas de eliminação indiscriminada de alimentos para o tratamento da DA, especialmente em bebês e crianças pequenas em risco de desenvolver alergia alimentar mediada por IgE e deficiências nutricionais. O tratamento focado em dietas de eliminação leva a subtratamento no contexto de um número crescente de opções terapêuticas disponíveis para tratar DA34.
Restrições alimentares (eliminação de alérgenos alimentares) para gestantes ou lactantes para prevenir o aparecimento de DA não devem ser recomendadas. Há a possibilidade de a DA poder ser exacerbada a partir da transferência para o lactente de alérgenos alimentares, como ovos, através do leite materno; no entanto, esses lactentes devem ser cuidadosamente diagnosticados com base nos resultados dos testes de eliminação e provocação alimentar via leite materno35.
Aeroalérgenos
Aeroalérgenos podem provocar lesões cutâneas eczematosas em pacientes sensibilizados com DA, que pode ser explicado pelo aumento da permeabilidade da pele para alérgenos inalantes em pacientes com defeitos da barreira cutânea. Testes de contato de atopia positivos estão associados à presença de IgE específica e história positiva de surtos de DA por alérgenos sazonais. Muitos aeroalérgenos que provocam DA são derivados de ácaros Dermatophagoides pteronyssinus e D. farinae. A atividade enzimática dos principais alérgenos de ácaros destrói as junções firmes das células epiteliais na mucosa brônquica e, portanto, também pode deteriorar a disfunção da barreira da pele em pacientes com DA36. Se esses alérgenos forem considerados fatores de exacerbação da erupção, eles devem ser cuidadosamente avaliados, considerando de forma abrangente o histórico médico, as mudanças ambientais e as alterações nas características da erupção. A avaliação deve incluir resultados de testes de eliminação e testes de provocação, se possível, e não baseados apenas nos sintomas clínicos, ou pelo título de IgE específicos, ou resultados de testes cutâneos. Semelhante ao manuseio de alérgenos alimentares, a eliminação de alérgenos ambientais é um adjuvante à farmacoterapia e aos cuidados da pele30.
Muitos pacientes documentam deterioração dos sintomas cutâneos ao contato com alérgenos de pelo de animais. No passado, evitar o contato com animais de estimação era uma recomendação para a prevenção primária de atopia. Entretanto, na atualidade somente a exposição ao epitélio do gato é considerada fator de risco, e por isso deve ser evitada29,30. Não há evidências de que a exposição a cães aumente o risco de DA em crianças, pelo contrário, pode até proteger devido à exposição a micróbios não patogênicos29,30. Uma vez que um paciente é sensibilizado a um animal de estimação e apresenta sintomas após contato, a evitação será necessária36.
Sudorese
Distúrbios na transpiração, bem como excesso de suor remanescente na superfície da pele exposta a altas temperaturas e umidade podem piorar os sintomas da DA. Alérgenos derivados de Malassezia sp. encontrados em resíduos de suor na superfície da pele que não evaporaram podem levar ao agravamento dos sintomas. Altas temperaturas e umidade na superfície da pele obstruem os poros de suor e induzem a transpiração. Para proteger contra a sudorese excessiva e da presença de suor excessivo sobre a pele, roupas íntimas de tecido respirável e de baixa higroscopia são recomendadas. Evitar altas temperaturas e umidade, e medidas apropriadas como tomar banho, enxaguar com água corrente e enxugar devem ser instituídas37.
Infecções cutâneas
Microbiota
A pele é local de vida para uma vasta coleção de microrganismos, incluindo bactérias, vírus, fungos e artrópodes. Esses microrganismos formam um ecossistema associado com habitat favorável, com abundância de dobras, invaginações e nichos especializados. A microbiota da pele vive em simbiose com fatores do sistema imune da pele, desempenhando um papel fundamental e complexo no controle da fisiologia e imunidade da pele35.
Papel das bactérias
Uma das características da DA é que os pacientes têm maior colonização bacteriana, especialmente por Staphylococcus aureus, que é encontrado na pele lesionada em mais de 90% dos pacientes com DA. S. aureus desempenha um papel importante na patogênese da DA, de modo que o tratamento para reduzir a colonização de S. aureus diminui a gravidade da doença e isso se correlaciona com a normalização do pH e da perda de água transepidérmica. A quantidade de S. aureus aumenta de 35% para 90% na composição do microbioma cutâneo durante as crises, e a gravidade das lesões de DA está associada à densidade relativa da colonização de S. aureus na pele.
Além de S. aureus, outras espécies (S. epidermidis e S. hemolyticus) estão muito aumentadas na pele lesionada de pacientes com DA. Em contraste, foi demonstrado que a pele inflamada de DA apresenta diminuição notável de Cutibacterium, Streptococcus, Acinetobacter, Corynebacterium e Prevotella.
Curiosamente, a maior concentração de S. epidermidis pode afetar o comportamento de S. aureus, por produzir moléculas que inibem seletivamente a colonização do S. aureus e aumentam ainda mais a produção de peptídeos antimicrobianos35.
Papel dos vírus
Embora as infecções virais da pele sejam relativamente menos comuns em pacientes com DA quando comparadas às bacterianas, infecções virais difusas e disseminadas são observadas em pacientes com DA, e algumas delas podem ser problemáticas ou até mesmo fatais. As infecções virais comuns na DA incluem o vírus causador do eczema herpético (EH), eczema vaccinatum (EV) ou eczema moluscatum (EM). A infecção pelo vírus Herpes simplex ocorre frequentemente em pacientes com DA e manifestase como uma erupção disseminada e distintamente monomórfica de vesículas em forma de cúpula acompanhadas de febre, mal-estar e linfadenopatia. O EH pode causar complicações graves, incluindo ceratoconjuntivite, viremia, meningite, encefalite ou sepse bacteriana secundária35.
Papel dos fungos
Os fungos também desempenham um papel no desenvolvimento e agravamento da DA. Em particular, o papel das leveduras Malassezia tem sido discutido em vários trabalhos. Malassezia sp. são leveduras constituintes da flora cutânea normal de humanos e habitam camadas superficiais do estrato córneo próximo a glândulas sebáceas e nas partes superiores dos folículos pilosos. A distribuição e o isolamento desta levedura variam em densidade e presença em vários locais e condições da pele. Houve relato de que a colonização por Malassezia é encontrada tanto em pacientes com DA quanto em indivíduos saudáveis, com taxas de detecção de 100% e 78%, respectivamente38. Entre os pacientes com DA, as áreas de cabeça e pescoço são mais propensas a serem colonizadas do que as de membros e tronco. Vários estudos indicaram que as Malassezia sp. induzem a produção de IgE específica, observada exclusivamente em pacientes com DA, mas não em pacientes com rinite alérgica, urticária ou dermatite de contato alérgica39.
DIAGNÓSTICO DIFERENCIAL
O espectro clínico amplo da DA pode levar a diagnósticos e tratamentos errôneos com frequência. As características da DA, incluindo idade de início, distribuição, prurido intenso, xerose, liquenificação e associação com atopia, podem ajudar a distinguir a DA dos demais diagnósticos40.
Eventualmente os pacientes com diagnóstico de DA podem apresentar características clínicas atípicas, levando o médico a questionar o diagnóstico. Nestes casos, tanto o conhecimento dos achados clínicos caracteristicos da DA quanto o reconhecimento de possíveis diagnósticos alternativos são importantes para o paciente, considerando que a conduta e o prognóstico podem ser totalmente diferentes41.
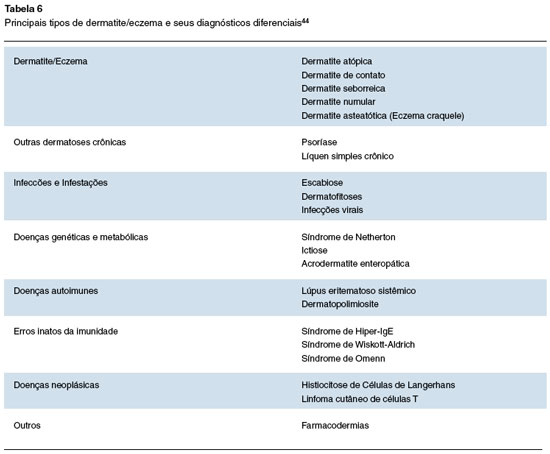
O diagnóstico diferencial da DA em crianças e adultos é amplo e inclui doenças primariamente dermatológicas, até mesmo outras que podem se manifestar com lesões cutâneas que se assemelham muito à DA. Estes devem ser considerados não apenas quando um paciente apresenta pela primeira vez uma erupção cutânea eczematosa, mas também quando um paciente diagnosticado com DA não responde à terapia apropriada42. Os principais diagnósticos estão listados na Tabela 6. Entre esses diagnósticos destacamos os Erros Inatos da Imunidade (EII), por serem doenças conduzidas pelo imunoalergista, fazendo-se necessário um olhar cuidadoso para o diagnóstico correto43.
Entre os EII destacam-se as conhecidas por Doenças Atópicas Primárias (DAP), uma subcategoria destes caracterizados por serem distúrbios monogênicos hereditários que apresentam predominantemente manifestações alérgicas. Isto dificulta seu diagnóstico enquanto EII por não apresentarem fenótipos de infecções de repetição como a maioria destas doenças45. É imperativo que os médicos sejam capazes de reconhecer as DAPs, considerando a terapêutica individual de cada caso e impactando na morbiletalidade destes pacientes. A Tabela 7 mostra os sinais clínicos de alerta que podem auxiliar no diagnóstico das DAPs.

Os principais diagnósticos diferenciais da DA e suas características morfológicas próprias são descritos a seguir.
Dermatite de contato alérgica
Seu diagnóstico é baseado no padrão da dermatite, normalmente sucedendo a exposicão à determinada substância e um teste de contato (patch test) positivo. Este padrão diz respeito à localizacão da lesão na área de pele em contato com o alérgeno (por exemplo, na face, para reação aos cosméticos). A característica da lesão se assemelha muito à DA, sendo por vezes impossível diferenciá-las apenas clinicamente. Os alérgenos mais comuns em crianças e adolescentes são os metais, fragrâncias, conservantes e corantes de coloração44.
Dermatite seborreica
Representa um importante diagnóstico diferencial da DA, sobretudo em sua forma infantil, pela similaridade na distribuicão das lesões. O diagnóstico é baseado na história clinica e exame fisico, incluindo a distribuição de eczema. A dermatite seborreica infantil geralmente começa nos primeiros três meses de vida, ou seja, antes da idade típica de início da DA. Quase sempre envolve a área da fralda, face e couro cabeludo. A região de fraldas costuma ser poupada na DA. Em comparação com a DA, as lesões tendem a ser menos inflamadas e as escamas mais gordurosas, podendo durar alguns meses, mas não ultrapassam os 12 meses de idade, o que também difere do caráter crônico da DA. Entretanto ambas as doenças podem ocorrer de forma concomitante40.
Psoríase
Embora mais comum em adolescentes e adultos, pode ocorrer em qualquer faixa etária. É uma dermatose crônica caracterizada mais frequentemente por lesões em placas e espessamento cutâneo, nitidamente demarcadas com eritema e com a presença de escamas prateadas nas regiões dos cotovelos, joelhos e couro cabeludo. Pode haver envolvimento ungueal e articular (artrite psoriática). A biópsia cutânea pode ser necessária para esclarecimento diagnóstico41.
Escabiose
O diagnóstico diferencial com DA inclui tanto a característica pruriginosa da infestação pelo Sarcoptes scabiei quanto às lesões cutâneas decorrentes deste prurido, com a presenca de pápulas eritematosas e escoriações, predominando nas áreas interdigitais, áreas flexurais do punho, pés e tornozelos, o que poderia caracterizar um eczema atípico. O diagnóstico é confirmado pela visualização dos ácaros à dermatoscopia40.
Ictiose vulgar
É o tipo mais comum das ictioses, causada pela mutação no gene da filagrina (FLG). O quadro clínico típico inclui pele seca com escamas finas e brancas, muitas vezes sem eritema. Prurido e lesões eczematosas podem aparecer, tornando difícil o diagnóstico diferencial com DA. Pode-se questionar se a lesão eczematosa da ictiose vulgar na verdade seria DA, uma vez que cerca de um terço de todos os pacientes com DA são heterozigotos para mutações no gene FLG41.
Síndrome de Netherton
Doença autossômica recessiva causada pela mutação no gene SPINK5. Ao nascimento, o recémnascido pode apresentar ictiose eritrodérmica. Em crianças mais velhas, a doença é caracterizada por uma dermatite distinta, ictiose linear circunflexa, onde as lesões cutâneas são disseminadas de forma linear serpiginosa ou circinada. As lesões são pruriginosas e muitas evoluem para placas eczematosas e liquenificação nas dobras. A dermatite pode ser de difícil distinção da DA, pois as crianças geralmente apresentam níveis elevados de IgE sérica e alergias alimentares. O exame do cabelo pode ser útil, pois à microscopia evidencia-se tricorrexe invaginata (cabelo de bambu)46.
Acrodermatite enteropática por deficiência de zinco
Pode ser genética ou adquirida (por falta de ingesta), caracterizando-se por manchas eritematosas e placas com crostas e erosões predominantemente em áreas periorificiais. Muitas vezes os pacientes apresentam outras manifestações, como diarreia, alopecia e déficit de crescimento. O diagnóstico é clínico, juntamente com a dosagem da fosfatase alcalina de zinco sérica e, muitas vezes, uma biópsia cutânea45.
Síndromes de Hiper-IgE (HIES)
São erros inatos da imunidade (EII) raros (formas autossômica dominante ou recessiva) e caracterizadas por eczema grave, infecções recorrentes da pele (S. aureus) e muitas vezes pneumonias (com formação de pneumatoceles) e níveis séricos de IgE muito altos (> 2000 UI/mL). Os pacientes têm características esqueléticas próprias com face característica (testa proeminente, ponte nasal larga, ponta nasal carnuda e prognatismo). As infeccões cutâneas se apresentam não apenas por impetigo, mas também por furúnculos e abscessos47.
Síndrome de Wiskott-Aldrich (WAS)
Síndrome genética caracterizada pela associação com o eczema, embora as primeiras manifestações cutâneas sejam lesões hemorrágicas com petéquias, hematomas, púrpura, epistaxe, sangramento oral ou diarreia sanguinolenta. As plaquetas caracteristicamente são pequenas e frequentemente ocorrem manifestações autoimunes e neoplasias (principalmente linfomas de células B)44.
Síndrome de Omenn
É uma síndrome rara de imunodeficiência combinada grave, de início precoce no primeiro ano de vida, caracterizada por eritrodermia (semelhante ao eczema) associada a diarreia crônica, pneumonite, déficit de crescimento, linfadenopatia e hepatoesplenomegalia, características que a distinguem da DA43.
Linfoma cutâneo de células T (Micose fungoide)
Doença rara mais frequentemente observada em adultos, com características que se assemelham à psoríase ou eczema numular nas fases iniciais. A biópsia cutânea deverá ser realizada naquelas lesões refratárias ao tratamento com corticosteroide tópico42.
AVALIAÇÃO DA GRAVIDADE E CONTROLE: ESCORES DE AFERIÇÃO
A avaliação da gravidade da DA é essencial para guiar as opções terapêuticas e ponderar a resposta ao tratamento. Na ausência de um padrão ouro ou de biomarcadores específicos disponíveis para uso clínico, vários instrumentos foram desenvolvidos e validados para mensurar a gravidade e controle da DA48,49.
Para aferição da gravidade clínica pelo profissional, os escores mais utilizados e amplamente validados são o índice Scoring Atopic Dermatitis (SCORAD) e o Eczema Area and Severity Index (EASI)48,49.Também é recomendada a avaliação da gravidade pelo próprio paciente e o instrumento mais utilizado é o Patient Oriented Eczema Measure (POEM)49. Além destes, o instrumento validado Investigator Global Assessment for Atopic Dermatitis (vIGA-AD) tem sido particularmente indicado como instrumento complementar para avaliar gravidade em ensaios clínicos50.
O índice SCORAD é amplamente utilizado na prática clínica, varia de 0 a 103 pontos e avalia a extensão e a intensidade das lesões (eritema, edema ou pápulas, exsudato ou crostas, escoriação, liquenificação e xerose cutânea), além dos sintomas subjetivos (prurido e impacto no sono). A DA é classificada como leve quando menor que 25 pontos; moderada, entre 25 e 50 pontos; e grave, quando maior que 50 pontos51,52. O tempo médio para avaliação é de 7 a 10 minutos; tem como vantagem considerar os sintomas subjetivos, a intensidade da xerose e das lesões localizadas em face, pálpebras, pescoço, mãos e pés; e como desvantagem em relação ao EASI ser redundante sobre os sinais inflamatórios cutâneos, um peso menor da extensão das lesões no cálculo final (máximo de 20% do valor) e apenas avaliar a intensidade da lesão representativa para aquele paciente48,52.
O PO-SCORAD (Patient-oriented SCORAD) é escore validado desenvolvido com base no SCORAD. É aplicativo com versão em português que permite ao próprio paciente avaliar a gravidade da DA. Apesar de menos acurado que o SCORAD no item extensão é um instrumento que aborda as lesões em três tipos de pele (branca, asiática e negra) e é de fácil preenchimento53.
O EASI varia de 0 a 72 pontos e engloba os sinais clínicos (eritema, edema/pápula, escoriação e liquenificação) em cada uma das quatro regiões do corpo (cabeça e pescoço, membros superiores, tronco e membros inferiores) e extensão da doença nestas regiões. É interpretado como: 0 = sem lesão; 0,1 a 1,0 = quase sem lesão; 1,1 a 7,0 = DA leve; 7,1 a 21,0 = DA moderada; 21,1 a 50,0 = DA grave; 50,1 a 72,0 = DA muito grave48,54,55. O EASI tem sido preferido ao SCORAD em ensaios clínicos porque avalia os quatro sinais clínicos fundamentais da DA, afere a intensidade das lesões nas quatro regiões corporais ao invés de apenas na lesão representativa, e distribui melhor a pontuação da extensão da doença em relação ao SCORAD. Há, contudo, a necessidade de associar outros escores para avaliação dos sintomas do paciente48,49.
O POEM utiliza sete perguntas autoaplicáveis para abordar o quanto os sinais e sintomas são vivenciados pelo paciente ao longo dos dias e foi amplamente validado49.Varia de 0 a 28 pontos, onde 0 a 2 pontos significa sem lesão ou quase sem lesão; 3 a 7 pontos, DA leve; 8 a 16 pontos, DA moderada; 17 a 24 pontos, DA grave; e 25 a 28 pontos, DA muito grave56. Há tradução e validação linguística para o português (cultura brasileira) disponível e de uso gratuito no site da Universty of Nottingham57.
O vIGA-AD considera a aparência geral das lesões de DA pelo avaliador. O escore varia de 0 a 4 (0 = sem lesão, 1 = quase sem lesão, 2 = DA leve, 3 = DA moderada, 4 = DA grave) e avalia a intensidade (eritema, infiltração ou pápulas, liquenificação, exsudação ou crostas) das lesões3. É instrumento rápido e simples, mas não afere a extensão da doença48.
Para avaliar o controle da DA e da resposta ao tratamento, podem ser utilizados os mesmos escores de gravidade de forma sequencial ou utilizar outros instrumentos específicos48,49. Para uso sequencial de escore de gravidade é necessário considerar se as variações estão acima da diferença mínima clinicamente importante (MCID) ou se há redução percentual do escore, exemplificado pelo SCORAD 50 ou EASI 75, com redução de 50% ou 75% em relação ao valor inicial, respectivamente48.
Recentemente foram desenvolvidos para o controle da DA o Atopic Dermatitis Control Tool (ADCT) e o Recap of atopic eczema (RECAP), ambos similares em conteúdo e validação e recomendados especialmente para ensaios clínicos. Não há preferência entre eles49, mas até o momento apenas o ADCT apresenta tradução e validação linguística para português do Brasil58.
O instrumento ADCT é formado por seis perguntas e se mostrou ferramenta válida e confiável para avaliar o controle da DA de pacientes maiores de 12 anos, com a capacidade de detectar mudanças clinicamente significativas no controle da doença ao longo do tempo.Varia de 0 (melhor controle da doença) a 24 pontos (pior controle), e a DA é considerada controlada se o escore for inferior a 7 pontos59.
Outros instrumentos de sintomas clínicos percebidos pelo doente e o impacto na qualidade de vida relacionada à saúde também podem ser avaliados na prática clínica e são recomendados para pesquisas. A iniciativa global Harmonising Outcome Measures for Eczema (HOME), com o objetivo de padronizar para ensaios clínicos os quatro principais domínios de desfechos em DA, em última atualização, indica o uso do EASI para avaliação de sinais de gravidade; POEM e escala numérica de pico de prurido em 24 horas para os sintomas referidos pelo paciente; qualidade de vida relacionada à doença por questionários de qualidade de vida de acordo com faixa etária (Dermatology Melhorar a barreira cutâneaLife Quality Index - DLQI para adultos; Children's Dermatology Life Quality Index - CDLQI dos 5 aos 16 anos de idade; Infants' Dermatitis Quality of Life Index - IDQoL para menores de 5 anos), e ADCTou RECAP para controle da atividade da DA49.
TRATAMENTO
Considerando a cronicidade da DA e os diferentes níveis de gravidade, os objetivos do tratamento da DA são os seguintes: (a) reduzir a extensão e a gravidade das lesões; (b) reduzir o prurido e melhorar a qualidade do sono; (c) manter normais as atividades diárias; (d) melhorar a qualidade de vida; (e) maximizar os períodos livres de doença; (f) prevenir as complicações infecciosas; e (g) evitar/minimizar eventos adversos do tratamento.
Cuidados gerais
Nos pacientes com DA leve esses objetivos anteriormente citados são alcançados apenas com a terapia tópica, diferente dos pacientes com DA moderada a grave, cujo tratamento é desafiador. Os princípios gerais incluem melhora da barreira cutânea, eliminação dos fatores desencadeantes, educação e participação ativas dos pacientes e familiares, e tratamento das lesões inflamatórias (Figura 1)1,60.
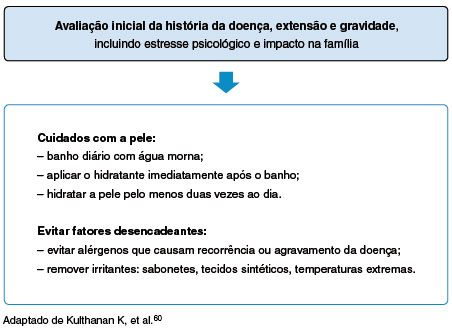
Figura 1
Fluxograma de tratamento inicial da dermatite atópica
Melhorar a barreira cutânea
Os pacientes com DA têm pele xerótica devido ao déficit de função da barreira e balanço desfavorável da perda e retenção de água transepidérmica61. Os hidratantes, quando aplicados regularmente, melhoram a função da barreira cutânea, aumentam a hidratação, reduzem a xerose, o prurido e a inflamação, diminuindo a necessidade do uso de agentes antiinflamatórios1. Estudos clínicos randomizados compararam o uso e não uso do hidratante nos participantes, demonstrando melhora do SCORAD, espaçamento das crises e diminuição do uso de anti-inflamatórios tópicos no grupo que utilizou o hidratante62.
A quantidade ideal que deve ser aplicada em recém-nascidos, lactentes, crianças e adolescentes/ adultos varia de 100, 150, 200 e 500 gramas por semana, respectivamente60,63.
Os hidratantes (Tabela 8) disponíveis para DA têm combinações variáveis de emolientes, substâncias oclusivas e umectantes1. Os emolientes preenchem os espaços entre os corneócitos, mantendo a hidratação; as substâncias oclusivas formam um filme hidrofóbico sobre a epiderme que diminui a evaporação da água e reduz a penetração de agentes irritantes, como alérgenos e toxinas; e os umectantes aumentam a hidratação da camada córnea, preservando a sua estrutura64. Também podem conter ceramidas e ácidos graxos essenciais1.

O hidratante ideal deve conter poucos ingredientes, com conservantes bem tolerados e ser livre de fragrâncias e sensibilizantes (lauril sulfato de sódio, cetil álcool, neomicina, lanolina animal, óleo de amendoim, parabenos, metilizotiazolinona) para evitar reações alérgicas cutâneas. Muitas vezes é necessário testar diferentes produtos até encontrar o que melhore a hidratação cutânea, não provoque ardência e seja da preferência do paciente quanto à textura, loção, creme ou baume. Os produtos tipo loção são preferíveis durante os meses quentes do ano, são de consistência mais fluida, e fáceis de espalhar. Nos períodos frios, os cremes e baumes, de consistência mais grossa, hidratam melhor61,64. As guias recomendam que o hidratante deve ser aplicado duas a três vezes ao dia, em especial com a pele ainda úmida nos primeiros três minutos após o banho, nas áreas da pele com e sem lesões1,65.
Uma nova era de hidratantes traz na sua composição novos ingredientes como canabinoides, lipídeos bioativos, moduladores do microbioma (pré e probióticos) e enzimas antioxidantes. Essas substâncias têm o propósito de exercer efeitos biológicos adicionais na pele: regular a produção de lipídeos, diminuir a transmissão neurossensorial dos sinais de prurido, reverter o estresse oxidativo, reduzir a atividade das células inflamatórias e modular a microbiota da pele66.
Tomar banho diariamente não está associado à piora clínica. O banho reduz os irritantes, bactérias e crostas da pele. Para evitar o ressecamento cutâneo no banho, é indicado o uso de água morna30. O banho pode ter duração de 5 a 10 minutos e ser realizado com sabonetes com pH fisiológico, ou seja, ligeiramente ácido, ou preferencialmente com os syndets 60,61. A guia europeia recomenda o uso de óleos de banho (Tabela 9) nos últimos dois minutos antes do término do banho36.

Identificar os fatores desencadeantes
a) Irritantes não específicos
Contactantes do dia a dia como saliva, suor, cabelo, fricção das roupas sintéticas e resíduo de xampu condicionador e sabonete podem exacerbar a DA.
b) Contactantes
Devemos suspeitar de dermatite de contato quando houver falha no tratamento ou localização atípica de eczema. O agente causal pode ser confirmado pelo teste de contato, em geral os mais comuns são os medicamentos de uso tópico, cosméticos, metal e/ou desinfetantes.
c) Alergia alimentar
Um alimento só deve ser afastado da dieta se for comprovado clinicamente e com exames específicos o seu envolvimento como uma das causas de piora da DA. A alergia alimentar na DA é mais comum na infância, em especial nos primeiros anos de vida e está relacionado a formas mais graves de DA. Os estudos mostram que restrições alimentares (alimentos alergênicos) para gestantes e lactantes não previnem a DA em seus bebês.
d) Aeroalérgenos
A poeira doméstica, pólens e pelos de animais são considerados fatores de piora clínica, mais comuns após os primeiros anos de vida, e essa alergia pode ser confirmada por teste de puntura e/ou pesquisa de IgE sérica específica.
e) Bactérias e fungos
A presença de S. aureus pode ser um dos fatores de exacerbação da DA. A administração de antibióticos não está indicada na ausência de infecção. Alguns estudos apontam melhora clínica com o uso de antifúngico tópico nas lesões da cabeça e pescoço, sugerindo associação de fungos dos gêneros Candida e Malassezia na exacerbação das lesões de DA30,60.
Educação do paciente e familiares
Por ser uma doença crônica e que requer acompanhamento de longo prazo, pacientes e familiares precisam ser educados no intuito de compreender o curso da doença, assim como abordar e prevenir as crises, melhorando a aderência ao tratamento e a qualidade de vida. Intervenções que incluam a educação do paciente diminuem o número de consultas médicas, facilitam a parceria médico e paciente/familiar e restabelecem a dinâmica familiar67. Programas de educação interdisciplinares com pediatras, dermatologistas, alergistas, psicólogos, e enfermagem auxiliam na melhora da qualidade de vida dos pacientes e seus familiares60. No Brasil existem alguns grupos de apoio à DA com este objetivo que podem ser encontrados no site aada.org.br. Este site também contém informações adequadas sobre dermatite atópica destinadas aos pacientes.
Estresse emocional
A DA tem impacto significante sobre a qualidade de vida dos pacientes e de seus familiares. Fatores de estresse e emocionais podem exacerbar a doença. Aconselhamento psicossomático, psicoterapia, técnicas de terapia comportamental e/ou técnicas de relaxamento podem beneficiar no manejo do paciente30,60,67.
Fototerapia
A fototerapia é utilizada no tratamento de várias doenças inflamatórias e imunomediadas desde o início do século passado, principalmente pela observação de que esses pacientes melhoravam no verão. Consiste no uso de espectros de onda ultravioleta (UV) que são irradiadas na pele do paciente durante períodos determinados e controlados. Os espectros utilizados são o ultravioleta A (RUVA), o uso de psoralênicos associados ao UVA (PUVA) e o ultravioleta B (UVB). A categoria do UVB inclui o Broad Band UVB (BB-RUVB), com faixa de 280 a 320 nm, ou seja, toda a faixa de UVB e o Narrow Band UVB (NB-RUVB), também chamado de Faixa Estreita (RUVB-FE), que utiliza a faixa de 301 a 311, um comprimento de onda mais estreito36,68,69.
No tratamento da DA as duas modalidades que existem apresentam eficácia similar: a RUVA de faixa média (340 a 400 nm, também chamada de UVA-1) e a RUVB-FE, sendo essa a mais segura. Os diferentes espectros apresentam resultados diferentes, e a RUVB-FE é indicada para quadros crônicos, e a UVA-1 para os quadros agudos69.
A fototerapia mostra-se eficaz por alterar a cascata de eventos biológicos e que resultam na supressão do sistema imunológico ligado às células T da pele. Especificamente na DA, provoca supressão da resposta dos linfócitos Th2, Th22 e Th1, melhorando a barreira cutânea. Além disso, reduz a colonização por Staphylococcus aureus, diminui o número de infecções e promove redução da produção de toxinas por essa bactéria68,69.
Dentro das modalidades terapêuticas da DA, a fototerapia é recomendada como adjuvante nas falhas dos tratamentos tópicos, antes da utilização de medicações sistêmicas imunossupressoras. Apesar da indicação de uso como adjuvante, a redução do SCORAD em alguns pacientes com uso isolado dessa modalidade terapêutica pode ser superior a 50% nas primeiras 12 semanas70. A sua eficácia foi demonstrada em publicações, sendo que a NB-UVB é recomendada em revisão sistemática recente que avaliou 32 publicações que incluíram 1.219 participantes (5 a 83 anos de idade) e todas as modalidades de fototerapia. A RUVB-FE foi mais efetiva que o placebo, com benefícios na melhora do eczema e na redução do prurido. A falta de uniformidade dos estudos, número pequeno de participantes, e mesmo a falta de avaliação de qualidade de vida dos pacientes ou utilização de escores de gravidade semelhantes dificultam a interpretação dos resultados de eficácia desses trabalhos68,70,71.
A segurança e a eficácia da fototerapia de RUVBFE são demonstradas em pacientes a partir de três anos de idade, porém deve ser evitada em crianças que não consigam seguir corretamente os protocolos de segurança. As taxas de remissão em um ano de terapia foram maiores que 50% para remissão completa ou quase completa, principalmente em crianças com fototipos maiores que III. A dificuldade em realizar a terapêutica em crianças, a falta de uniformidade nas diferentes publicações e principalmente o reduzido número de participantes na faixa etária pediátrica ainda são fatores a serem melhorados72-74.
A terapêutica com fototerapia na DA é padronizada, mas os diferentes tipos de pele, fenótipos da doença e mesmo tolerância à sua realização podem influenciar diretamente nos resultados. Nos casos em que se usa a PUVA-1, para os fototipos de I a III recomenda-se iniciar com 1 J/cm2, e para os fototipos de IV a VI 2 J/cm2, ambos com um incremento de 1 J/cm2 a cada duas ou três sessões. Recomenda-se que as sessões sejam realizadas duas a três vezes por semana. Nos casos de uso da RUVB-FE, a dose inicial é de 100 mj/cm2 sendo que a duração ou a dose total da sessão devem seguir a tabela padrão do fabricante do aparelho69.
Um dos maiores problemas dessa modalidade terapêutica é o custo e principalmente a disponibilidade de equipamentos e médicos capacitados para a sua realização. Em algumas regiões do Brasil essa modalidade não é uma opção viável, onde os equipamentos se encontram em grandes centros ou capitais e a necessidade de sessões frequentes impossibilita a sua aderência, principalmente de pacientes de cidades distantes destes centros. Durante a pandemia de COVID-19, vários relatos de fototerapia com equipamentos em casa aumentaram a abrangência do atendimento de pacientes, podendo o tratamento ser realizando em pacientes mais distantes sem a realização do seu deslocamento, porém o custo destes equipamentos e a segurança do seu uso em casa ainda são fatores de preocupação. O surgimento de novas tecnologias e principalmente aparelhos portáteis e com menor custo são uma possibilidade futura de melhora na assistência desses pacientes68,73,75.
Outra preocupação ainda é a possibilidade de aumento de risco de câncer de pele associado à exposição à fototerapia, principalmente em pacientes pediátricos, sendo o seguimento destes pacientes atualmente em terapêutica essencial para definir esse risco73.
A fototerapia apresenta bons resultados clínicos e aparentemente é segura, porém o tamanho das amostras dos pacientes estudados e mesmo o custo da sua utilização ainda são fatores limitantes para o seu uso rotineiro, principalmente na faixa etária pediátrica.
Tratamento farmacológico
Para o controle da DA é necessária uma abordagem adaptada para cada fase. O plano terapêutico deve ser elaborado em decisão compartilhada com o paciente e sua família. Incluir no plano terapêutico controle de curto, médio e longo prazos, com estratégias para as crises agudas e um roteiro do controle de longo prazo. O objetivo é reduzir a gravidade, o número, e o período das crises76. Idealmente o plano deve ser entregue por escrito, com a medicação a ser utilizada e o tempo de uso77,78.
Tópico
A terapia tópica é necessária para todos os pacientes, independentemente da intensidade da DA. Nas formas graves a terapia tópica deve ser associada aos medicamentos sistêmicos76,77.
Corticosteroides tópicos (CET) e inibidores tópicos da calcineurina (ITC) são indicados como terapia de base. Nos últimos anos novas substâncias tópicas estão disponíveis ou em fase de estudo. São terapias emergentes os inibidores tópicos da fosfodiesterase-4 e inibidores tópicos da Janus kinase76,79, porém ainda não disponíveis no Brasil.
Corticosteroides tópicos
O mecanismo de ação dos CET inclui efeitos anti-inflamatórios, antiproliferativos e imunossupressores. Suprimem a atividade inflamatória e reduzem o número de células inflamatórias e liberação de citocinas, incluindo neutrófilos, monócitos, linfócitos, células de Langerhans, IL-1α, IL-1β, IL-2 e fator de necrose tumoral. Sua eficácia foi demonstrada em diversos veículos e doses, com inúmeros ensaios clínicos randomizados80.
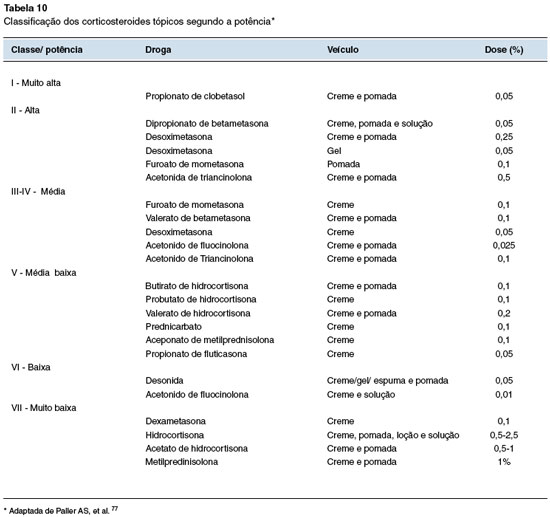
Os CET são a primeira linha de tratamento para as crises agudas de DA, sua efetividade é alcançada com a aplicação correta, na potência indicada para cada região e na quantidade suficiente. Existem sete níveis de potência que variam de muito baixa a muito alta (Tabela 10), e a potência deve ser adaptada à gravidade da lesão e à região a ser tratada77. Evitar corticosteroides potentes em áreas de pele fina, como na face e nas pregas. Nas crianças, preferir corticosteroides de média e baixa potência81.
A aplicação deve iniciar tão logo surjam os sintomas de prurido e eritema, e a duração da terapia tópica com esteroides é guiada pela melhora clínica. Entretanto, seu uso é restrito às áreas com lesões inflamatórias e por períodos de 7 a 14 dias, ou até que as lesões melhorem81. Podem ser aplicados uma ou duas vezes ao dia com semelhante eficácia. O uso de forma proativa é indicado para os casos graves e de difícil controle, ou seja, depois da melhora do surto aplicar em dois dias da semana nas áreas mais resistentes ao tratamento, idealmente após três meses voltar a utilizar de forma reativa81,82.
Não há um padrão universal para quantificar o CET em cada aplicação. Espremer o tubo para cobrir a falange distal de um adulto permite aplicar em uma área de lesão equivalente a duas palmas das mãos81.
Os corticosteroides apresentam efeitos colaterais indesejados, o que facilita a baixa adesão ao seu uso, decorrente sobretudo de corticofobia, e determina resposta clínica insuficiente. Os efeitos colaterais cutâneos incluem atrofia, telangiectasia, estrias, hipertricose e erupção acneiforme76. A maioria destes efeitos melhora com a suspensão da medicação81. Os efeitos colaterais são evitados quando corticosteroides são utilizados corretamente e em associação à hidratação cutânea83.
Inibidores tópicos da calcineurina
Os ITC inibem a transcrição de genes de citocinas pró-inflamatórias, como IL-2, que são dependentes do fator nuclear de ativação de células T. Estão aprovados para o tratamento da DA: tacrolimus pomada 0,03% (em crianças de 2 a 15 anos e adultos) e pomada 0,1% (em maiores de 15 anos e adultos) para DA moderada a grave, e pimecrolimus creme1% para DA leve a moderada em crianças maiores de três meses de idade. São seguros e eficazes de curto prazo (três semanas) e de longo prazo (cinco anos) para o tratamento da DA81.
Os ITC estão indicados para uso em áreas sensíveis de pele mais fina, como pregas cutâneas e face, em duas aplicações diárias nas áreas com lesão. Não causam os efeitos colaterais tópicos observados com os CET, mas pode haver prurido e queimação no local da aplicação83. Alertar o paciente para este sintoma ajuda a evitar a suspensão do tratamento, e se necessário é possível utilizar CET durante alguns dias previamente e depois trocar para imunomodulador, minimizando assim a sensação de ardência81.
Inibidores da fosfodiesterase-4
O uso dos inibidores da fosfodiesterase-4 (PDE4) na DA advém da função intracelular da PDE4 nos queratinócitos. Os leucócitos circulantes dos pacientes com DA têm atividade PDE4, envolvida na produção de citocinas inflamatórias, como IL-4, IL-5, IL-10, IL-13 e prostaglandina E2, pela degradação de monofosfato de adenosina. A PDE4 leva à redução na transcrição de inúmeras citocinas envolvidas na inflamação aguda e crônica, e o crisaborol, um dos inibidores de PDE4, foi avaliado em ensaios clínicos77.
Crisaborol pomada 2% foi aprovado pelo FDA em 2016 para o tratamento de DA leve a moderada em pacientes maiores de dois anos de idade, e em março de 2020 para maiores de três meses83.Vários ensaios clínicos mostraram que o produto é eficaz na melhora das lesões da DA, gravidade da doença e diminuição do prurido, com perfil favorável de segurança76, no entanto pode haver ardência, o que limita seu uso83.
Inibidores tópicos da JAK/STAT
A via Janus kinase/transdutor de sinalização e ativação de transcrição (JAK/STAT) é utilizada por inúmeras citocinas envolvendo aumento da resposta de células Th2, ativação de eosinófilos e supressão de células T reguladoras. Os inibidores JAK/STAT são categorizados como pequenas moléculas que bloqueiam alvos intracelulares77. Seu uso proporciona a prevenção da sinalização de citocinas Th2 que induzem o processo inflamatório na DA. Vários agentes farmacêuticos direcionados a esse grupo de tirosina quinases (incluindo JAK1, JAK2, JAK3 e TYK2) estão sendo avaliados em pacientes com DA, em terapias sistêmicas e tópicas76.
Hipoclorito de sódio
Banhos de hipoclorito de sódio constituem uma técnica antisséptica para o tratamento de DA moderada a grave em pacientes com infecções bacterianas cutâneas de repetição. Tem atividade antiestafilocócica, inclusive contra Staphylococcus aureus resistente à meticilina. Está indicado para infecções ativas de pele e para a terapia de manutenção. O efeito antimicrobiano é atribuído à sua capacidade de causar agregação irreversível de proteínas bacterianas84. Também permite melhorar a função da barreira cutânea81.
Indica-se formular hipoclorito de sódio 5% e colocar 100 mL na água do banho, em uma banheira de 100 litros. Banhar durante 10 minutos, enxaguar, e aplicar hidratantes. É indicado realizá-lo em três dias da semana, por um período mínimo de três meses81.
Revisão sistemática sobre o uso de banhos com hipoclorito de sódio demonstrou que quatro dos cinco estudos observaram diminuição da gravidade da DA84. A eficácia e segurança de longo prazo desse agente antisséptico não é conhecida, principalmente com relação ao uso contínuo84.
Wet Wrap Therapy
A técnica das bandagens úmidas ou wet wrap therapy (WWT) é um adjuvante para tratar as crises e restaurar a barreira cutânea nos pacientes refratários e graves, que não toleram o uso de CET sem as bandagens81. Trata-se da aplicação, depois do banho, de hidratantes em camadas generosas, associados ou não a corticosteroides nas áreas de lesão. Sobre o hidratante é aplicada uma bandagem úmida e a seguir uma bandagem seca. A WWT pode permanecer durante 2 a 10 horas e ser realizada diariamente durante até 14 dias. Ajuda a hidratar a pele, diminui o prurido e representa uma barreira física que dificulta a escoriação da pele.
Em ensaios clínicos a WWT foi mais eficaz do que usar apenas hidratantes85, no entanto, deve-se ter cautela quando CET de alta potência são aplicados, pois a absorção aumentada pode levar à supressão do eixo hipotálamo-hipófise-adrenal. Assim, CET de baixa ou média potência são apropriadas para uso na WWT. Não está claro se a WWT está ou não associada ao aumento do risco de infecções cutâneas76.
Sistêmico
Antibioticoterapia
Pacientes com DA são mais susceptíveis a infeções cutâneas por bactérias, fungos e vírus por diversos motivos, tais como pela inibição de peptídeos antimicrobianos. Entre as bactérias, o S. aureus é o mais associado com a doença, colonizando até 90% dos pacientes, mesmo em áreas sem lesão. A colonização por S. aureus intensifica o processo inflamatório cutâneo devido à liberação de toxinas com ação de superantígenos, que acentuam o prurido. O prurido, por sua vez, favorece a colonização por aureus, retroalimentando o processo81. Pacientes com DA podem ter maiores taxas de colonização por S. aureus resistentes à meticilina (MRSA). Em dois estudos brasileiros, as taxas de colonização por S. aureus e por MRSA foram, respectivamente, de 73,6% e 0% em Porto Alegre (RS), e de 82,9% e 22,2% na cidade do Rio de Janeiro86,87. No Rio de Janeiro, a colonização por MRSA associou-se positivamente com maior gravidade da DA e uso de ciclosporina87.
A colonização da pele por S. aureus pode ser reduzida com tratamento anti-inflamatório efetivo com uso tópico de corticosteroides ou inibidores da calcineurina81. Hipoclorito de sódio (0,005%) possuiu ação antisséptica e pode ser utilizado de forma intermitente na forma de banho de imersão. A presença de crostas amareladas, exsudato e pústulas é característica dos casos de infecção bacteriana e pode ser tratada com antibióticos tópicos (ácido fusídico ou mupirocina). Antibióticos sistêmicos devem ser utilizados em casos de superinfecção bacteriana extensa, com preferência para as cefalosporinas de primeira geração81,88. Antibióticos de maior espectro podem ser empregados em casos de infecção por MSRA88. O uso profilático ou por longos períodos de antibióticos (tópicos ou sistêmicos) não é recomendado.
Imunossupressores
A imunossupressão sistêmica é recurso adotado em adultos e crianças com formas graves de DA refratárias à terapêutica habitual. Apesar da recente introdução de novos e promissores tratamentos como imunobiológicos e pequenas moléculas, como os inibidores de JAK, fármacos imunossupressores orais (IOs) como os corticosteroides, a ciclosporina A (CsA), o metotrexato (MTX), a azatioprina (AZA) e o micofenolato mofetil (MFM) são opções terapêuticas estabelecidas na prática clínica e amplamente disponíveis para estes pacientes89.
Até o momento, entre os IOs habitualmente prescritos para este fim, apenas a ciclosporina é aprovada em nosso meio para maiores de 18 anos. Desse modo, uma parcela significativa de pacientes com DA moderada/grave está sujeita a prescrições "off-label" para o controle de sua doença90,91.
Antes de iniciar uma terapia com imunossupressores, é necessário conhecer as indicações, as contraindicações, os efeitos adversos e as interações medicamentosas, para poder minimizar os riscos do tratamento. Na faixa etária pediátrica com tendência evolutiva de melhora, é importante avaliar riscos e benefícios desses medicamentos, que por vezes podem apresentar efeitos colaterais graves.
a) Corticosteroides sistêmicos
A corticoterapia sistêmica (CS) no tratamento da DA é limitada pelos conhecidos efeitos colaterais e escassez de estudos controlados de longo prazo em adultos e crianças. Assim sendo, seu uso deve ser extremamente cauteloso e restrito a casos excepcionais, e a dose diária não deve exceder 0,5 mg/kg peso corporal de prednisona ou prednisolona67,89.
Alguns pacientes podem se beneficiar de cursos rápidos de CS nas agudizações graves, entretanto a melhora clínica é frequentemente associada à alta taxa de recorrência dos sintomas após a retirada da medicação, resultando em casos de difícil controle. Uso frequente do corticosteroide oral implica na instituição de outras terapias imunossupressoras poupadoras desta terapia89.
b) Ciclosporina A
A CsA é um polipeptídeo cíclico lipofílico que inibe as vias dependentes da calcineurina e determina na diminuição do número de células TCD4+ e TCD8+ ativadas na epiderme, e consequentemente de várias citocinas pró-inflamatórias, tais como IL-2 e IFN-g92.
Estudos de revisão sistemática e metanálise recomendam a CsA como tratamento de primeira linha para DA grave de adultos, crianças e adolescentes para os quais a terapêutica convencional foi ineficaz ou inapropriada89,93.
A dose habitualmente utilizada é de 3-5 mg/kg/ dia, dividida em duas tomadas diárias. Uma vez que a eficácia clínica seja alcançada, a redução de dose de 0,5-1,0 mg/kg/dia a cada duas semanas é recomendada, até atingir-se a dose de manutenção de 2,5-3 mg/kg. A duração do tratamento é variável e deve ser guiada por critérios clínicos de eficácia e tolerância à droga. Ambas as terapias, de curto (três meses) e longo prazo são eficazes, porém não deve exceder dois anos de regime contínuo67.
O monitoramento da função renal e da pressão arterial é imprescindível, e na presença de alterações laboratoriais ou aumento da pressão arterial, a CsA deve ser interrompida, ou sua dose reduzida. Os efeitos nefrotóxicos são mais prováveis de ocorrer se a dose exceder 5 mg/kg do peso corporal, em pacientes com valores elevados de creatinina sérica, idosos ou com o uso prolongado da medicação. Em geral, estes efeitos são revertidos com a suspensão do tratamento. Terapia combinada de CsA com radiação ultravioleta não é recomendada, devido ao risco aumentado de malignidade cutânea e linfoproliferativa93,94.
Embora não existam estudos controlados disponíveis que avaliem a eficácia da vacinação em crianças durante a terapia com CsA, deve-se considerar que as vacinas atenuadas podem não ser eficazes durante o seu uso95. As vacinas com microrganismos vivos atenuados estão contraindicadas.
c) Metotrexato
O MTX é um análogo do ácido fólico capaz de inibir de forma competitiva e irreversível a enzima diidrofolato redutase, impedindo a conversão de diidrofolato a tetraidrofolato. Desta forma, interfere na síntese de DNA e RNA, bem como na proliferação de linfócitos92.
Apesar da escassez de ensaios clínicos randomizados sobre seu uso na DA, o MTX é amplamente utilizado de modo "off-label" como uma opção terapêutica acessível e de baixo custo em pacientes com doença grave e refratária96,97.
Estudos que avaliaram o emprego de MTX em adultos, crianças e adolescentes com DA grave demonstraram que, em geral, a droga é bem tolerada e apresenta bom perfil de segurança, além de eficácia clínica comparável à CsA e azatioprina98-100.
Quando comparado à CsA, o MTX apresenta um início de ação mais lento, no entanto apresenta boa eficácia em terapia prolongada99.
As doses iniciais (5 a 10 mg/semana) e de manutenção (7,5 a 25 mg/semana) variam de acordo com a faixa etária e resposta terapêutica. MTX pode ser administrado por formulação oral ou por via intramuscular, sempre com suplementação semanal de ácido fólico (5 mg) durante o tratamento. Os efeitos colaterais mais comuns incluem distúrbios gastrointestinais e elevação das enzimas hepáticas que são revertidos com a interrupção do tratamento. Reações adversas graves como mielossupressão, hepatotoxicidade e fibrose pulmonar são muito raras101,102. Por se tratar de medicamento teratogênico, homens e mulheres em idade fértil devem usar métodos contraceptivos eficazes durante a terapia. Além disso, o seu uso é contraindicado durante a lactação67.
d) Azatioprina
A AZA é um análogo das purinas que bloqueia a síntese de RNA e DNA interferindo na proliferação de células T e B, e na função das células apresentadoras de antígenos92.
Ensaios clínicos realizados em adultos mostraram, quando comparados ao placebo, melhora de modo significativo dos escores de lesões cutâneas, prurido, perturbação do sono e interferência com as atividades cotidianas e laborais103.
É recomendada como uma opção terapêutica de segunda linha para DA moderada a grave em adultos, especialmente nos casos em que a CsA não é eficaz ou é contraindicada67. O seu início de ação é lento, e os seus benefícios podem não ser aparentes até dois a três meses após o início de tratamento104.
As reações adversas mais comuns com a AZA são náuseas e vômitos, que podem surgir nas primeiras semanas de terapia, e que são revertidos com a descontinuação do medicamento. Efeitos colaterais graves como leucopenia, hepatoxicidade e mielossupressão também podem ocorrer. Esta última é dependente de deficiência parcial ou total da atividade da tiopurina metiltransferase (TPMT). Deste modo, antes da introdução da droga os pacientes devem ser avaliados quanto a atividade e/ou genotipagem desta enzima a fim de reduzir o risco de mielotoxicidade e adaptação da dose terapêutica mais segura92.
O monitoramento laboratorial é essencial durante o tratamento com AZA, e a dose recomendada é de 1 a 3 mg/kg/dia. Estudo realizado com crianças com DA grave e níveis normais de TPMT antes do início do tratamento, não mostrou mielossupressão empregando-se a dose de 2,5-3,5 mg/kg105. Em pacientes adultos com DA moderada/grave, nos quais a dose de AZA foi adaptada à atividade de TPMT (1,0 mg/ kg por dia), ocorreu melhora clínica semelhante em relação aos pacientes com atividade normal de TPMT que receberam 2,5 mg/kg de AZA16. Assim como a CsA, a AZA não deve ser combinada com terapia UV, e proteção UV eficaz deve ser utilizada67.
e) Micofenolato mofetil (MFM)
O MFM é um imunossupressor que inibe a biossíntese de purinas, levando à redução da proliferação linfocitária. A sua utilidade e bom perfil de segurança foi documentada em ensaios clínicos não controlados em adultos, crianças e adolescentes com DA recalcitrante. Entretanto, permanece como opção terapêutica de terceira linha em razão dos poucos estudos de eficácia em larga escala106,107. Eventos adversos gastrointestinais como náusea ou diarreia são os efeitos colaterais mais frequentes durante terapia com MMF, sendo mais comuns durante o início do tratamento. Em função de sua teratogenicidade, pacientes em idade fértil, independentemente de sexo, devem usar métodos contraceptivos eficazes durante a terapia com MFM67.
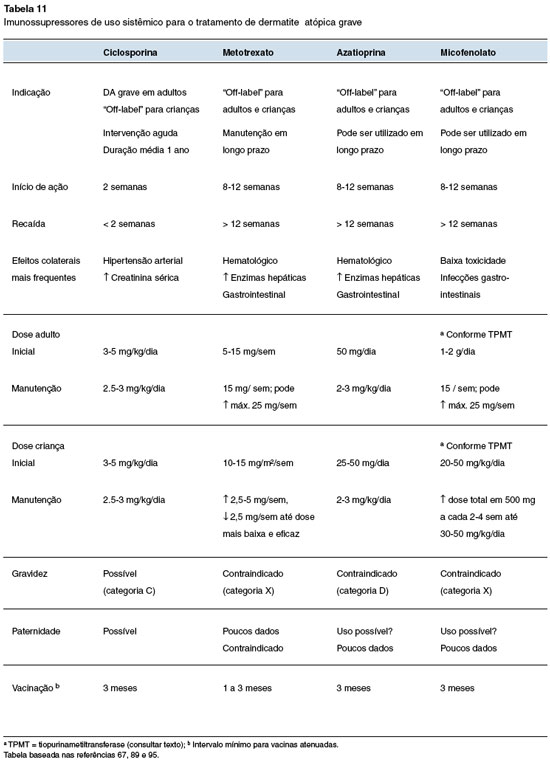
Na Tabela 11 estão descritas as principais características dos imunossupressores de uso sistêmico mais frequentemente utilizados no tratamento da DA grave.
Imunobiológicos
Os imunobiológicos são uma realidade na prática clínica atual e têm ganho cada vez mais espaço no cenário do tratamento das doenças inflamatórias. É uma classe de agentes farmacológicos desenvolvidos por engenharia genética e dirigidos para alvos/ mediadores da inflamação alérgica. O avanço no conhecimento sobre a fisiopatogenia e o advento das terapias alvo-específicas produziu uma revolução no tratamento das doenças imunomediadas108,109.
Os imunobiológicos na atualidade são utilizados para modificar a resposta Th2, bloqueando IgE e as citocinas como IL-4, IL-13 e IL-22, IL-32, IL-17/ IL-23, que têm papel fundamental na patogênese da DA108. São medicamentos seguros e a avaliação clínica (anamnese/exame físico) são suficientes para a sua prescrição a pacientes com formas moderada/ grave de DA não controlada apesar de adequadamente tratados, além de não requerer avaliações laboratoriais mais intensas como ocorre com os imunossupressores.
a) Inibidores de IL-4 e/ou IL-13
- Dupilumabe
Dupilumabe é o primeiro imunobiológico aprovado para uso clínico pela FDA (US Food and Drug Administration), pela EMA (European Medicines Agency) e pela Agência Nacional de Vigilância Sanitária (Anvisa) para o tratamento da DA em crianças maiores de 6 anos, adolescentes e adultos com DA moderada a grave não controlada com as terapias usuais108,109. Esse medicamento também é indicado na asma alérgica e rinossinusopatia crônica associada à polipose nasal110.
Dupilumabe é um anticorpo monoclonal IgG4 específico, recombinante humano que se liga à subunidade alfa dos receptores para IL-4 e IL-13. Isto resulta na dowregulation do receptor que sinaliza a via JAK/STAT responsável pela regulação da expressão de vários genes envolvidos na patogênese da DA109.
Ao bloquear a via de IL-4 e IL-13, dupilumabe bloqueia três mecanismos de doença diferentes e relevantes na DA: a diminuição da função de barreira da pele causada pela dowregulation da proteína filagrina, o switch de classe para IgE causada por citocinas Th2, e a diferenciação global de Th2 do infiltrado inflamatório109,111,112.
A avaliação da eficácia da monoterapia com dupilumabe (dose inicial: 600 mg, seguida de 300 mg a cada 2 semanas, SC) por 16 semanas mostrou redução de 82,5% para o EASI 50, 60,3% para o EASI 75, e 36,5% para o EASI 90. A melhora das lesões cutâneas e a redução do prurido ocorreram duas semanas após o início do tratamento e se manteve por até um ano quando combinado com CET113.
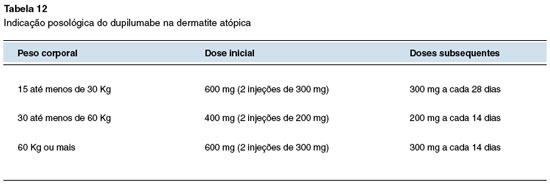
Recomenda-se que o imunobiológico seja administrado de modo concomitante ao tratamento de base que o paciente venha realizando diariamente (higiene ambiental, cuidados com banho, hidratação da pele e medicação tópica, quando necessário) (Tabela 12). Efeitos colaterais com uso da medicação são mínimos, sendo o mais comum a conjuntivite (5% a 28%)114,115.
- Traloquinumabe
Ainda não disponível em nosso meio, o traloquinumabe é anticorpo humanizado e neutralizante de IL-13 por inibir a interação daquela com as subunidades do receptor de IL-13R-alfa109. O traloquinumabe atua interferindo com a dowregulation da filagrina na barreira cutânea promovida pela IL-13. A IL-13 está aumentada na pele lesionada e na pele não lesionada dos indivíduos com DA e se correlaciona com a gravidade da doença108. Documentou-se que a presença de biomarcadores relacionados ao aumento da IL-13 associou-se a melhor resposta ao tratamento como esse biológico116.
- Lebrikizumabe
É outro anticorpo monoclonal humanizado específico e dirigido à IL-13, todavia estudos ainda em andamento não permitem inferir qual regime de dosagem seria o mais adequado, assim como sobre o seu perfil de segurança108.
b) Nemolizumabe
É um anticorpo monoclonal específico dirigido ao receptor alfa da IL-31, principal citocina envolvida no prurido de pacientes com DA. É outro biológico com alta probabilidade de aprovação futura para o tratamento da DA. Em pacientes com DA moderada/ grave, estudo duplo-cego de nemolizumabe contra placebo documentou maior eficácia do biológico no controle do prurido desses pacientes109.
c) Fezakinumabe
O fezakinumabe é um anticorpo monoclonal específico humanizado dirigido contra a IL-22108,117. Em lesões agudas e crônicas da DA documentouse aumento da IL-22 que esteve relacionado à sua gravidade. A IL-22 é produzida pelas células Th22 e age sobre os queratinócitos prejudicando a função da barreira cutânea. Estudo em pacientes com SCORAD ≥ 50 documentou melhora clínica significativa à 12ª semana de tratamento com fezakinumabe, quando comparado ao placebo117. Além disso, houve melhora progressiva em todos os desfechos avaliados até a semana 20, sendo que na 10ª semana o tratamento foi interrompido, o que sugere persistência do efeito terapêutico após a sua interrupção117.
Os imunobiológicos surgem como medicamentos modernos, e o avanço do conhecimento sobre o mecanismo da doença levarão à identificação de endotipos que permitirão escolher os melhores candidatos para estas terapias específicas, contribuindo para uma medicina personalizada ou medicina de precisão na DA.
d) Pequenas moléculas
As pequenas moléculas são fármacos sintéticos de baixo peso molecular com capacidade de difusão intracelular, sendo capazes de interferir com vias de ativação intracelulares. Estes fármacos, quando comparados aos agentes imunossupressores sistêmicos utilizados no tratamento da DA, têm menor potencial de efeitos adversos, pois permitem a supressão mais seletiva das vias imunológicas118. Quando comparados aos imunobiológicos, têm maior potencial de efeitos adversos devido à inibição de um maior número de vias inflamatórias e não estão licenciados para uso em crianças. Na Tabela 13 estão descritas as principais diferenças entre os biológicos e as pequenas moléculas.
Inibidores de JAK
As enzimas JAK são importantes mediadores da ação intracelular de diversas substâncias, entre elas as citocinas inflamatórias (Figura 2). Quando seus receptores são ativados, ocorre a fosforilação das proteínas transdutoras de sinal e ativadoras de transcrição (STAT), que podem ser translocadas para o núcleo celular, induzindo a transcrição e regulação da expressão de genes selecionados. A via estimula a expressão de diversas moléculas e citocinas que facilitam a mobilização de leucócitos e a proliferação celular. Assim, a via JAK/STAT tem papel fundamental para a função das células hematopoiéticas e imunológicas e estudos recentes mostram que tal via pode ter mais suscetibilidade para ativação em pacientes com asma, DA e rinite alérgica, doenças caracterizadas pelo aumento das IL inflamatórias do tipo 2119,120.

Figura 2
A) Sinalização de JAK com citocinas envolvidas na resposta imunológica e doenças imunomediadas.
B) via JAK/STAT
Adaptado de Ahn J, et al.123
Os inibidores de JAK são pequenas moléculas, ou seja, medicamentos com baixo peso molecular, que conseguem facilmente atravessar a membrana celular e atingir alvos intracelulares. Assim, atuam inibindo a sinalização mediada por citocinas específicas, agindo em cadeias de receptores específicos dos subtipos da JAK: JAK-1, JAK-2, JAK-3 e/ou Tirosina-Kinase 2 (TYK-2)121,122.
O prurido crônico depende da sinalização neuronal de JAK-1, e a inibição de JAK parece bloquear diretamente a transmissão neuronal do prurido123. O prurido crônico é dependente da sinalização neuronal de IL-4Ra e JAK-1, e pacientes que falharam em outros tratamentos imunossupressores melhoraram de modo acentuado quando tratadas com inibidores de JAK. O bloqueio JAK/STAT também pode afetar a ativação do eosinófilo, maturação de células B, quimiocinas epidérmicas e numerosas outras vias da fisiopatologia da DA124.
O primeiro medicamento inibidor de JAK aprovado para a prática clínica ocorreu em 2011, para uma doença autoimune125. Seu uso clínico é abrangente, com aplicações desde a oncologia até o combate a doenças virais, e apresenta grande potencial de ação em doenças alérgicas e de resposta imunológica do tipo 2. As perspectivas futuras dos inibidores de JAK vêm sendo cada vez mais estudadas em DA e seu uso tem sido recentemente regulamentado em diversos países, tanto em apresentações tópicas como sistêmicas.
Na Tabela 14 são apresentados os estudos de fase III com inibidores de JAK em DA, sua eficácia e segurança.
O upadacitinibe é um inibidor seletivo da JAK-1 que bloqueia a ação das principais citocinas próinflamatórias. Já foi previamente autorizado para uso em artrite reumatoide em diversos países. Com os promissores resultados publicados, o upadacitinibe foi aprovado para o tratamento de DA em pacientes maiores de 12 anos pela União Europeia em agosto de 2021150, pela FDA em janeiro de 2022151 e pela ANVISA em maio do mesmo ano, para uso com doses iniciais de 15 mg/dia152.
O abrocitinibe é um inibidor seletivo da JAK-1, de ação sistêmica e administração por via oral. O medicamento também já está aprovado para uso em pacientes com DA pela FDA para pacientes maiores de 18 anos nos Estados Unidos, desde janeiro de 2022153. Esse fármaco está em processo de regulamentação no Brasil.
O baricitinibe é um inibidor da JAK-1 e JAK-2 e seu uso em DA vem sendo estudado desde 2016, quando se iniciaram os estudos de fase 2. Apesar de ter eficácia menor em relação aos outros dois inibidores de JAK orais com estudos de fase 3 para DA, o baricitinibe foi o primeiro inibidor de JAK aprovado para o tratamento do eczema na Europa, em setembro de 2020154, e está disponível em nosso país.
O ruxolitinibe é um inibidor tópico da JAK-1 e JAK-2. Foi desenvolvido para otimizar a ação do medicamento diretamente nas áreas afetadas e diminuir os riscos de efeitos adversos sistêmicos. Em setembro de 2021, o ruxolitinibe foi aprovado para uso em DA pela FDA, sendo o primeiro inibidor de JAK aprovado para uso nos Estados Unidos, na concentração de 1,5% em pacientes acima dos 12 anos147.
O delgocitinibe é um inibidor pan-JAK, ou seja, inibe JAK-1, JAK-2, JAK-3 e TYK-2, de apresentação tópica. O delgocitinibe foi aprovado para uso tópico em DA no Japão, na concentração 0,25% e 0,5% para a população adulta e crianças maiores de dois anos de idade desde março de 2021155.
Considerando o potencial de eventos adversos observados nos ensaios clínicos pivotais com os inibidores da JAK na DA, é necessária avaliação clínica e laboratorial antes do início do tratamento para a avaliação de contraindicações, bem como o monitoramento de ocorrências clínicas e alterações laboratoriais ao longo do tratamento. Na avaliação clínica, é importante investigar o histórico e fatores de risco para doenças infecciosas (tuberculose, Herpes zoster, hepatites virais e infecção pelo HIV), avaliar fatores de risco para tromboembolismo e histórico de neoplasias malignas. A avaliação laboratorial inicial deve incluir hemograma, função hepática, função renal, lipidograma, marcadores de hepatite virais (B e C) e sorologia anti-HIV. O monitoramento de toxidade laboratorial inclui como exames básicos o hemograma, função hepática, função renal e lipidograma, que devem ser realizados a cada três meses, e exames adicionais, de acordo com o cenário clínico. A investigação de tuberculose ativa e latente deve ser realizada através de PPD, radiografia de tórax e ensaio de liberação de interferon-gama (IGRA) pré-tratamento e ao longo do tratamento, caso haja indicação clínica. É recomendável ainda que o calendário de imunizações esteja completo antes do início do tratamento156.
RECOMENDAÇÕES GERAIS PARA A TERAPIA SISTÊMICA
A terapia sistêmica, segundo as recomendações de diretrizes nacionais e internacionais, deve ser reservada para a DA grave, ou seja, pacientes que não obtêm controle adequado da doença com a terapia tópica otimizada e a fototerapia. A avaliação da gravida-de deve ser realizada por instrumentos padronizados e validados amplamente utilizados, como o SCORAD e o EASI. É importante também avaliar o impacto na qualidade de vida dos pacientes pelo DLQI e CDLQI. Pacientes com formas moderadas de DA, mas com grande impacto na qualidade de vida, também são candidatos à terapia sistêmica64,156,157.
Antes de iniciar a terapia sistêmica é importante rever o diagnóstico diferencial, excluindo condições graves que mimetizam a DA, como linfoma de células T e erros inatos da imunidade; avaliar a adesão ao tratamento; investigar a participação de fatores desencadeantes e agravantes, como exposição a alérgenos (inalantes, alimentos, contactantes), irritantes e aspectos psicológicos. A escolha da terapia sistêmica deve ser personalizada e participativa, levando em conta a faixa etária, comorbidades, perfil de eventos adversos, necessidade de monitoramento laboratorial, preferências do paciente (medicação oral x injetável) e o cenário local de acesso aos diversos medicamentos. Na Tabela 15 estão descritas as principais características dos medicamentos para terapia sistêmica na DA licenciados no país, incluindo aqueles com uso "off-label"157.
CONSIDERAÇÕES FINAIS
A DA é doença muito prevalente na infância e ten-de à remissão com o decorrer do tempo na maioria dos casos. As alterações da barreira cutânea com possibilidade de penetração de alérgenos e patógenos e a consequente desregulação imunológica são as principais causas para explicar o processo inflamatório que se estabelece no nível da pele158.
A partir do dano epitelial, muitas células e produtos celulares estão envolvidos nesse processo. Sabemos atualmente que células Th2, Th17, Th22 e ILC-2 são aquelas que participam mais ativamente da fisiopatogenia da DA. Muitos estudos têm mostrado a importância da liberação de várias citocinas por essas células, cujas ações, diretas ou indiretas, causam maior diferenciação epidérmica e disfunção mais grave da barreira cutânea. Vale ressaltar que muitas destas citocinas têm também a função de ativar células que liberam produtos que iniciam, agravam ou perpetuam o processo inflamatório25.
Vários medicamentos têm sido utilizados no senti-do de inibir a inflamação que se estabelece na derme. Os corticosteroides e os inibidores da calcineurina de uso tópico são ainda as drogas mais utilizadas como agentes anti-inflamatórios nas etapas iniciais do tratamento.
Nos últimos anos, a partir do entendimento da importância do processo inflamatório, os imunossupressores sistêmicos como ciclosporina, azatioprina, metotrexato e micofenolato mofetil passaram a ser o último recurso na inibição desse processo. O seu uso requer cuidados especiais em função da possibilidade de efeitos colaterais significativos, principalmente quando prescritos por tempo prolongado.
É importante citar que outros medicamentos com atividade anti-inflamatória, como os corticosteroides sistêmicos podem ser prescritos em situações muito particulares e por poucos dias75.
O advento dos imunobiológicos e inibidores da JAK no arsenal do tratamento da DA grave a moderada possibilita hoje um tratamento seguro e eficaz para essa população de pacientes. Considerando o alto custo desses fármacos, as diretrizes nacionais e internacionais recomendam o uso nas formas graves de DA e baseado em critérios bem definidos de gravidade e falha na terapia tópica otimizada22,159.
Os imunobiológicos inibem a ação de citocinas pró-inflamatórias ou seus receptores. O dupilumabe (anti IL-4/IL-13) foi o primeiro imunobiológico a ser utilizado e muitos outros vêm sendo testados em ensaios clínicos de fase III. Alguns já estão disponibilizados ou em breve serão liberados para uso clínico, tais como: anti-TSLP, anti-IL-13, anti-IL31, anti-IL33 e anti-IL17159. As pequenas moléculas, os inibidores da JAK, também já vêm sendo prescritos com ótimos resultados83. Essas novas classes de medicamentos mais recentes diminuem a gravidade da doença reduzindo o processo inflamatório, melhorando o aspecto da pele e o prurido cutâneo, o que vem sendo comprovado utilizando-se ferramentas como o SCORAD e o EASI.
Uma das expectativas para os próximos anos é a de termos uma maior compreensão dos fatores que favorecem o desenvolvimento da doença, como a genética e epigenética, os expossomas externo e interno e outros que fazem parte da sua fisiopatologia160. Esperamos também que no futuro sejam identificados biomarcadores que possibilitem uma abordagem individualizada com base nos fenótipos e endotipos, bem como novas alternativas terapêuticas que nos auxiliem no melhor manejo dessa doença extremamente complexa161,162.
REFERÊNCIAS
1. Langan SM, Irvine AD, Weidinger S. Atopic dermatitis. Lancet. 2020;396:345-60. doi: 10.1016/S0140-6736(20)31286-1.
2. Hanifin JM, Rajka G. Diagnostic features of atopic dermatitis. Acta Derm Venereol. 1980;92:44-7.
3. Williams HC, Burney PGJ, Hay RJ, Archer CB, Shipley MJ, Hunter JJA, et al. The UK Working Party's Diagnostic Criteria for Atopic Dermatitis.I.Derivation of a minimum set of discriminators for atopic dermatitis. Br J Dermatol. 1994;131:383-96. doi: 10.1111/j.13652133.1994.tb08532.x.
4. Eichenfield LF, Tom WL, Chamlin SL, Feldman SR, Hanifin JM, Simpson EL, et al. Guidelines of care for the management of atopic dermatitis: section 1. Diagnosis and assessment of atopic dermatitis. J Am Acad Dermatol. 2014;70:338-51. doi: 10.1016/j.jaad.2013.10.010.
5. Hughes AJ, Tawfik SS, Baruah KP, O'Toole EA, O'Shaughnessy RFL. Tape strips in dermatology research. Br J Dermatol. 2021;185(1):26-35. doi: 10.1111/bjd.19760.
6. Hadi HA, Tarmizi AI, KhalidKA, GajdácsM,AslamA,JamshedS.The Epidemiology and Global Burden of Atopic Dermatitis: A Narrative Review. Life (Basel). 2021;11(9):936. doi: 10.3390/life11090936.
7. Odhiambo JA, Williams HC, Clayton TO, Robertson CF, Asher MI; ISAAC Phase Three Study Group. Global variations in prevalence of eczema symptoms in children from ISAAC Phase Three. J Allergy Clin Immunol. 2009;124(6):1251-8.e23. doi: 10.1016/j.jaci.2009.10.009.
8. Solé D, Mallol J, Wandalsen DF, Aguirre V, Latin American ISAAC Phase 3 Study Group. Prevalence of symptoms of eczema in Latin America: results of the International Study of Asthma and Allergies in Childhood (ISAAC) Phase 3. J Investig Allergol Clin Immunol. 2010,20:311-23.
9. Mallol J, García-Marcos L, Solé D, Brand P, EISL Study Group. International prevalence of recurrent wheezing during the first year of life: variability, treatment patterns and use of health resources. Thorax. 2010;65(11):1004-9. doi: 10.1136/thx.2009.115188.
10. Bylund S, Kobyletzki LB, Svalstedt M, Svensson Å.Prevalence and Incidence of Atopic Dermatitis: A Systematic Review. Acta Derm Venereol. 2020;100(12):adv00160. doi: 10.2340/00015555-3510.
11. Antunes AA, Solé D, Carvalho VO, Bau AEK, Kuschnir FC, Mallozi MC, et al. Guia prático de atualização em dermatite atópica - Parte I: etiopatogenia, clínica e diagnóstico. Posicionamento conjunto da Associação Brasileira de Alergia e Imunologia e da Sociedade Brasileira de Pediatria.Arq Asma Alergia Imunol.2017;1(2):131-56. doi: 10.5935/2526-5393.20170019.
12. Pires MC, Santos RNR. Dermatites e Eczemas. In: Sittart JAS & Pires MC.Dermatologia na Prática Médica.São Paulo:Roca;2007. p.31-62.
13. Ramírez-Marín HA, Silverberg JI. Differences between pediatric and adult atopic dermatitis. Pediatr Dermatol. 2022;39(3):345-53. doi: 10.1111/pde.14971.
14. Bieber T, D'Erme AM, Akdis CA, Traidl-Hoffmann C, Lauener R, Schäppi G, et al. Clinical phenotypes and endophenotypes of atopic dermatitis: Where are we, and where should we go? J Allergy Clin Immunol. 2017;139(4S):S58-S64. doi: 10.1016/j.jaci.2017.01.008.
15. Tokura Y, Hayano S.Subtypes of atopic dermatitis:From phenotype to endotype. Allergol Int. 2022;71(1):14-24. doi: 10.1016/j.alit.2021.07.003.
16. Roduit C, Frei R, Depner M, Karvonen AM, Renz H, Braun-Fahrländer C, et al. Phenotypes of Atopic Dermatitis Depending on the Timing of Onset and Progression in Childhood. JAMA Pediatr. 2017;171(7):655-62. doi: 10.1001/jamapediatrics.2017.0556.
17. Fania L, Moretta G, Antonelli F, Scala E, Abeni D, Albanesi C, et al. Multiple roles for cytokines in atopic dermatitis: from pathogenic mediators to endotype-specific biomarkers to therapeutic targets. Int J Mol Sci. 2022;23:2684-701. doi: 10.3390/ijms23052684.
18. Girolomoni G, de Bruin-Weller M, Aoki V, Kabashima K, Deleuran M, Puig L, et al. Nomenclature and clinical phenotypes of atopic dermatitis. Ther Adv Chronic Dis. 2021 Mar 26;12:20406223211002979. doi: 10.1177/20406223211002979.
19. Weidinger S, Beck L, Bieber T, Kabashima K, Irvine A. Atopic Dermatitis.Nat Rev Dis Primers.2018;4(1):1.doi:10.1038/s41572018-0001-z.
20. Shaker M, Murray RGP, Mann JA. The ins and outs of an 'outside-in' view of allergies: atopic dermatitis and allergy prevention. Curr Opin Pediatr. 2018;30(4):576-81. doi: 10.1097/MOP.0000000000000646.
21. Cork M, Robinson D, Vasilopoulos Y, Ferguson A, Moustafa M, MacGowan A, et al. News perspectives on epidermal barrier dysfunctional in atopic dermatitis:gene - environment interactions. J Allergy Clin Immunol. 2006;118(1):3-21. doi: 10.1016/j.jaci.2006.04.042.
22. Kabashima K.New concept of the pathogenesis of atopic dermatitis interplay among barrier, allergy, and pruritus as a trinity.J Dermatol Sci. 2013;70(3):3-11. doi: 10.1016/j.jdermsci.2013.02.001.
23. De Benedetto A, Rafaels NM, Mc Girl L, Ivanov A, Ivanov AI, Georas SN, et al.Tight junctions in patients with atopic dermatitis.J Allergy Clin Immunol. 2011;127:773-88. doi: 10.1016/j.jaci.2010.10.018.
24. Paller AS, Kong HH, SeedP, Naik S, Scharschmidt TC, Gallo RL, et al. The microbiome in patients with atopic dermatitis. J Allergy Clin Immunol. 2019; 143:26-35. doi: 10.1016/j.jaci.2018.11.015.
25. Simon D, Wollenberg A, Reinz H, Simon HU. Atopic dermatitis: Collegium Internationale Allergologicum (CIA) Update 2019. Int Arch Immunol. 2019; 178(3):207-18. doi: 10.1159/000497383.
26. Czarnovwicki T, He H, Krueger JG, Guttman-Yassky E. Atopic dermatitis endotypes and implications for targeted therapeutics. J Allergy Clin Immunol. 2019;143:1-11. doi: 10.1016/j. jaci.2018.10.032.
27. Sroka-TomaszewskaJ,Trzeciak M. Molecular Mechanisms of Atopic Dermatitis Pathogenesis. Int J Mol Sci. 2021;22(8):4130. doi: 10.3390/ijms22084130.
28 .Bae JS, Da F, Liu R, He L, Lv H, Fisher EL, et al. Contribution of Staphylococcal Enteroxin B to Staphylococcus aureus Systemic Infection. J Infect Dis. 2021;223(10):1766-75. doi: 10.1093/infdis/jiaa584.
29. Yue H, Umehara Y, Trujillo-Paez JV, Peng G, Nguyen HLT, Chieosilapatham P, et al. Exogenous factors in the pathogenesis of atopic dermatitis: Irritants and cutaneous infections. Clin Exp Allergy. 2021;51:382-92. doi: 10.1111/cea.13820.
30. Katoh N, Ohya Y, Ikeda M, Ebihara T, Katayama I, Saeki H, et al. Japanese guidelines for atopic dermatitis 2020. Allergol Int. 2020;69(3):356-69. doi: 10.1016/j.alit.2020.02.006.
31. Nguyen GH, Andersen LK, Davis MDP. Climate change and atopic dermatitis: is there a link? Int J Dermatol. 2019;58(3):279-282. doi: 10.1111/ijd.14016.
32. Domíngues O, Plaza AM, Alvaro M. Relantionship Between Atpoic Dermatitis and Food Allergy. Cur Pediatr Rev. 2020;16(2):115-22. doi: 10.2174/1573396315666191111122436.
33. Zhong Y, Samuel M, van Bever H, Tham EH. Emollients in infancy to prevent atopic dermatitis:A systematic review and meta-analysis. Allergy. 2022;77(6):1685-99. doi: 10.1111/all.15116.
34. Oykhman P, Dookie J, Al-Rammahy H, de Benedetto A, Asiniwasis RN, LeBovidge J. Dietary Elimination for the Treatment of Atopic Dermatitis: A Systematic Review and Meta-analysis. J Allergy Clin Immunol Pract. 2022 Oct;10(10):2657-2666.e8. doi: 10.1016/j.jaip.2022.06.044
35. Byrd AL, Belkaid Y, Segre JA. The human skin microbiome. Nat Rev Microbiol.2018;16(3):143-55. doi: 10.1038/nrmicro.2017.157
36. Wollenberg A, Barbarot S, Bieber T, Christen-Zaech S, Deleuran M, Fink-Wagner A. Consensus-based European guidelines for treatment of atopic eczema (atopic dermatitis) in adults and children: part I. J Eur Acad Dermatol Venereol. 2018;32(5):657-82. doi: 10.1111/jdv.14891.
37. Hiragun T, Ishii K, Hiragun M, Suzuki H, Kan T, Mihara S, et al. Fungal protein MGL_1304 in sweat is an allergen for atopic dermatitis patients. J Allergy Clin Immunol. 2013;132:608e15. doi: 10.1016/j. jaci.2013.03.047.
38. SugitaT,Suto H, Unno T, Tsuboi R,Ogwa h, Shinoda T,etal.Molecular analysis of Malassezia microflora on the skin of atopic dermatitis patients and healthy subjects.J Clin Microbiol.2001;39(10):3486-90. doi: 10.1128/JCM.39.10.3486-3490.2001.
39. Tamagawa-Mineoka R, Katoh N.Atopic Dermatitis:Identification and Management of Complicating Factors. Int J Mol Sci. 2020;21:2671. doi:10.3390/ijms21082671.
40. Barrett M, Luu M. Differential Diagnosis of Atopic Dermatitis. Immunol Allergy Clin North Am. 2017;37(1):11-34. doi: 10.1016/j.iac.2016.08.009.
41. Fishbein AB, Silverberg JI, Wilson EJ, Ong PY. Update on Atopic Dermatitis: Diagnosis, Severity Assessment, and Treatment Selection. J Allergy Clin Immunol Pract. 2020;8(1):91-101. doi: 10.1016/j.jaip.2019.06.044.
42. Brar KK, Nicol NH, Boguniewicz M. Strategies for Successful Management of Severe Atopic Dermatitis. J Allergy Clin Immunol Pract. 2019;7(1):1-16. doi: 10.1016/j.jaip.2018.10.021.
43. Stadler PC, Renner ED, Milner J, Wollenberg A. Inborn Error of Immunity or Atopic Dermatitis: When to be Concerned and How to Investigate. J Allergy Clin Immunol Pract. 2021;9(4):1501-7. doi: 10.1016/j.jaip.2021.01.037.
44. Mortz CG, Brockow K, Bindslev-Jensen C, Broesby-Olsen S.It looks like childhood eczema but is it? Clin Exp Allergy.2019;49(6):744-53. doi: 10.1111/cea.13381.
45. Vaseghi-Shanjani M, Smith KL, Sara RJ, Modi BP, Branch A, Sharma M, et al. Inborn errors of immunity manifesting as atopic disorders.J Allergy Clin Immunol.2021;148(5):1130-9.doi:10.1016/j.jaci.2021.08.008.
46. Huang E, Ong PY.Severe Atopic Dermatitis in Children.Curr Allergy Asthma Rep. 2018;18(6):35. doi: 10.1007/s11882-018-0788-4.
47. Cinicola BL, Corrente S, Castagnoli R, Lougaris V, Giardino G, Leonardi L, et al.Primary atopic disorders and chronic skin disease. Pediatr Allergy Immunol. 2022;33(Suppl 27): 65-8. doi: 10.1111/pai.13633.
48. Chopra R, Silverberg JI. Assessing the severity of atopic dermatitis in clinical trials and practice.Clin Dermatol.2018;36(5):606-15.doi: 10.1016/j.clindermatol.2018.05.012.
49. Williams HC, Schmitt J, Thomas KS, Spuls PI, Simpson EL, Apfelbacher CJ, et al.The HOME Core outcome set for clinical trials of atopic dermatitis.J Allergy Clin Immunol.2022;149(6):1899-911. doi: 10.1016/j.jaci.2022.03.017.
50. Simpson E, Bissonnette R, Eichenfield LF, Guttman-Yassky E, King B, Silverberg JI, et al.The Validated Investigator Global Assessment for Atopic Dermatitis (vIGA-AD): The development and reliability testing of a novel clinical outcome measurement instrument for the severity of atopic dermatitis.J Am Acad Dermatol.2020;83(3):839-46. doi: 10.1016/j.jaad.2020.04.104.
51. European Task Force on Atopic Dermatitis.Severity Scoring of Atopic Dermatitis:The SCORAD Index.Dermatology.1993;186:23-31.doi: 10.1159/000247298.
52. Oranje AP, Glazenburg EJ, Wolkerstorfer A, de Waard-Van Der Spek FB. Practical issues on interpretation of scoring atopic dermatitis: The SCORAD index, objective SCORAD and the three-item severity score. Br J Dermatol. 2007;157(4):645-8. doi: 10.1111/j.13652133.2007.08112.x.
53. Stalder JF, Barbarot S, Wollenberg A, Holm EA, de Raeve L, Seidenari S, et al. Patient-Oriented SCORAD (PO-SCORAD): A new self-assessment scale in atopic dermatitis validated in Europe. Allergy: Eur J Allergy Clin Immunol. 2011;66(8):1114-21. doi: 10.1111/j.1398-9995.2011.02577.x.
54. Hanifin JM, Thurston M, Omoto M, Cherill R, Tofte SJ, Graeber M. The eczema area and severity index (EASI): assessment of reliability in atopic dermatitis.EASI Evaluator Group.Exp Dermatol. 2001;10(1):11-8. doi: 10.1034/j.1600-0625.2001.100102.x.
55. Hanifin JM, Baghoomian W, Grinich E, Leshem YA, Jacobson M, Simpson EL. The Eczema Area and Severity Index -A Practical Guide. Dermatitis. 2022;33(3):187-92. doi: 10.1097/DER.0000000000000895.
56. Spuls PI, Gerbens LAA, Simpson E, Apfelbacher CJ, Chalmers JR, Thomas KS, et al.Patient-Oriented Eczema Measure (POEM), a core instrument to measure symptoms in clinical trials: a Harmonising Outcome Measures for Eczema (HOME) statement.Br J Dermatol. 2017;176:979-84. doi: 10.1111/bjd.15179.
57. University of Nottingham.POEM - Patient Oriented Eczema Measure [Internet].Disponível em: www.nottingham.ac.uk/research/groups/cebd/resources/poem.aspx. Acessado em: 15/07/2022.
58. Atopic dermatitis control tool (ADCT) [Internet]. Disponível em: www.adcontroltool.com. Acessado em: 15/07/2022.
59. Simpson E, Eckert L, Gadkari A, Mallya UG, Yang M, Nelson L, et al.Validation of the Atopic Dermatitis Control Tool (ADCT©) using a longitudinal survey of biologic-treated patients with atopic dermatitis. BMC Dermatol. 2019;19(1):15. doi: 10.1186/s12895-019-0095-3.
60. Kulthanan K, Tuchinda P, Nitiyarom R, Chunharas A, Chantaphakul H, AunhachokeK, et al.Clinical practice guidelines for the diagnosis and management of atopic dermatitis. Asian Pac J. Allergy Immunol.2021;39:145-55. doi: 10.12932/AP-010221-1050.
61. Waldman AR, Ahluwalia J, Udkoff J, Borok JF, Eichenfield LF. Atopic Dermatitis. Pediatr Rev. 2018; 39(4):180-91. doi: 10.1542/pir.2016-0169.
62. Van Zurren EJ, Fedorowicz Z, Arents BWM. Emollients and moisturisers for eczema: abridged Cochrane systematic review including GRADE assessments.Br J Dermatol.2017;177(5):1256-71. doi: 10.1111/bjd.15602.
63. Eichenfield LF, Boguniewicz M, Simpson EL, Russel Jj, Block JK, Feldman SR, et al. Translating Atopic Dermatitis Management Guidelines Into Practice for Primary Care Providers. Pediatrics. 2015;136(3):554-65. doi: 10.1542/peds.2014-3678.
64. Carvalho VO, Solé D, Antunes AA, Bau AEK, Kuschnir FC, Mallozi MC, et al. Guia prático de atualização em dermatite atópica - Parte II:abordagem terapêutica.Posicionamento conjunto da Associação Brasileira de Alergia e Imunologia e da Sociedade Brasileira de Pediatria. Arq Asma Alergia Imunol. 2017;1(2):157-82. doi: 10.5935/2526-5393.20170020.
65. ePoidevin LM, Lee DE, Shi VY. A comparison of international management guidelines for atopic dermatitis. Pediatr Dermatol. 2018;36(1):36-65. doi: 10.1111/pde.13678.
66. Chandan N, Rajkumar JR, Shi VY, Lio PA.A new era of moisturizers.J Cosmet Dermatol. 2021;20(8):2425-30. doi: 10.1111/jocd.14217.
67. Wollenberg A, Barbarot S, Bieber T, Christen-Zaech S, Deleuran M, Fink-Wagner A, et al. Consensus-based European guidelines for treatment of atopic eczema (atopic dermatitis) in adults and children: part II. J Eur Acad Dermatol Venereol. 2018;32:850-78. doi: 10.1111/jdv.14888.
68. Myers E, Kheradmand S, Miller R. An Update on Narrowband Ultraviolet B Therapy for the Treatment of Skin Diseases. Cureus. 2021;13(11):e19182. doi: 10.7759/cureus.19182
69. Sociedade Brasileira de Dermatologia. Manual Prático de Fototerapia. 1ªed. Rio de Janeiro: SBD; 2020. p. 86.
70. Torres T, Ferreira EO, Gonçalo M, Mendes-Bastos P, Selores M, Filipe P.Update on Atopic Dermatitis.Acta Med Portug.2019;32(9):606-13. doi: 10.20344/amp.11963.
71. Musters AH, Mashayekhi S, Harvey J, Axon E, Lax SJ, Flohr C, et al. Phototherapy for atopic eczema.Cochrane Database of Systematic Rev. 2021;10(10): CD013870. doi: 10.1002/14651858.CD013870. pub2.
72. Hunjan MK, Brockley JR, Buka R,Ramesh R.Treatment ofpaediatric eczema with narrowband ultraviolet light B therapy. Photodermatol Photoimmunol Photomed. 2021;37(2):105-10. doi: 10.1111/phpp.12615.
73. Kemény L, Varga E, Novak Z.Advances in phototherapy for psoriasis and atopic dermatitis.Exp Rev Clin Immunol.2019;15(11):1205-14. doi: 10.1080/1744666X.2020.1672537.
74. Seccombe E, Wynne MD, Clancy C, Godfrey KM, Fityan A. A retrospective review of phototherapy in children, at a tertiary paediatric dermatology unit. Photodermatol Photoimmunol Photomed. 2021;37(1):34-8. doi: 10.1111/phpp.12604.
75. Sidbury R, Davis DM, Cohen DE, Cordoro KM, Berger TG, Bergman JN, et al.Guidelines of care for the management of atopic dermatitis: section 3. Management and treatment with phototherapy and systemic agents. J Amer Acad Dermatol. 2014;71(2):327-49. doi: 10.1016/j.jaad.2014.03.030.
76. Diaz A, Guttman-Yassky E. Topical agents for the treatment of atopic dermatitis. Expert Rev Clin Immunol. 2019;15(4):369-82. doi: 10.1080/1744666X.2019.1564038.
77. Paller AS, Mancini AJ. Hurwitz Clinical Pediatric Dermatology: a textbook of skin disorders of childhood and adolescence. 6ª ed. Nova Iorque: Elsevier; 2022.
78. Chisolm SS, Taylor SL, Balkrishnan R, Feldman SR.Written action plans: potential for improving outcomes in children with atopic dermatitis.J Am Acad Dermatol.2008;59(4):677-83.doi:10.1016/j.jaad.2008.04.025.
79. Bissonnette R, Papp KA, Poulin Y, Gooderham M, Raman M, Mallbris L, et al.Topical tofacitinib for atopic dermatitis:a phase IIa randomized trial. Br J Dermatol. 2016;175(5):902-11. doi: 10.1111/bjd.14871.
80. Hoare C, Li Wan Po A, Williams H. Systematic review of treatments for atopic eczema. Health Technol Assess. 2000;4(37):1-191.
81. Wollenberg A, Christen-Zäch S, Taieb A, Paul C, Thyssen JP, de Bruin-Weller M, et al.ETFAD/EADV Eczema task force 2020 position paper on diagnosis and treatment of atopic dermatitis in adults and children.J Eur Acad Dermatol Venereol.2020;34(12):2717-44. doi: 10.1111/jdv.16892.
82. Katoh N. Future perspectives in the treatment of atopic dermatitis. J Dermatol. 2009;36(7):367-76. doi: 10.1111/j.13468138.2009.00662.x.
83. Chovatiya R, Paller AS. JAK inhibitors in the treatment of atopic dermatitis. J Allergy Clin Immunol. 2021;148(4):927-40. doi: 10.1016/j.jaci.2021.08.009.
84. Chopra R, Vakharia PP, Sacotte R, Silverberg JI. Efficacy of bleach baths in reducing severity of atopic dermatitis:A systematic review and meta-analysis. Ann Allergy Asthma Immunol. 2017;119(5):435-40. doi: 10.1016/j.anai.2017.08.289.
85. Devillers AC, Oranje AP.Efficacy and safety of 'wet-wrap' dressings as an interventiontreatment in childrenwith severe and/orrefractory atopic dermatitis: a critical review of the literature. Br J Dermatol. 2006;154(4):579-85. doi: 10.1111/j.1365-2133.2006.07157.x.
86. Petry V, Lipnharski C, Bessa G, Silveira V, Weber M, Bonamigo R, et al. Prevalence of community-acquired methicillin-resistant Staphylococcus aureus and antibiotic resistance in patients with atopic dermatitis in Porto Alegre, Brazil. Int J Dermatol. 2014;53:731-5. doi: 10.1111/ijd.12020.
87. Abad E, Ferreira D, Cavalcante F, Saintive S, Goudouris E, Prado E, etal.Highincidence ofacquiring methicillin-resistant Staphylococcus aureus in Brazilian children with Atopic Dermatitis and associated risk factors. J Microbiol Immunol Infect. 2020;53:724-730. doi: 10.1016/j.jmii.2018.12.014.
88. Briscoe C, Reich P, Fritz S, Coughlin C. Staphylococcus aureus antibiotic susceptibility patterns in pediatric atopic dermatitis.Pediatr Dermatol. 2019;36:482-5. doi: 10.1111/pde.13867.
89. Siegels D, Heratizadeh A, Abraham S, Binnmyr J, Brockow K, Irvine AD, et al. Systemic treatments in the management of atopic dermatitis: A systematic review and meta-analysis. Allergy. 2021;76(4):1053-76. doi: 10.1111/all.14631.
90. Brasil.Agência Nacional de Vigilância Sanitária (ANVISA).Bulário eletrônico [Internet].Disponível em: https://consultas.anvisa.gov.br/#/bulario/q/?nomeProduto=CICLOSPORINA. Acessado em: 17/08/2022.
91. Simpson EL, Bruin-Weller M, Flohr C, Ardern-Jones MR, Barbarot S, Deleuran M, et al. When does atopic dermatitis warrant systemic therapy? Recommendations from an expert panel of the International Eczema Council. J Am Acad Dermatol. 2017;77(4):623-33. doi: 10.1016/j.jaad.2017.06.042.
92. Davari DR, Nieman EL, McShane DB, Morrell DS. Current Perspectives on the Systemic Management of Atopic Dermatitis.J Asthma Allergy. 2021;14:595-607. doi: 10.2147/JAA.S287638.
93. Roekevisch E, Spuls P I, Kuester D, Limpens J, Schmitt J. Efficacy and safety of systemic treatments for moderate-to-severe atopic dermatitis: A systematic review. J Allergy Clin Immunol. 2014;133:429-38. doi: 10.1016/j.jaci.2013.07.049.
94. Aliaga GLC, Anagusko CLY, Gomes LS, Mamede LQ, Moraes P, Cunha PS, et al. Adverse effects of using cyclosporine in patients with severe atopic dermatitis. Arq Asma Alergia Imunol. 2020;4(1):99-102.
95. Associação Brasileira de Imunizações (SBIM). Calendários de vacinação SBIm para pacientes especiais - 2021-2022 [Internet]. Disponível em: https://sbim.org.br/images/calendarios/calendsbim-pacientes-especiais.pdf. Acessado em: 20/08/2022.
96. Diniz AF, Bruscky DMV, Falcão ACA, Melo ACCDB, Peixoto DM, Sarinho ESC. Metotrexato em crianças e adolescentes com dermatite atópica: série de casos. Arq Asma Alergia Imunol. 2020;4(4):458-63. doi:10.5935/2526-5393.20200068.
97. Weatherhead SC, Wahie S, Reynolds NJ, Meggitt SJ. An open-label, dose-ranging study of methotrexate for moderate-to severe adult atopic eczema. Br J Dermatol. 2007;156(2):346-51. doi: 10.1111/j.1365-2133.2006.07686.x.
98. Goujon C, Viguier M, Staumont-Sallé D, Bernier C, Guillet G, Lahfa M, et al. Methotrexate Versus Cyclosporine in Adults with Moderate-to-Severe Atopic Dermatitis: A Phase III Randomized Noninferiority Trial. J Allergy Clin Immunol Pract. 2018;6(2):562569.e3. doi: 10.1016/j.jaip.2017.07.007.
99. El-Khalawany MA, Hassan H, ShaabanD, Ghonaim N, Eassa B. Methotrexateversuscyclosporinein thetreatment of severeatopic dermatitis in children: a multicenter experience from Egypt. Eur J Pediatr. 2013;172:351-6. doi: 10.1007/s00431-012-1893-3.
100. Schram ME, Roekevisch E, Leeflang MM, Bos JD, Schmitt J, Spuls PI. A randomized trial of methotrexate versus azathioprine for severe atopic eczema.J Allergy Clin Immunol.2011;128:353-9. doi: 10.1016/j.jaci.2011.03.024
101. Deo M, Yung A, Hill S, Rademaker M. Methotrexate for treatment of atopic dermatitis in children and adolescents. Int J Dermatol. 2014;53(8):1037-41. doi: 10.1111/ijd.12314.
102. Garritsen FM, Roekevisch E, van der Schaft J, Deinum J, Spuls PI, de Bruin-Weller MS. Ten years experience with oral immunosuppressive treatment in adult patients with atopic dermatitis in two academic centres.J Eur Acad Dermatol Venereol. 2015;29(10):1905-12. doi: 10.1111/jdv.13064.
103. MeggittSJ, Gray JC, ReynoldsNJ.Azathioprine dosed bythiopurine methyltransferase activity for moderate-to-severe atopic eczema:a double-blind, randomised controlled trial.Lancet.2006;367:839-46. doi: 10.1016/S0140-6736(06)68340-2.
104. Akdis CA, Akdis M, Bieber T, Bindslev-Jensen C, Boguniewicz M, Eigenmann P, et al. Diagnosis and treatment of atopic dermatitis in children and adults: European Academy of Allergology and Clinical Immunology/ American Academy of Allergy, Asthma and Immunology/PRACTALL Consensus Report. J Allergy Clin Immunol. 2006;118:152-69. doi: 10.1016/j.jaci.2006.03.045.
105. Murphy LA, Atherton DJ. Azathioprine as a treatment for severe atopic eczema in children with a partial thiopurine methyl transferase (TPMT) deficiency. Pediatr Dermatol. 2003;20:531-4.73. doi: 10.1111/j.1525-1470.2003.20617.x.
106. Murray ML, Cohen JB.Mycophenolatemofetil therapy for moderate to severe atopic dermatitis. Clin Exp Dermatol. 2007;32:23-27. doi: 10.1111/j.1365-2230.2006.02290.x.
107. Waxweiler WT, Agans R, Morrell DS.Systemic treatment of pediatric atopic dermatitis with azathioprine and mycophenolatemofetil. Pediatr Dermatol. 2011;28:689-94. doi: 10.1111/j.15251470.2011.01488.x.
108. Reis AP, Aarestrup FM. Imunoterapia e imunobiológicos na dermatite atópica. Arq Asma Alergia Imunol. 2019;3(2):123-32. doi: 10.5935/2526-5393.20190022
109. Seegräber M, Srour J, Walter A, Knop M, Wollenberg A.Dupilumab for treatment of atopic dermatitis. Exp Rev Clin Pharmacol. 2018;11:467-74. doi: 10.1080/17512433.2018.1449642.
110. Matsuyama C. Dupilumabe: novo horizonte no tratamento da rinossinusite crônica com pólipos nasais (RSCcPN); Sanofi 2022.
111. Dupilumabe -bula disponível na Internet. São Paulo: Sanofi Medley Farmacêutica Ltda;2022.Disponível em:https://consultas.anvisa.gov.br/#/bulario/q/?nomeProduto=Dupixent. Acessado em: 11/08/2022.
112. Harb H, Chatila TA. Mechanisms of Dupilumab. Clin Exp Allergy. 2020;50(1):5-14. doi: 10.1111/cea.13491.
113. Aoki V, Lorenzini D, Orfali RL, Zaniboni MC, Oliveira ZN, Rivitti-Machado MC, et al. Consensus on the therapeutic management of atopic dermatitis - Brazilian Society of Dermatology. An Bras Dermatol. 2019;94(2 Suppl 1):67-75.
114. Simpson EL, Paller AS, Siegfried EC, Boguniewicz M, Sher L, Gooderham MJ, et al. Efficacy and safety of dupilumab in adolescents with uncontrolled moderate to severe atopic dermatitis: a phase 3 randomized clinical trial. JAMA Dermatol. 2020;156(1):44-56. doi: 10.1001/jamadermatol.2019.3336.
115. Wollenberg A, Ariens L, ThurauS, vanLuijk C, Seegräber M, de Bruin-Weller M.Conjunctivitis occurring in atopic dermatitis patients treated with dupilumab - clinical characteristics and treatment. J Allergy Clin Immunol Pract.2018;6(5):1778-80.e1.doi:10.1016/j.jaip.2018.01.034.
116. Wollenberg A, Howell MD, Guttman-Yassky E, Silverberg JI, Kell C, Ranade K, et al. Treatment of atopic dermatitis with tralokinumab, an anti-IL-13 monoclonal antibody. J Allergy Clin Immunol. 2018;143(1):135-41. doi: 10.1016/j.jaci.2018.05.029.
117. Guttman-Yassky E, Brunner PM, Neumann AU, Khattri S, Pavel AB, Malik K. Efficacy and safety of fezakinumab (an IL-22 monoclonal antibody) in adults with moderate-to-severe atopic dermatitis inadequately controlled by conventional treatments: a randomized, double-blind, phase 2a trial. J Am Acad Dermatol. 2018;78:872-81. doi: 10.1016/j.jaad.2018.01.016.
118. Ahn J, Grinich EE, Choi Y, Guttman-Yassky E, Simpson EL. Emerging systemic therapeutic biologics and small molecules for atopic dermatitis: how to decide wich treatment is right for your patients. J Allergy Clin Immunol Pract. 2021;9:1449-60. doi: 10.1016/j.jaip.2021.02.003.
119. Howell MD, Fitzsimons C, Smith PA. JAK/STAT inhibitors and other small molecule cytokine antagonists for the treatment of allergic disease. Ann Allergy Asthma Immunol. 2018;120(4):367-75. doi:10.1016/j.anai.2018.02.012.
120. Klein B, Treudler R, Simon JC. JAK inhibitors in dermatology - small molecules, big impact? Overview of the mechanism of action, previous study results and potential adverse effects.J Dtsch Dermatol Ges. 2022;20(1):19-24. doi: 10.1111/ddg.14668.
121. Soeberdt M, Kilic A, Abels C.Small molecule drugs for the treatment of pruritus in patients with atopic dermatitis. Eur J Pharmacol. 2020;881:173242. doi: 10.1016/j.ejphar.2020.173242.
122. Li Q, Kang C. Mechanisms of Action for Small Molecules Revealed by Structural Biology in Drug Discovery. Int J Mol Sci. 2020;21(15):5262. doi: 10.3390/ijms21155262.
123. Ahn J, Choi Y, Simpson EL. Therapeutic New Era for Atopic Dermatitis: Part 2. Small Molecules. Ann Dermatol. 2021;33(2):101-7. doi: 10.5021/ad.2021.33.2.101.
124. Oetjen LK, Mack MR, Feng J, Whelan TM, Niu H, Guo CJ, et al. Sensory neurons co-opt classical immune signaling pathways to mediate chronic itch. Cell. 2017;171:217-28. doi: 10.1016/j.cell.2017.08.006.
125. FDA. Ruloxitinib. Drugs@FDA: FDA-Approved Drugs. Disponível em: https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=215309. Acessado em: 10/07/2022.
126. Nogueira LB, Chong-Silva DC, Rosário Filho NA, Chong-Neto HJ. Inibidores de JAK no tratamento da dermatite atópica. Arq Asma Alerg Imunol. 2022;6(3):331-43.
127. Guttman-Yassky E, Teixeira HD, Simpson EL, Papp KA, Pangan AL, Blauvelt A, et al. Once-daily upadacitinib versus placebo in adolescents and adults with moderate-to-severe atopic dermatitis (Measure Up 1 and Measure Up 2): results from two replicate double-blind, randomised controlled phase 3 trials. Lancet. 2021;397(10290):2151-68. doi: 10.1016/S01406736(21)00588-2.
128. Reich K, Teixeira HD, de Bruin-Weller M, Bieber T, Soong W, Kabashima K, Werfel T, et al. Safety and efficacy of upadacitinib in combination with topical corticosteroids in adolescents and adults with moderate-to-severe atopic dermatitis (AD Up):results from a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet. 2021;397(10290):2169-81. doi: 10.1016/S01406736(21)00589-4.
129. Mendes-Bastos P, Ladizinski B, Guttman-Yassky E, Jiang P, Liu J, Prajapati VH, et al. Characterization of acne associated with upadacitinib treatment in patients with moderate-to-severe atopic dermatitis:A post hoc integrated analysis of 3 phase 3 randomized, double-blind, placebo-controlled trials.J Am Acad Dermatol.2022 Oct;87(4):784-791. doi: 10.1016/j.jaad.2022.06.012.
130. Simpson EL, Papp KA, Blauvelt A, Chu CY, Hong HC, Katoh N, et al. Efficacy and Safety of Upadacitinib in Patients with Moderate to Severe Atopic Dermatitis: Analysis of Follow-up Data From the Measure Up 1 and Measure Up 2 Randomized Clinical Trials.JAMA Dermatol.2022;158(4):404-13.doi:10.1001/jamadermatol.2022.0029.
131. Silverberg JI, de Bruin-Weller M, Bieber T, Soong W, Kabashima K, Costanzo A, et al.Upadacitinib plus topical corticosteroids in atopic dermatitis:Week 52 AD Up study results.J Allergy Clin Immunol. 2022;149(3):977-87.e14. doi: 10.1016/j.jaci.2021.07.036.
132. Blauvelt A, Teixeira HD, Simpson EL, Costanzo A, De Bruin-Weller M, Barbarot S, et al. Efficacy and Safety of Upadacitinib vs Dupilumab in Adults with Moderate-to-Severe Atopic Dermatitis:A Randomized Clinical Trial.JAMA Dermatol.2021;157(9):1047-55. doi: 10.1001/jamadermatol.2021.3023.
133. Silverberg JI, Simpson EL, Thyssen JP, Gooderham M, Chan G, Feeney C, et al. Efficacy and Safety of Abrocitinib in Patients With Moderate-to-Severe Atopic Dermatitis: A Randomized Clinical Trial. JAMA Dermatol. 2020;156(8):863-73. doi: 10.1001/jamadermatol.2020.1406.
134. Simpson EL, Sinclair R, Forman S, Wollenberg A, Aschoff R, Cork M, et al. Efficacy and safety of abrocitinib in adults and adolescents with moderate-to-severe atopic dermatitis (JADE MONO-1): a multicentre, double-blind, randomised, placebo-controlled, phase 3 trial. Lancet. 2020;396(10246):255-66. doi: 10.1016/S0140-6736(20)30732-7.
135. Blauvelt A, Boguniewicz M, Brunner PM, Luna PC, Biswas P, DiBonaventura M, et al. Abrocitinib monotherapy in Investigator's Global Assessment nonresponders: improvement in signs and symptoms of atopic dermatitis and quality of life. J Dermatolog Treat. 2022 Aug;33(5):2605-13. doi: 10.1080/09546634.2022.2059053.
136. Blauvelt A, Silverberg JI, Lynde CW, Bieber T, Eisman S, Zdybski J, et al.Abrocitinib induction, randomized withdrawal, and retreatment in patients with moderate-to-severe atopic dermatitis: Results from the JAK1 Atopic Dermatitis Efficacy and Safety (JADE) REGIMEN phase 3 trial.J Am Acad Dermatol.2022;86(1):104-12. doi: 10.1016/j.jaad.2021.05.075.
137. Thyssen JP, Yosipovitch G, Paul C, Kwatra SG, Chu CY, DiBonaventura M, et al.Patient-reported outcomes from the JADE COMPARE randomized phase 3 study of abrocitinib in adults with moderate-to-severe atopic dermatitis. J Eur Acad Dermatol Venereol. 2022;36(3):434-43. doi: 10.1111/jdv.17813.
138. Alexis A, de Bruin-Weller M, Weidinger S, Soong W, Barbarot S, Ionita I, et al. Rapidity of Improvement in Signs/Symptoms of Moderate-to-Severe Atopic Dermatitis by Body Region with Abrocitinib in the Phase 3 JADE COMPARE Study. Dermatol Ther (Heidelb). 2022;12(3):771-85. doi: 10.1007/s13555-02200694-1.
139. Shi VY, Bhutani T, Fonacier L, Deleuran M, Shumack S, Valdez H, et al.Phase 3 efficacy and safety of abrocitinib in adults with moderate-to-severe atopic dermatitis after switching from dupilumab (JADE EXTEND).J Am Acad Dermatol.2022;87(2):351-8.doi:10.1016/j. jaad.2022.04.009.
140. Eichenfield LF, Flohr C, Sidbury R, Siegfried E, Szalai Z, Galus R, et al. Efficacy and Safety of Abrocitinib in Combination With Topical Therapy in Adolescents With Moderate-to-Severe Atopic Dermatitis: The JADE TEEN Randomized Clinical Trial. JAMA Dermatol. 2021;157(10):1165-73. doi: 10.1001/ jamadermatol.2021.2830.
141. Reich K, DeLozier AM, Nunes FP, Thyssen JP, Eichenfield LF, Wollenberg A, et al.Baricitinib improves symptoms in patients with moderate-to-severe atopic dermatitis and inadequate response to topical corticosteroids: patient-reported outcomes from two randomized monotherapy phase III trials. J Dermatol Treat. 2020;22:1-10. doi: 10.1080/09546634.2020.1839008.
142. Bieber T, Reich K, Paul C, Tsunemi Y, Augustin M, Lacour JP, et al.;BREEZE-AD4 study group.Efficacy and safety of baricitinib in combinationwith topicalcorticosteroids inpatientswith moderate-to-severe atopic dermatitis with inadequate response, intolerance or contraindication to ciclosporin: results from a randomized, placebo-controlled, phase III clinical trial (BREEZE-AD4). Br J Dermatol. 2022;187(3):338-52. doi: 10.1111/bjd.21630.
143. Silverberg JI, Boguniewicz M, Waibel J, Weisman J, Strowd L, Sun L, et al. Clinical Tailoring of Baricitinib 2 mg in Atopic Dermatitis: Baseline Body Surface Area and Rapid Onset of Action Identifies Response at Week 16.Dermatol Ther (Heidelb).2022;12(1):137-48. doi: 10.1007/s13555-021-00640-7.
144. Simpson EL, Forman S, Silverberg JI, Zirwas M, Maverakis E, Han G, et al.Baricitinib in patients with moderate-to-severe atopic dermatitis: Results from a randomized monotherapy phase 3 trial in the United States and Canada (BREEZE-AD5). J Am Acad Dermatol. 2021;85(1):62-70. doi: 10.1016/j.jaad.2021.02.028.
145. Reich K, Kabashima K, Peris K, Silverberg JI, Eichenfield LF, Bieber T, et al. Efficacy and Safety of Baricitinib Combined With Topical Corticosteroids for Treatment of Moderate to Severe Atopic Dermatitis: A Randomized Clinical Trial. JAMA Dermatol. 2020;156(12):1333-43. doi: 10.1001/jamadermatol.2020.3260.
146. de Bruin-Weller MS, Serra-Baldrich E, Barbarot S, Grond S, Schuster C, Petto H, et al. Indirect Treatment Comparison of Baricitinib versus Dupilumab in Adults with Moderate-to-Severe Atopic Dermatitis. Dermatol Ther (Heidelb). 2022;12(6):1481-91. doi: 10.1007/s13555-022-00734-w.
147. Papp K, Szepietowski JC, Kircik L, Toth D, Eichenfield LF, Leung DYM, et al.Efficacy and safety of ruxolitinib cream for the treatment of atopic dermatitis:Results from 2 phase 3, randomized, double-blind studies. J Am Acad Dermatol. 2021;85(4):863-72. doi: 10.1016/j.jaad.2021.04.085.
148. Nakagawa H, Nemoto O, Igarashi A, Saeki H, Kabashima K, Oda M, et al. Delgocitinib ointment in pediatric patients with atopic dermatitis:A phase 3, randomized, double-blind, vehicle-controlled study and a subsequent open-label, long-term study. J Am Acad Dermatol. 2021;85(4):854-62. doi: 10.1016/j.jaad.2021.06.014.
149. Nakagawa H, Nemoto O, Igarashi A, Saeki H, Murata R, Kaino H, Nagata T. Long-term safety and efficacy of delgocitinib ointment, a topical Janus kinase inhibitor, in adult patients with atopic dermatitis. J Dermatol. 2020;47(2):114-20. doi: 10.1111/13468138.15173.
150. European Medicines Agency. Rinvoq - european medicines agency [Internet]. Disponível em: https://www.ema.europa.eu/en/medicines/human/EPAR/rinvoq. Acessado em: 22/07/2022.
151. FDA. Upadacitinib - Drugs@FDA: FDA-Approved Drugs [Internet]. Disponível em: https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=BasicSearch.process. Acessado em: 15/07/2022.
152. Diário Oficial da União. Ministério da Saúde/Agência Nacional de Vigilância Sanitária/2ª Diretoria/Gerência-Geral de Medicamentos e Produtos. Resolução Re Nº 1.355, de 28 de Abril de 2022. Disponível em: https://www.in.gov.br/web/dou/-/resolucao-ren-1.355-de-28-de-abril-de-2022-396547245. Acessado em: 15/07/2022.
153. FDA. Abrocitinib - Drugs@FDA: FDA-ApprovedDrugs [Internet]. Disponível em: https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=BasicSearch.process. Acessado em: 12/07/ 2022.
154. European Medicines Agency. Olumiant - european medicines agency [|Internet]. Disponível em: https://www.ema.europa.eu/en/medicines/human/EPAR/olumiant. Acessado em: 22/07/2022.
155. Dhillon S. Delgocitinib: First Approval. Drugs. 2020;80(6):609-15. doi: 10.1007/s40265-020-01291-2.
156. Torres T, Gonçalo M, Lopes MJP, Claro C, Ramos L, Selores M, et al. Portuguese recommendations for the treatment of atopic dermatitis with biologic therapy and JAK inhibitors in adult patients. Drugs Contex. 2021;10:2021-9-5. doi: 10.7573/dic.2021-9-5.
157. Wollenberg A, Kinberger M, Arents B, Aszodi N, Avila Valle G, Barbarot S, et al. European guideline (EuroGuiDerm) on atopic eczema: part I - systemic therapy. J Eur Acad Dermatol Venereol. 2022;36:1409-31. doi: 10.1111/jdv.18345.
158. Ahn K, Kim BE, Leung DYM. Recent advances in atopic dermatitis. Curr Opin Immunol. 2020;16:14-21. doi: 10.1016/j. coi.2020.02.007.
159. Wu J, Guttman-Yassky E. Efficacy of biologics in atopic dermatitis. Exp Opin Biol Ther. 2020;20(5):525-38. doi: 10.1080/14712598.2020.1722998.
160. Stefanovic N, Flohr C, Irvine AD. The exposome in atopic dermatitis. Allergy. 2020;75(1):63-74. doi: 10.1111/all.13946.
161. Moyle M, Cevikbas F, Harden J, Guttman-Yassky E. Understanding the immune landscape in atopic dermatitis.The era of biologics and emerging therapeutic approaches. Exp Dermatol. 2019;28:756-68. doi: 10.1111/exd.13911.
162. Puar N, ChovatiyaR ,Paller AS. New treatments in atopic dermatitis. Ann Asthma Immunol. 2021;126(1):21-31. doi: 10.1016/j. anai.2020.08.016.