Número Atual: Abril-Junho 2022 - Volume 6 - Número 2
- Imprimir
- Indicar
- Estatísticas
- (0)
Comentários - Como Citar
- Download da Citação
- Artigos Relacionados
-
Outros dos
Autores
Comunicações Clínicas e Experimentais
Pitiríase liquenoide pós-vacinação contra COVID-19: um relato de caso
Pityriasis lichenoides after COVID-19 vaccination: a case report
Isabela Ceschin Maestri1; Monica Preto Guimarães1; Tsukiyo Kamoi2; Rafaela Ceschin Fernandes3, Renato Nisihara1,2
DOI: 10.5935/2526-5393.20220030
1. Universidade Positivo, Medicina - Curitiba, PR, Brasil
2. Universidade Federal do Paraná, Hospital de Clínicas - Curitiba, PR, Brasil
3. Faculdade Pequeno Príncipe, Medicina - Curitiba, PR, Brasil
Endereço para correspondência:
Renato Nisihara
E-mail: renatonisihara@gmail.com
Submetido em: 29/06/2021
Aceito em: 19/02/2022
Não foram declarados conflitos de interesse associados à publicação deste artigo
RESUMO
O artigo aborda o primeiro relato de caso que associa o desenvolvimento de pitiríase liquenoide com a vacinação contra a COVID-19. Em uma revisão literária foram encontrados escassos estudos que associam a pitiríase liquenoide como reação a outras vacinas. O mecanismo de desenvolvimento da doença ainda não é bem conhecido. Sabe-se apenas que se trata de uma reação inflamatória imunomediada. O diagnóstico da pitiríase liquenoide é clínico e é considerado um desafio, devido ao grande número de diagnósticos diferenciais e das diferentes formas de apresentação da doença. Desse modo, a maioria dos casos exige amparo na biópsia e em exames laboratoriais. As opções terapêuticas podem incluir o uso de antibióticos e imunossupressores. Destaca-se ainda a efetividade da fototerapia como tratamento de escolha da pitiríase liquenoide, podendo proporcionar uma resolução quase que completa das lesões e não causar efeitos sistêmicos que outras terapias poderiam trazer.
Descritores: Pitiríase liquenoide, vacinas contra COVID-19, vacinas.
INTRODUÇÃO
A pitiríase liquenoide (PL) é um distúrbio dermatológico imunomediado incomum e de etiologia desconhecida. Contudo, sabe-se que pode ocorrer em associação com a exposição a medicamentos, infecções, contraste radiológico e vacinas1.
A doença pode se manifestar de duas formas: a pitiríase liquenoide e varioliforme aguda (PLEVA) e a pitiríase liquenoide crônica (PLC)2. A primeira remete a um quadro agudo caracterizado por múltiplas lesões ulceradas ou pápulas avermelhadas crostosas, as quais geralmente cicatrizam deixando sequelas, como hiper/hipopigmentação ou cicatrizes varioliformes. Ela possui períodos de remissão variáveis, com curso limitado. Já a segunda, se manifesta através de pápulas escamosas marrom-avermelhadas que podem durar anos e também gerar sequelas. Entretanto, há casos com lesões que remetem aos dois diagnósticos2,3. Além disso, existe uma variante clínica da PLEVA, a doença de Mucha-Habermann ulceronecrótica febril (FUMHD), que é caracterizada por lesões cutâneas ulceronecróticas associadas a febre alta e sintomas sistêmicos. É um quadro mais grave e com potencial maligno associado a proliferações linfoides T4.
O diagnóstico da PL é clínico e necessita de investigações diferenciais para varicela, papulose linfomatoide, sífilis secundária, vasculite e pitiríase rósea5. Logo, para a diferenciação etiológica, são necessários exames laboratoriais e/ou análise histológica.
Este estudo tem por objetivo o relato de um caso de PL pós-vacinação com a vacina contra SARS-CoV-2 CoronaVac®, descrevendo os achados e conduta clínica.
RELATO DO CASO
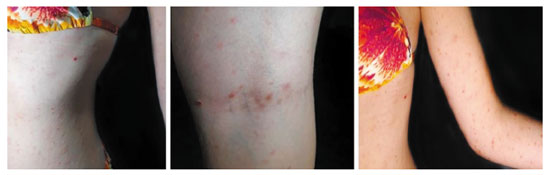
Paciente do sexo feminino, 20 anos, previamente hígida, comparece à consulta dermatológica ao notar o aparecimento de pápulas avermelhadas, não pruriginosas, em toda superfície corporal há cerca de uma semana e meia. O surgimento das lesões se deu após três dias da primeira dose da vacina contra o SARS-CoV-2 desenvolvida pela Sinovac (China) e produzida no Brasil pelo Instituto Butantan6. A CoronaVac® é composta pelo vírus inativado e uma solução de hidróxido de alumínio7. A vacina foi realizada pela injeção intramuscular em deltoide direito (0,5 mL). Paciente relatou que as lesões iniciaram de forma lenta no tronco, mas evoluíram rapidamente para as demais áreas do corpo. Destaca-se que as pápulas surgiram em regiões de menor exposição solar, como região interna e posterior dos membros. À análise clínica, confirma-se a presença de pápulas eritematosas (Figura 1). Somente na fossa poplítea se observou a presença de três lesões violáceas. Tal fato sugere que as lesões estavam em diferentes estágios de desenvolvimento. No tórax, notou-se lesões maiores com descamação em colarete. Para o controle das lesões, recomendou-se o uso de um creme manipulado com baixa concentração de desonida (0,05 mk) em 100 mL de loção hidratante, com aplicação de uma vez ao dia, mas sem resposta.
Solicitou-se os testes treponêmico e não treponêmico para sífilis, os quais vieram negativos. Após a segunda dose da vacina, percebeu-se um aumento das lesões, indicando biópsia e o início de limeciclina (300 mg) uma vez ao dia.
A biópsia foi feita em três áreas diferentes, com análise histopatológica evidenciando alterações semelhantes. Dentre os achados, a epiderme apresentou acantose irregular discreta, paraceratose multifocal com lagos serosos, espongiose multifocal moderada, exocitose de linfócitos raríssimos e queratinócitos necróticos. Já a derme superficial mostrou edema e moderado infiltrado inflamatório perivascular linfocitário com hemácias extravasadas. Os achados sugerem uma dermatite espongiótica e de interface. Confirmou-se assim a hipótese de PL, descartando diagnósticos diferenciais. Neste momento, foi iniciado o tratamento com tetraciclina (500 mg) duas vezes ao dia, por dez dias; contudo, sem melhora.
De acordo com os achados, o diagnóstico firmado foi de PLC, embora o período entre o início e a resolução das lesões seja compatível com PLEVA. Desse modo, o médico assistente optou por um tratamento mais brando, com dez sessões de fototerapia, notando significativa resolução das lesões após a segunda sessão.
DISCUSSÃO
Neste caso, a hipótese é de que a vacina tenha desencadeado uma reação inflamatória imunomediada. Logo, torna-se notável a relevância desse estudo por ser o primeiro relatado sobre a associação da PL com a vacinação da COVID-19. Durante a revisão de literatura, foram encontrados escassos estudos relacionando a PL com outros tipos de vacina, como a tríplice viral, influenza e dupla do adulto1,8,9. Sugere-se, portanto, que a PL seja desencadeada por uma resposta inflamatória a antígenos extrínsecos. A vacina SARS-CoV-2 Coronavac® é administrada em duas doses, com intervalo de duas a quatro semanas. Por ser uma vacina desenvolvida recentemente, ainda não há dados concretos sobre a caracterização e frequência de todos seus efeitos adversos.
A PL é uma doença dermatológica relacionada à formação de lesões com amplas variações de morfologia. As lesões primárias na PLEVA se desenvolvem formando necrose central com crosta hemorrágica e possuem resolução gradual3. Já na PLC, essas lesões se apresentam como um quadro monomórfico de pápulas eritemato-acastanhadas recobertas por uma escama aderente. Tanto o quadro crônico como o agudo são mais prevalentes no sexo masculino, e acometem adolescentes e adultos jovens10.
O diagnóstico é clínico e confirmado por biópsia, contudo é um desafio pelos múltiplos diagnósticos diferenciais. Além disso, pode haver a superposição entre suas classificações. Os achados histopatológicos incluem infiltrado linfocítico superficial paravascular ou liquenoide com alteração vacuolar da camada basal, paraqueratose, queratinócitos necróticos individuais na epiderme e extravasamento de hemácias3. Tais alterações são mais evidentes na PLEVA, sendo que na PLC são menos exuberantes. A descrição histopatológica é compatível com a da paciente, e sugere-se o quadro de PLC.
A doença apresenta curso variável e com recorrências comuns. Geralmente a PLEVA se resolve em semanas, enquanto a PLC pode levar meses2. O tratamento pode envolver agentes tópicos, antibióticos, fototerapia e imunossupressores2. A antibioticoterapia com eritromicina ou tetraciclina pode ser benéfica para a redução do curso da doença3. No caso da paciente, iniciou-se o uso da limeciclina e posteriormente da tetraciclina. Apesar da primeira derivar da tetraciclina, há casos de resposta insatisfatória, enquanto a da segunda pode ser efetiva. A fototerapia é o tratamento de escolha quando não há resposta ao uso de antibióticos orais2. Tal método foi resolutivo no caso da paciente. Em casos graves e refratários, há indicação de uso de corticoides sistêmicos, metotrexato ou ciclosporina2.
CONCLUSÃO
A pitiríase liquenoide é uma doença pouco frequente, necessitando, por vezes, de amparo na biópsia para diagnóstico diferencial.
Este relato de caso abordou o primeiro quadro relatado de pitiríase liquenoide crônica relacionado à vacina CoronaVac®.
REFERÊNCIAS
1. Merlotto MR, Bicudo NP, Marques MEA, Marques SA. Pityriasis lichenoides et varioliformis acuta following anti-tetanus and diphtheria adult vaccine. Ann Bras Dermatol. 2020;95:259-60.
2. Wolff K, Johnson RA, Saavedra AP. Dermatologia de Fitzpatrick: atlas e texto [recurso eletrônico]. 8ª ed. Porto Alegre: AMGH; 2019.
3. Eichenfield LF, Frieden IJ. Dermatologia neonatal e infantil. 3ª ed. Rio de Janeiro: Elsevier; 2016. p. 554.
4. Reichel A, Grothaus J, Ott H. Pityriasis lichenoides acuta (PLEVA) pemphigoides: A rare bullous variant of PLEVA. Pediatr Dermatol. 2020;37:710-12. doi.org/10.1111/pde.14181.
5. Ankad BS, Beergouder SL. Pityriasis lichenoides et varioliformis acuta in skin of color: new observations by dermoscopy. Dermatol Pract Concept. 2017; 31:7(1):27-34. doi: 10.5826/dpc.0701a05.
6. Instituto Butantan. Vacina adsorvida COVID-19 (inativada). Bula profissional da saúde [Internet]. 2021. Disponível em: https://vacinacovid.butantan.gov.br/assets/arquivos/Bulas_Anvisa/Bula_PS_vacina%20adsorvida%20covid-19%20(inativada).pdf . Acessado em: 28/05/2021.
7. Zhang Y, Zeng G, Pan H, Li C, Hu Y, Chu K, et al. Safety, tolerability, and immunogenicity of an inactivated SARS-CoV-2 vaccine in healthy adults aged 18-59 years: a randomised, double-blind, placebo-controlled, phase 1/2 clinical trial. Lancet Infect Dis. 2021;21(2):181-92.
8. Zang JB, Coates SJ, Huang J, Vonderheid EC, Cohen BA. Pityriasis lichenoides: Long-term follow-up study. Pediatr Dermatol. 2018;35(2):213-9. doi: 10.1111/pde.13396.
9. Castro BA, Pereira JM, Meyer RL, Trindade FM, Pedrosa MS, Piancastelli AC. Pityriasis lichenoides et varioliformis acuta after influenza vaccine. Ann Bras Dermatol. 2015;90(3 Suppl 1):181-4. doi:10.1590/abd1806-4841.20153492.
10. Azulay L, Hanauer L, Leal F, Azulay DR. Atlas de Dermatologia - Da Semiologia ao Diagnóstico. 3ª ed. Rio de Janeiro: GEN Guanabara Koogan. 2020. p. 1136.