Número Atual: Janeiro-Março 2021 - Volume 5 - Número 1
- Imprimir
- Indicar
- Estatísticas
- (0)
Comentários - Como Citar
- Download da Citação
- Artigos Relacionados
-
Outros dos
Autores- Fernando Monteiro Aarestrup
- Anna Caroline Nóbrega Machado Arruda
- Clóvis Eduardo Santos Galvão
- Gil Bardini Alves
- Geórgia Véras de Araújo Gueiros Lira
- Ernesto Akio Taketomi
- Marcos Reis Gonçalves
- Mariana Graça Couto Miziara
- Sidney Souteban Maranhão Casado
- Simone Valladão Curi
- Veridiana Aun Rufino Pereira
- Elaine Gagete
ARTIGO ESPECIAL
Posicionamento da Associação Brasileira de Alergia e Imunologia sobre o manejo da imunoterapia específica com alérgenos (ITA) em pacientes vacinados contra COVID‑19
Position statement of the Brazilian Association of Allergy and Immunology on the management of allergen-specific immunotherapy (AIT) in patients vaccinated against COVID‑19
Fernando Monteiro Aarestrup; Anna Caroline Nóbrega Machado Arruda; Clóvis Eduardo Santos Galvão; Gil Bardini Alves; Geórgia Véras de Araújo Gueiros Lira; Ernesto Akio Taketomi; Marcos Reis Gonçalves; Mariana Graça Couto Miziara; Sidney Souteban Maranhão Casado; Simone Valladão Curi; Veridiana Aun Rufino Pereira; Elaine Gagete
Departamento Científico de Imunoterapia da Associação Brasileira de Alergia e Imunologia - ASBAI
Endereço para correspondência:
Fernando Monteiro Aarestrup
E-mail: fmaarestrup@hotmail.com
Submetido em: 23/02/2021
Aceito em: 05/03/2021
RESUMO
A pandemia de COVID-19 representa um grande desafio para todas as especialidades médicas. A imunoterapia com alérgenos (ITA) é considerada o único procedimento terapêutico capaz de modificar a história natural das doenças alérgicas, e caracteriza o estado da arte na área de Alergia e Imunologia. Esta estratégia terapêutica de imunomodulação é capaz de promover a remissão e controle das doenças alérgicas por períodos prolongados, mesmo após o seu término. Existem poucos dados em relação ao emprego da ITA em pacientes vacinados contra COVID-19, e até o momento não há um posicionamento oficial das sociedades internacionais da área de Alergia e Imunologia Clínica. Este documento tem como objetivo estabelecer recomendações práticas para o manejo da ITA em pacientes que receberam a vacina contra COVID-19. Os fenômenos imunológicos envolvidos na imunoprofilaxia vacinal e no mecanismo de ação da ITA foram comparados, proporcionando o estabelecimento de recomendações precisas.
Descritores: Imunoterapia com alérgenos, dessensibilização imunológica, COVID-19.
INTRODUÇÃO
Em 11 de março de 2020 a Organização Mundial da Saúde (OMS) declarou a existência de uma pandemia causada por um novo tipo de coronavírus humano, o SARS-CoV-2. Desde então, profissionais de saúde e cientistas buscam maneiras de controlar a disseminação desta nova doença, denominada COVID-19, via desenvolvimento de novos fármacos e estratégias de imunoprofilaxia vacinal1-3.
Segundo a OMS, os dados epidemiológicos atuais da doença são alarmantes, com mais de 100 milhões de casos confirmados e aproximadamente 2 milhões de mortes em todo mundo. Até o momento, não existem terapêuticas específicas eficazes no combate a infecção pelo SARS-CoV2. Felizmente, de maneira inédita na história da medicina, estratégias terapêuticas vacinais contra uma doença foram desenvolvidas em menos de um ano, possibilitando o início da imunização da população4-5.
Este documento tem como objetivo estabelecer recomendações práticas sobre como proceder o manejo da imunoterapia específica com alérgenos (ITA) em pacientes que receberam a vacina contra COVID-19.
VACINAS CONTRA COVID-19
Várias metodologias foram utilizadas para o desenvolvimento de imunizantes contra a COVID-194-5. A seguir descreveremos resumidamente os tipos de plataformas tecnológicas empregadas.
Inativação viral
Esta tecnologia clássica consiste na replicação viral em cultura de células e posterior inativação dos vírus por agentes químicos ou físicos. Adjuvantes podem ser acrescentados a estas vacinas conferindo aumento da imunogenicidade. São exemplos de imunoprofilaxia vacinal específica com vírus inativados as vacinas da gripe - causada por vírus influenza, da hepatite A e contra a poliomielite.
Vetores virais não replicantes
Esta nova tecnologia utiliza vírus geneticamente modificados, com total ausência de potencial patogênico. Nesta técnica, os vírus transportam o gene que codifica a proteína spyke (proteína S) do SARS-CoV-2. Portanto, esse vírus carreador do código genético apenas leva a mensagem para a produção da proteína S, funcionando como um vetor vacinal na célula humana. A partir desse momento o sistema imunológico inicia o desenvolvimento de uma resposta específica contra o SARS-CoV-2.
Vacinas baseadas em RNA mensageiro (mRNA)
Esta inovadora plataforma de produção é estudada há muito tempo, entretanto, é a primeira que é utilizada na prática médica. Consiste na administração de mRNA sintético que codifica a proteína S do SARS-CoV-2, induzindo a produção desta proteína pelas próprias células humanas. Esta molécula de mRNA contém exclusivamente informação genética específica, não tendo potencial para modificar o genoma humano ou causar COVID-19. O processo acontece exclusivamente no citoplasma e, em momento algum, há interação entre o mRNA viral e o DNA da célula humana. Esta plataforma de desenvolvimento de vacinas baseadas em mRNA possibilita a produção de imunizantes em alta escala, em curto espaço de tempo, além de permitir futuras alterações caso ocorram mutações virais que venham a gerar novas variantes do SARS-CoV-2.
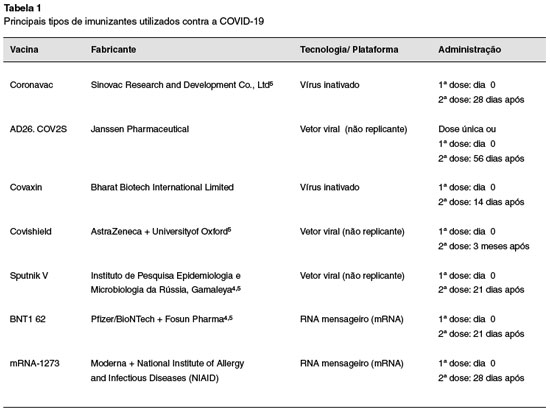
Na Tabela 1 encontram-se as características gerais das principais vacinas que estão sendo utilizadas em todo o mundo.
FUNDAMENTOS DO MECANISMO IMUNOLÓGICO DA IMUNOPROFILAXIA VACINAL E ITA
O desenvolvimento de vacinas com finalidade de estimular resposta protetora contra agentes infecciosos revolucionou a história da humanidade. O mecanismo básico da imunoprofilaxia vacinal atua, principalmente, por meio do desenvolvimento de memória imunológica antígeno específica. Tanto a resposta imune celular mediada por células T, quanto a resposta imune humoral coordenada pelas células B, participam deste processo. A utilização de diversas estratégias utilizando de micro-organismos inteiros inativados ou atenuados, moléculas específicas de agentes infecciosos e, recentemente, as vacinas que empregam a tecnologia de RNA-m, representam a medida mais importante de prevenção de doenças infecciosas em termos de saúde pública4,5.
As diferentes plataformas de produção de vacina contra COVID-19 induzem resposta imunológica celular com o desenvolvimento de clones específicos de células T capazes de reconhecer o SARS-CoV-2 desenvolvendo resposta efetora via produção de citocinas, cujo objetivo principal é impedir a replicação viral. O estímulo vacinal também atua promovendo a proliferação clonal de células B específicas, levando à produção de imunoglobulinas da classe IgG, que têm como finalidade o combate ao SARS-CoV-2.As vacinas de vírus inativados estimulam o sistema imune através de várias moléculas concomitantemente. Entretanto, as novas tecnologias e produção de vacinas utilizando vetores virais promovem a indução da resposta imune via a proteína da espícula do vírus (proteína S). Embora estejamos falando de plataformas tecnológicas diferentes, o mecanismo básico da resposta imune protetora é o mesmo, independente do tipo de vacina administrado4,5,7.
Fundamentalmente, a imunoprofilaxia se caracteriza por memória imunológica que proporciona rápida e efetiva resposta à antígenos específicos. Mecanismos diversos de reconhecimento antígênico e de resposta imune efetora são utilizados com o intuito de conter a proliferação dos agentes infecciosos.
A ITA vem sendo utilizada há mais de um século como estratégia terapêutica para modificar a resposta imunológica específica para determinados alérgenos. Atualmente, muito é conhecido a respeito das células e das citocinas envolvidas no mecanismo de ação da ITA, que tem como base a imunomodulação, induzindo tolerância imunológica periférica específica. Diversos tipos celulares participam deste processo, envolvendo tanto a resposta imune inata, quanto a adaptativa. As células linfoides inatas (CLI), células T e células B coordenam este processo por meio de uma rede de citocinas que orquestra a resposta por células efetoras, tais como mastócitos, eosinófilos e basófilos. O mecanismo de imunomodulação na ITA tem como personagens principais as células T reguladoras (Treg), células B reguladoras (Breg) e as citocinas imunossupressoras fator de crescimento de células transformadas beta (TGF-b) e interleucina 10 (IL-10). A imunomodulação na ITA atua sobre a resposta inflamatória do tipo 2, reduzindo células T CD4+ TH2 alérgeno-específicas na circulação, além de diminuir a atividade de células linfoides inatas tipo 2 (CLI-2). As células Treg e Breg, principalmente através da síntese de TGF- e IL-10, induzem tolerância periférica aos alérgenos. Adicionalmente, a ITA modifica o perfil de produção de citocinas Th2 para Th1. Deste modo, ocorre diminuição da produção de IL-4, IL-5 e IL-13 em resposta à presença de alérgenos específicos, reduzindo a resposta inflamatória do tipo 2, que, classicamente ocorre em indivíduos atópicos. Como resultado deste processo de imunomodulação, a ITA diminui a produção de IgE e aumenta a produção de IgG4 específicas para o alérgeno. Todos estes fenômenos imunológicos acima descritos caracterizam a dessensibilização, promovendo tolerância ao alérgeno6-8,12-15.
Concluindo em linhas gerais, a ITA é uma estratégia de imunomodulação da resposta alérgeno-específica, não apresentando similaridades diretas com a imunoprofilaxia vacinal utilizada na prevenção de doenças infecciosas.
IMUNIZAÇÃO CONTRA COVID-19 E ADMINISTRAÇÃO DE ITA
A Academia Americana de Alergia, Asma e Imunologia (AAAAI), a Academia Europeia de Alergia, Asma e Imunologia Clínica (EAACI) e a Associação Brasileira de Alergia e Imunologia (ASBAI) recomendam a não interrupção da ITA durante a pandemia de COVID-19, possibilitando o controle adequado de doenças alérgicas respiratórias, como rinite e asma. Adaptações de esquemas terapêuticos e medidas de biossegurança durante a aplicação foram sugeridas para reduzir a possibilidade de transmissão do SARS-CoV-2 nos pacientes em uso de ITA específica para aeroalérgenos ou veneno de himenópteros6-12.
A Agência Nacional de Vigilância Sanitária (ANVISA) aprovou, recentemente, dois imunizantes contra a COVID-19 para utilização em nosso país, via Plano Nacional de Imunização (PNI). Este novo cenário faz com que seja necessário posicionamento sobre o manejo da ITA em pacientes submetidos à imunização contra COVID-19. O processo contínuo de avaliação de novos imunizantes pela ANVISA irá, certamente, em um curto espaço de tempo, oferecer à população brasileira diversos tipos de vacinas.
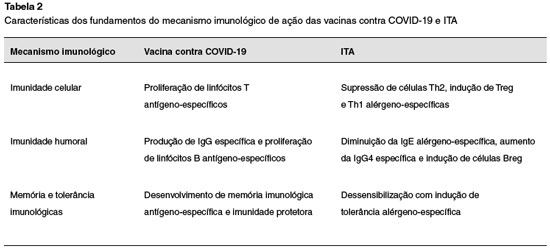
Classicamente, órgãos governamentais de saúde e Sociedades Médicas que abordam o tema imunoprofilaxia vacinal recomendam intervalo de duas semanas entre a aplicação de algumas vacinas6,13. Tal recomendação está relacionada com a possibilidade de dois imunizantes diferentes, aplicados com pequeno intervalo de tempo, levar à diminuição da resposta imunológica vacinal. Existem poucos dados em relação ao emprego da ITA em pacientes vacinados contra COVID-19 e, até o momento, não há um posicionamento oficial das sociedades internacionais da área de Alergia e Imunologia Clínica. Deve-se levar em consideração que a dessensibilização alérgica que caracteriza a ITA não tem como finalidade induzir resposta contra um novo antígeno; sendo o mecanismo de ação da ITA baseado na regulação da resposta imunológica alérgeno-específica já existente, induzindo a tolerância imunológica. A administração da ITA, seja por via subcutânea (ITSC) ou por via sublingual (ITSL), conceitualmente, não interfere na indução da resposta vacinal, visto que atuam por mecanismos de ação diferentes dos que ocorrem na imunoprofilaxia para doenças infecciosas6-8,12-15 (Tabela 2). Entretanto, estudos são necessários para melhor avaliar esta questão.
A aplicação de ITSC, embora apresente alto padrão de segurança, pode causar reações no local da aplicação e efeitos adversos sistêmicos, tais como coriza, prurido nasal, dentre outros, que podem ser confundidos com sintomas reacionais dos imunizantes contra COVID-19 e com sinais e sintomas da própria COVID-19. A exemplo do que ocorre com a aplicação de outros imunizantes, recomenda-se intervalo de no mínimo duas semanas entre as aplicações da ITSC e vacina contra COVID-19. Este posicionamento é válido tanto para o emprego da ITA específica para aeroalérgenos quanto para veneno de himenópteros. Com relação à ITSL, devido à pequena ocorrência de efeitos adversos, orienta-se não suspender ou postergar o tratamento em virtude da administração da vacina contra COVID-19.
SITUAÇÕES ESPECIAIS
- Em casos específicos, as aplicações de ITA por via subcutânea (ITSC) poderão ser realizadas com o intervalo de no mínimo 48 horas antes e após a aplicação da vacina contra COVID-19. Esta sugestão leva em consideração os riscos sobre a perda de controle da doença alérgica devido aos prejuízos decorrentes sobre o processo de dessensibilização; entretanto, os riscos e benefícios devem ser avaliados.
- Em pacientes com história prévia de reações com ITSL, pode ser recomendado um período de intervalo de 48 horas antes e após a aplicação da vacina contra COVID-19. Esta sugestão leva em consideração a possibilidade, mesmo que pouco frequente, da ocorrência de efeitos adversos da ITSL, que possam ser confundidos com os da aplicação das vacinas contra COVID-19.
REFERÊNCIAS
1. World Health Organization. WHO's COVID-19 response [site na internet]. Disponível em: https://www.who.int/emergencies/diseases/novel-coronavirus-2019/interactive-timeline#.
2. World Health Organization. WHO Coronavirus Disease (COVID-19) Dashboard [site na internet]. Disponível em: https://covid19.who.int/
3. Aarestrup FM. Imunopatologia da COVID-19 e suas implicações clínicas. Arq Asma Alerg Imunol. 2020;4(2):172-80.
4. Sharma O, Sultan AA, Ding H, Triggle CR. A Review of the Progress and Challenges of Developing a Vaccine for COVID-19. Front Immunol. 2020;14,11:585354.
5. Izda V, Jeffries MA, SawalhaAH. COVID-19: A review of therapeutic strategies and vaccine candidates. Clin Immunol. 2021;222:108634.
6. American Academy of Allergy, Asthma and Immunology [site na internet]. Disponível em: https://www.aaaai.org/ask-the-expert/scit. Acessado em: 08/02/2021.
7. Klimek L, Jutel M, Akdis C, Bousquet J, Akdis M, Bachert C, et al. ARIA-MASK Study Group: Handling of allergen immunotherapy in the COVID-19 pandemic: An ARIA-EAACI statement. Allergy. 2020;75(7):1546-54.
8. Dell'Edera A, Borghesan F, Favero E, Rattazzi M, Scarpa R, Tartaglia L, et al. Venom immunotherapy during COVID-19 pandemic: Experience fro a University Allergy Center in Northern Italy. World Allergy Organ J. 2020;13(12):100489.
9. Compalati E, Erlewyn-Lajeunesse M, Runa Ali F, Ojeda Fernández P, Garcia Nuñez I, Frati F, et al. Allergen Immunotherapy in the Era of SARS-CoV-2. J Investig Allergol Clin Immunol. 2020;30(6):459-61.
10. Machado AS, Falcão ACAM, Serpa FS, Sano F, Rizzo JA, Elabras Filho J, et al. Recomendações da Associação Brasileira de Alergia e Imunologia para pacientes com Asma durante a COVID-19. Arq Asma Alerg Imunol. 2020;4(1):133-4.
11. Rosario Filho NA, Magalhães Rios JL, Morandi JLB, Tebyriçá JN, Lira GVGA, Antila MA, et al. Imunoterapia específica em época de pandemia de COVID-19. Arq Asma AlergImunol. 2020;4(2):238.
12. Klimek L, Pfaar O, Worm M, Bergmann KC, Bieber T, Buhl R, et al. Allergenimmunotherapy in the current COVID-19 pandemic: A position paper of AeDA, ARIA, EAACI, DGAKI and GPA: Position paper of the German ARIA Group in cooperation with the Austrian ARIA Group, the Swiss ARIA Group, German Society for Applied Allergology (AEDA), German Society for Allergology and Clinical Immunology (DGAKI), Society for Pediatric Allergology (GPA) in cooperation with AG Clinical Immunology, Allergology and Environmental Medicine of the DGHNO-KHC and the European Academy of Allergy and Clinical Immunology (EAACI). Allergol Select. 2020 May 28;4:44-52.
13. Sociedade Brasileira de Imunizações [site na internet]. Disponível em: https://sbim.org.br. Acessado em: 08/02/2021.
14. Kleine-Tebbe J, Klimek L, Hamelmann E, Pfaar O, Taube C, Wagenmann, et al. Severe allergic reactions to the COVID-19 vaccine - statement and practical consequences. Allergol Select. 2021;5:26-8.
15. Taketomi EA, Miranda JS, Cunha-Júnior JC, Silva DAO. Allergen-specific immunotherapy follow-up by measuring allergen-specificIgG as an objective parameter. In: Metodiev K (ed.). Immunotherapy. Rijeka: InTech, 2017. p.381-401. Disponível em: http://dx.doi.org/10.5772/66711.